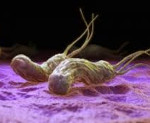
хеликобактериоз код по мкб 10
Другие уточненные инфекционные агенты как причина болезней, классифицированных в других рубриках (B98)
Алфавитные указатели МКБ-10
Внешние причины травм — термины в этом разделе представляют собой не медицинские диагнозы, а описание обстоятельств, при которых произошло событие (Класс XX. Внешние причины заболеваемости и смертности. Коды рубрик V01-Y98).
Лекарственные средства и химические вещества — таблица лекарственных средств и химических веществ, вызвавших отравление или другие неблагоприятные реакции.
В России Международная классификация болезней 10-го пересмотра (МКБ-10) принята как единый нормативный документ для учета заболеваемости, причин обращений населения в медицинские учреждения всех ведомств, причин смерти.
МКБ-10 внедрена в практику здравоохранения на всей территории РФ в 1999 году приказом Минздрава России от 27.05.97 г. №170
Выход в свет нового пересмотра (МКБ-11) планируется ВОЗ в 2022 году.
Сокращения и условные обозначения в Международой классификации болезней 10-го пересмотра
БДУ — без дополнительных уточнений.
НКДР — не классифицированный(ая)(ое) в других рубриках.
† — код основной болезни. Главный код в системе двойного кодирования, содержит информацию основной генерализованной болезни.
* — факультативный код. Дополнительный код в системе двойного кодирования, содержит информацию о проявлении основной генерализованной болезни в отдельном органе или области тела.
Helicobacter pylori (H.pylori)
Рубрика МКБ-10: B98.0
Содержание
Определение и общие сведения [ править ]
Первые сообщения о выявлении кислотоустойчивых спиралевидных организмов в желудке кошек и собак были опубликованы в конце XIX в. (1893-1896 гг.). Однако у людей аналогичные бактерии обнаружены только через 40 лет J. Doenges (1938). Еще через 2 года появились сообщения о связи спиралевидных бактерий с язвенной болезнью и опухолями желудка, но фактическое подтверждение и выделение культур возбудителя произошло только спустя 35 лет, тогда эти микроорганизмы были ошибочно идентифицированы как псевдомонады. В то время не уделялось внимания исчезновению уреазной активности в желудке после лечения больных тетрациклином.
Зависимость частоты инфицирования детей от благосостояния семьи и уровня образования матери подтверждена и в России.
Частота обнаружения HP у школьников существенно различается в разных странах и составляет в среднем 4,2% в Бельгии, 28,9% в Италии, 56% на островах Океании, 80,6% в Бенине, 84% в Индии, 63% в Чехии и 96% в Албании. Значение этнического фактора в распространенности HP-инфекции не доказано. Так, у турецких детей, проживающих на юге Турции и в Германии, уровень обсемененности HP составил 72 и 64%. Американские исследователи отмечают значительное преобладание HP-инфекции среди чернокожего населения США африканского происхождения.
Пути передачи инфекции недостаточно изучены.
Этиология и патогенез [ править ]
После попадания в желудок НР способен адаптироваться к новому хозяину и противодействовать иммунным механизмам элиминации благодаря мимикрии и генетической изменчивости. Последняя может быть обусловлена интеграцией ДНК от других штаммов НР с последующей инкорпорацией ее в свой геном. Генетический анализ штаммов НР, выделенных из биоптатов тела желудка пациентов с различными гастродуоденальными заболеваниями, показал, что изоляты существенно отличаются у пациентов, но остаются генетически стабильными в течение как минимум 4 лет.
Действие большинства факторов патогенности HP на чувствительные к ним мишени имеет общий характер:
• каталаза препятствует перевариванию фагоцитированных бактериальных клеток;
• фосфолипаза A гидролизует лецитины желчи с образованием цитотоксического лизолецитина;
• фосфолипаза A2 способствует снижению гидрофобности апикальной мембраны эпителиоцитов;
• фосфолипаза C обладает гемолитической активностью;
• протеазы оказывают неспецифическое деструктурирующее ткани воздействие;
• алкогольдегидрогеназа способствует образованию из эндо- и экзогенного этанола ацетальдегида, обладающего выраженной цитотоксичностью.
Иммунный ответ на инфекцию Helicobacter pylori
Изучение показателей местного и общего иммунного статуса у пациентов с HP-инфекцией показало, что у большинства больных наблюдались различные нарушения: снижение IgA, Т-лимфоцитов, особенно Т-хелперов, а также соотношения Тх/Тс, снижение выработки лизоцима, комплемента и фагоцитарной активности нейтрофилов. HP нарушает ответ антиген-специфических CD4+ CD25+ регуляторных клеток, с чем связывают более высокую степень поражения СОЖ. Токсин VacA, свойственный всем штаммам HP, ингибирует активацию Т-лимфоцитов через механизмы, зависимые от образования специфических анионных каналов, блокирующих транслокацию фактора транскрипции NFAT в ядро клетки, обеспечивающей сигнальную активацию CD4+ и CD8+ клеток. VacA ингибирует также внутриклеточную передачу сигнала через MKK3/6 и p38. Все эти данные указывают на способность VacA нарушать иммунный ответ на HP, позволяя возбудителю длительно персистировать и колонизировать СОЖ, обусловливая хроническое течение заболевания.
Клинические проявления [ править ]
Патогенная роль H. pylori в развитии заболеваний и клиническая картина описана в соответствующих рубриках:
1. Инфекция Helicobacter pylori и хронический гастрит;
2. Аутоиммунный гастрит и инфекция Helicobacter pylori;
3. Язвенная болезнь и инфекция Helicobacter pylori;
4. Инфекция Helicobacter pylori и проблема рака желудка;
6. Внежелудочные проявления инфекции Helicobacter pylori.
Helicobacter pylori (H.pylori): Диагностика [ править ]
За прошедшие с момента открытия HP годы разработано немало методов его диагностики, среди них есть инвазивные, требующие взятия биоптата СОЖ, и неинвазивные; прямые (идентифицирующие непосредственно микроорганизма или его антигены) и непрямые (идентифицирующие продукты его жизнедеятельности или антитела к нему). Существуют методы, проводимые in vitro в различных пробах (биоптате, крови, секретах) и in vivo после приема внутрь мочевины. Каждый из возможных методов имеет свои преимущества и недостатки, и «идеальный» метод до сих пор не найден. Именно поэтому в каждой ситуации выбор метода должен основываться на соотношении стоимости и эффективности и строго соответствовать поставленной задаче: скрининг, первичная диагностика или динамический контроль эффективности эрадикационной терапии. Выбор метода диагностики зависит и от условий проводимого исследования: необходимо учитывать возможность проведения эндоскопии и биопсии, оснащенность лаборатории, наличие необходимой техники и инструментов, подготовку медицинского персонала.
Дифференциальный диагноз [ править ]
Helicobacter pylori (H.pylori): Лечение [ править ]
Helicobacter pylori (хеликобактер пилори)

Заблуждения, связанные с Helicobacter pylori
Нередко, при обнаружении Helicobacter pylori, пациенты начинают беспокоиться об их эрадикации (уничтожении). Само наличие Helicobacter pylori в желудочно-кишечном тракте не является причиной для немедленной терапии с применением антибиотиков или других средств. В России количество носителей Helicobacter pylori достигает 70 % населения и подавляющее большинство из них не страдает какими-либо заболеваниями желудочно-кишечного тракта. Процедура эрадикации предполагает прием двух антибиотиков (например, кларитромицина и амоксициллина). У пациентов, имеющих повышенную чувствительность к антибиотикам, возможны аллергические реакции — от антибиотик-ассоциированной диареи (не тяжелое заболевание) до псевдомембранозного колита, вероятность возникновения которого мала, но процент летальных исходов большой. Кроме того, прием антибиотиков отрицательно воздействует на «дружественную» микрофлору кишечника, мочеполовых путей и способствует развитию резистентности к данному виду антибиотиков. Имеются данные, что после успешной эрадикации Helicobacter pylori в течение ближайших лет чаще всего наблюдается реинфекция слизистой желудка, которая уже через 3 года составляет 32±11 %, через 5 лет — 82–87%, а через 7 лет — 90,9% (Циммерман Я.С.).
Пока боль не проявилась, хеликобактериоз лечить не следует. Более того, у детей до восьмилетнего возраста вообще не рекомендуется проводить эрацикационную терапию, потому что у них иммунитет еще не сформирован, антитела к Helicobacter pylori не вырабатываются. Если у них провести эрадикацию до 8-летнего возраста, то через день, пообщавшись кратковременно с другими детьми, «схватят» эти бактерии (П.Л. Щербаков).
Helicobacter pylori однозначно требует эрадикации, если у больного имеется язва желудка или двенадцатиперстной кишки, МАLТома или если у него была резекция желудка по поводу рака. Многие авторитетные гастроэнтерологи (не все) в этот список включают также атрофический гастрит.
Эрадикация Helicobacter pylori может быть рекомендована для снижения риска развития рака желудка. Известно, что как минимум 90% случаев рака желука связаны с H. pylori-инфекцией (Старостин Б.Д.).
 |  |  |
| Helicobacter pylori от экспериментально моноинфицированных мышей (A), слизистой оболочки желудка человека (B) и культивированные на пластине агара (C). Как выделенных от экспериментально инфицированных мышей, так и при биопсии человека поверхность Helicobacter pylori является грубой, а жгутики имеют тенденцию склеиваться. За исключением коккоидной формы, морфология сравнительно хорошо сохраняется в культуре на агаре (С). Масштабные метки = 1 мкм. Источник: Stoffel M.H. et al. Distinction of Gastric Helicobacter spp. in Humans and Domestic Pets by Scanning Electron Microscopy / January 2001. DOI: 10.1046/j.1523-5378.2000.00036.x. Blackwell Science, 1083-4389/00/232–239. Inc. Volume 5 • Number 4 • 2000. | ||
Факторы вирулентности Helicobacter pylori
Язва двенадцатиперстной кишки, ассоциированная с Helicobacter pylori
Схемы эрадикации Helicobacter pylori
Всемирной организаций здравоохранения к активным препаратам в отношении Helicobacter pylori отнесены метронидазол, тинидазол, коллоидный субцитрат висмута, кларитромицин, амоксициллин и тетрациклин (Подгорбунских Е.И., Маев И.В., Исаков В.А.).

Эрадикация Helicobacter pylori не всегда достигает цели. Очень широкое и неправильное применение распространенных антибактериальных средств привело к повышению устойчивости к ним Helicobacter pylori. На рисунке справа (взято из статьи Белоусовой Ю.Б., Карпова О.И., Белоусова Д.Ю. и Бекетова А.С.) показана динамика резистентности к метронидазолу, кларитромицину и амоксициллину штаммов Helicobacter pylori, выделенных от взрослых (сверху) и от детей (снизу). Признано, что в разных странах мира (разных регионах) целесообразно применение разных схем. Ниже даны рекомендации по эрадикации Helicobacter pylori, изложенные в Стандартах диагностики и лечения кислотозависимых и ассоциированных с Helicobacter pylori заболеваний принятых Научным обществом гастроэнтерологов России в 2010 г. Выбор схемы эрадикации зависит от наличия индивидуальной непереносимости пациентами конкретных лекарств, а также чувствительности штаммов Helicobacter pylori к этим лекарствам. Применение кларитромицина в эрадикационных схемах возможно лишь в регионах, где резистентность к нему менее 15–20 %. В регионах с резистентностью выше 20 % его использование целесообразно только после определения чувствительности Helicobacter pylori к кларитромицину бактериологическим методом или методом полимеразной цепной реакции.
Антациды могут применяться в комплексной терапии в качестве симптоматического средства и в монотерапии — до проведения рН-метрии и диагностики Helicobacter pylori.
Первая линии антигеликобактерной терапии
Вариант 1. Один из ингибиторов протонной помпы (ИПП) в стандартной дозировке (омепразол 20 мг, лансопразол 30 мг, пантопразол 40 мг, эзомепразол 20 мг, рабепразол 20 мг) 2 раза в день и амоксициллин (500 мг 4 раза в день или 1000 мг 2 раза в день) в сочетании с кларитромицином (500 мг 2 раза в день), или джозамицином (1000 мг 2 раза в день), или нифурателем (400 мг 2 раза в день) в течение 10–14 дней.
Вариант 2. Лекарства, используемые при варианте 1 (один из ИПП в стандартной дозировке, амоксициллин в сочетании с кларитромицином, или джозамицином, или нифурателем) с добавлением четвертого компонента — висмута трикалия дицитрата 120 мг 4 раза в день или 240 мг 2 раза в день в течение 10–14 дней. 
Вариант 3 (при наличии атрофии слизистой оболочки желудка с ахлоргидрией, подтвержденной при рН-метрии). Амоксициллин (500 мг 4 раза в день или 1000 мг 2 раза в день) в сочетании с в сочетании с кларитромицином (500 мг 2 раза в день) или джозамицином (1000 мг 2 раза в день), или нифурателем (400 мг 2 раза в день), и висмута трикалия дицитрат (120 мг 4 раза в день или 240 мг 2 раза в день) в течение 10-14 дней.
Примечание. При сохранении язвенного дефекта по результатам контрольной эндоскопии на 10–14-й день от начала лечения рекомендовано продолжить терапию висмута трикалия дицитратом (120 мг 4 раза в день или 240 мг 2 раза в день) и/или ИПП в половинной дозе в течение 2–3 недель. Пролонгированная терапия висмута трикалия дицитратом показана также в целях улучшения качества послеязвенного рубца и скорейшей редукции воспалительного инфильтрата
Вариант 4 (рекомендуется только пожилым больным в ситуациях, при которых полноценная антигеликобактерная терапия невозможна):
а) ИПП в стандартной дозировке в сочетании с амоксициллином (500 мг 4 раза в день или 1000 мг 2 раза в день) и висмута трикалия дицитратом (120 мг 4 раза в день или 240 мг 2 раза в день) в течение 14 дней
б) висмута трикалия дицитрат по 120 мг 4 раза в день в течение 28 дней. При наличии болей — короткий курс ИПП.
Вариант 5 (при наличии поливалентной аллергии к антибиотикам или отказе больного от антибактериальной терапии). Один из ИПП в стандартной дозировке в сочетании с 30 %-ным водным раствором прополиса (100 мл 2 раза в день натощак) в течение 14 дней.
Вторая линия антигеликобактерной терапии
Выполняется при отсутствии эрадикации Helicobacter pylori после терапии первой линии.
Вариант 1. Один из ИПП в стандартной дозировке, висмута трикалия дицитрат по 120 мг 4 раза в день, метронидазол по 500 мг 3 раза в день, тетрациклин 500 мг 4 раза в день в течение 10–14 дней.
Вариант 2. Один из ИПП в стандартной дозировке, амоксициллин (500 мг 4 раза в день или 1000 мг 2 раза в день) в сочетании с нитрофурановым препаратом: нифурателем (400 мг 2 раза в день) или фуразолидоном (100 мг 4 раза в день) и висмута трикалия дицитрат (120 мг 4 раза в день или 240 мг 2 раза в день) в течение 10–14 дней.
Вариант 3. Один из ИПП в стандартной дозировке, амоксициллин (500 мг 4 раза в день или 1000 мг 2 раза в день), рифаксимин (400 мг 2 раза в день), висмута трикалия дицитрат (120 мг 4 раза в день) в течение 14 дней.
Третья линия антигеликобактерной терапии
При отсутствии эрадикации Helicobacter pylori после лечения второй линии рекомендуется подбор терапии только после определения чувствительности Helicobacter pylori к антибиотикам.
В последнее десятилетие разработано большое число различных схем эрадикации Helicobacter pylori. Некоторые схемы на основе висмута трикалия дицитрата имеются в статье «Де-нол».
По мнению некоторых исследователей, сегодня перспективной является гибридная терапия. Она включает 7-дневный курс ИПП (стандартная доза) и амоксициллина (1 г 2 раза в день) с последующим 7-дневным курсом четырехкомпонентной схемы с применением ИПП (стандартная доза), амоксициллина (1 г 2 раза в день), кларитромицина (500 мг 2 раза в день) и метронидазола (500 мг 2 раза в день) (Парцваниа-Виноградова Е.В.).
Рекомендации «Маастрихт IV» в отношении схем эрадикации H. pylori
В 1987 г. была основана Европейская группа по изучению инфекции H. pylori — European helicobacter pylori study group (EHSG), целью которой явилось содействие междисциплинарным исследованиям патогенеза H. pylori-ассоциированных заболеваний. По месту проведения первой согласительной конференции все соглашения называются Маастрихтскими. Четвертая согласительная конференция прошла во Флоренции в ноябре 2010 года. Выработка Guidelines (рекомендаций) по результатам этой конференции продолжалась два года. Схемы эрадикационной терапии в соответствии с консенсусом Маастрихт IV представлены на рисунке ниже (Маев И.В. и др.):
Материалы для профессионалов здравоохранения, касающиеся заболеваний, ассоциированных с Helicobacter pylori
Статьи, методические рекомендации
Видео
Кадр из видео: Шурпо Е.М. Хронический гастрит
(лекция для студентов медицинского университета)
Кадр «Методы диагностики Hp-инфекции» из видеолекции Е.В. Гостищевой «Анатомо-физиологические особенности органов пищеварения у детей. Методика и методы исследования пищеварительной системы у детей» для студентов Медицинской академии имени С.И. Георгиевского Крымского федерального университета имени В.И. Вернадского
Кадр «Диагностика Helicobacter pylori» из видеолекции Бурсикова А.В. «Клинические и дополнительные методы исследования ЖКТ» для студентов 2-го курса Ивановской государственной медицинской академии (ИвГМА)
На сайте GastroScan.ru в разделе «Видео» имеются подраздел для пациентов «Популярная гастроэнтерология» и подраздел «Для врачей», содержащий видеозаписи докладов, лекций, вебинаров по различным направлениям гастроэнтерологии для профессионалов здравоохранения.
Проведение эрадикации Helicobacter pylori у беременных и кормящих матерей
Распространённость Helicobacter pylori в разных странах и в России
По данным Всемирной гастроэнтерологической организации (Helicobacter pylori в развивающихся странах, 2010, WGO) более половины населения Земли является носителями Helicobacter pylori), при этом частота инфицированности значительно варьируется между различными странами, а также внутри этих стран. В целом, инфицированность возрастает с возрастом. В развивающихся странах инфицированность Helicobacter pylori значительно более выражена у лиц молодого возраста, чем в развитых странах.
ВГО приводит следующие цифры:
| Страна (регион) | Возрастные группы | Частота инфицированности |
|---|---|---|
| Европа | ||
| Восточная Европа | взрослые | 70 % |
| Западная Европа | взрослые | 30-50 % |
| Албания | 16-64 | 70,7 % |
| Болгария | 1-17 | 61,7 % |
| Чехия | 5-100 | 42,1 % |
| Эстония | 25-50 | 69 % |
| Германия | 50-74 | 48,8 % |
| Исландия | 25-50 | 36 % |
| Нидерланды | 2-4 | 1,2 % |
| Сербия | 7-18 | 36,4 % |
| Швеция | 25-50 | 11 % |
| Северная Америка | ||
| Канада | 5-18 | 7,1 % |
| Канада | 50-80 | 23,1 % |
| США и Канада | взрослые | 30 % |
| Азия | ||
| Сибирь | 5 | 30 % |
| Сибирь | 15-20 | 63 % |
| Сибирь | взрослые | 85 % |
| Бангладеш | взрослые | > 90 % |
| Индия | 0-4 | 22 % |
| Индия | 10-19 | 87 % |
| Индия | взрослые | 88 % |
| Япония | взрослые | 55-70 % |
| Австралия и Океания | ||
| Австралия | взрослые | 20 % |
Причиной разной инфицированности может быть социоэкономическое различие между популяциями. Заражение Helicobacter pylori в основном происходит орально-оральным или фекально-оральным путями. Отсутствие санитарии, безопасной питьевой воды, базовых понятий о гигиене, а также ограниченная диета и большое скопление населения, могут играть роль в высокой распространенности инфекции.
Россия относится к странам с очень высокой распространенностью хеликобактерной инфекции. В некоторых регионах, например, в Восточной Сибири, эта цифра превышает 90% и в монголоидной, и в европеоидной популяции. В Москве инфицированность Helicobacter pylori ниже. По данным ЦНИИ Гастроэнтерологии около 60% жителей ВАО Москвы – носители хеликобактера. Хотя в отдельных группах населения хеликобактер более распространен. В частности, среди работников промышленных предприятий Москвы инфицированы Helicobacter pylori 88 % (Бордин Д.С.).
Helicobacter pylori в систематике бактерий
Helicobacter pylori у животных
Helicobacter pylori в МКБ-10
Helicobacter pylori упоминается в «Классе I. Некоторые инфекционные и паразитарные болезни (A00-B99)» Международной классификации болезней МКБ-10, бактерия включена в блок «B95-B98 Бактериальные, вирусные и другие инфекционные агенты» и имеет код рубрики «B98.0 Helicobacter pylori [H. pylori] как причина болезней, классифицированных в других рубриках». Данный код предназначен для использования в качестве дополнительного, когда целесообразно идентифицировать инфекционных агентов болезней, классифицированных в других рубриках.
Хеликобактериоз
Хеликобактериоз — это латентное или манифестировавшее инфекционное заболевание, при котором слизистая желудка колонизируется хеликобактериями. Обычно протекает бессимптомно. При клинической манифестации проявляется болями, чувством тяжести и дискомфорта в эпигастрии, диспепсией, учащением дефекации. Для длительного течения характерны признаки анемизации: слабость, быстрая утомляемость, головокружения, головные боли. Диагностируется с помощью ИФА, ПЦР, дыхательного теста, эзофагогастродуоденоскопии и анализа биоптата. Стандартные схемы лечения предполагают назначение блокаторов протонного насоса, антибактериальных препаратов и солей висмута.
МКБ-10
Общие сведения
Инфицирование хеликобактерией (Helicobacter pylori) наблюдается почти у 60% населения планеты. По данным наблюдений в сфере клинической гастроэнтерологии, распространенность хеликобактериоза напрямую зависит от материального уровня жителей: в развивающихся государствах этот показатель выше, чем в развитых, в семьях с годовым доходом более 70 тыс. долларов инфицированность встречается спорадически.
Кислотоустойчивые бактерии были впервые выделены из слизистой желудка австралийскими учеными Дж. Уорреном и Б. Маршаллом в 1982 году. Наиболее часто хеликобактериоз выявляется после 60 лет, повышенной восприимчивостью к хеликобактерной инфекции обладают больные с ослабленным иммунитетом.
Причины хеликобактериоза
Заболевание вызывается микроаэрофильной грамотрицательной бактерией Helicobacter pylori, реже другими видами хеликобактера, тропными к желудочному эпителию и устойчивыми в кислотной среде. Источниками заражения являются пациенты, страдающие явным или латентным хеликобактериозом, носители микроорганизма, домашние и сельскохозяйственные животные, у которых высеиваются другие разновидности хеликобактерий (H. acinonychis, H. felis, H. salomonis, H. mustelae).
Основными путями инфицирования являются алиментарный и водный. Возможно контактно-бытовое заражение при пользовании общими с носителем или больным посудой, полотенцами, зубной щеткой и другими предметами личной гигиены. Новорожденным детям возбудитель хеликобактериоза чаще всего передается контактно-бытовым способом. Патоген отличается относительной устойчивостью к окружающей среде: при кипячении хеликобактерии гибнут практически мгновенно, при обработке дезинфицирующими составами — в течение нескольких минут.
Патогенез
Механизм развития хеликобактериоза определяется особенностями колонизации бактерией слизистой желудка. Инфицирующей считается доза патогена от 10 тыс. до 1 млрд. микробных тел. Хеликобактерии адгезируются к желудочным эпителиоцитам, скапливаясь преимущественно в межклеточных промежутках, с помощью жгутиков мигрируют к участкам выделения мочевины и гемина, необходимых для жизнедеятельности возбудителей. Расщепление мочевины микробной уреазой до аммиака и двуокиси углерода позволяет создать вокруг колонии слой, защищающий хеликобактера от соляной кислоты.
Аммиак, цитотоксины и высокоактивные энзимы (муциназа, липаза, протеаза), продуцируемые микробом, разрушают слизисто-бикарбонатный барьер и оказывают повреждающее воздействие на желудочный эпителий. В зависимости от состояния защитных факторов желудка возникший инфекционный процесс может протекать латентно с минимальными патоморфологическими изменениями слизистой или остро с инфильтрацией эпителиальной оболочки, активацией системы простагландинов, выраженной клинической симптоматикой воспаления.
Хронический гастрит с инфильтрацией лимфоцитами антрального эпителия является продолжением острого процесса или следствием активации возбудителя при снижении иммунитета у пациентов с первично-латентной формой хеликобактериоза. Значительный дисбаланс между недостаточным защитным действием слизисто-бикарбонатного слоя и высокой агрессивностью желудочного сока приводит к формированию язвы желудка, дисплазии эпителиоцитов. Поражение двенадцатиперстной кишки и пищевода возможно только при желудочной метаплазии их эпителия.
Симптомы хеликобактериоза
Почти у 90% пациентов инфицирование H. pylori длительное время протекает бессимптомно и выявляется при обследовании по поводу других болезней ЖКТ. В случае быстрой первичной манифестации возбудителя у больных развивается острый период хеликобактериоза, который длится около 10 дней. Основными жалобами являются периодические боли в эпигастральной области, чувство тяжести, дискомфорта после приема пищи, тошнота. Может наблюдаться учащение дефекации, изменение характера стула. Пациенты жалуются на отрыжку, изжогу и вздутие живота.
Общее состояние больных обычно остается удовлетворительным, иногда отмечается кратковременный субфебрилитет, снижение работоспособности. После стихания острых проявлений хеликобактериоза отмечается периодический абдоминальный дискомфорт, тошнота и снижение аппетита. При хроническом течении заболевания и атрофическом поражении слизистой желудка возникают признаки анемии — частые головные боли и головокружения, бледность кожных покровов, снижение АД и тахикардия.
Осложнения
Наиболее частое последствие хеликобактериоза — усиление выработки соляной кислоты и гастрина, снижение факторов защиты, приводящее к возникновению хронического гастрита типа В. По мере прогрессирования заболевания формируются участки атрофии слизистой оболочки желудка, снижается кислотность. Хеликобактерная инфекция является причиной 95% язв двенадцатиперстной кишки, 80% язв желудка. В современных исследованиях доказана связь патологии с развитием гастроэзофагеальной рефлюксной болезни.
При хеликобактериозе снижается выработка внутреннего фактора Касла, что нарушает всасывание витамина В12 и вызывает мегалобластную анемию. При этом у пациентов, кроме типичных признаков анемии, возникают патогномоничные симптомы — лакированный язык, фуникулярный миелоз (поражение периферической нервной системы). Наиболее опасное осложнение патологии — метаплазия и дисплазия атрофированной слизистой, значительно повышающая риск рака желудка.
Диагностика
Постановка диагноза хеликобактериоза во время клинического осмотра пациента затруднена, что объясняется полиморфностью и неспецифичностью жалоб. Диагностический поиск включает комплексную лабораторно-инструментальную оценку состояния желудочно-кишечного тракта больного. Наиболее информативными для диагностики являются такие методы, как:
Дифференциальная диагностика
В первую очередь дифференциальную диагностику заболевания проводят с функциональной диспепсией. Основными диагностическими критериями, свидетельствующими в пользу хеликобактериоза, являются наличие воспалительных изменений слизистой желудка и двенадцатиперстной кишки, выявление H. Pylori с помощью инвазивных методов исследования. В остром периоде болезнь нужно дифференцировать с кишечными инфекциями. Кроме гастроэнтеролога для обследования пациента привлекают инфекциониста.
Лечение хеликобактериоза
Выбор тактики зависит от клинического течения патологии. Выявленным носителям инфекции рекомендовано наблюдение. При развитии на фоне хеликобактерной инфекции гастрита, язвы желудка или двенадцатиперстной кишки, желудочной MALT-лимфомы назначается одна из трехкомпонентных, четырехкомпонентных или усеченных схем эрадикации хеликобактера. Консервативное лечение обычно длится 10-14 дней. С учетом решений Маастрихтских согласительных конференций и рекомендаций Научного общества гастроэнтерологов России для терапии хеликобактериоза могут применяться:
Прогноз и профилактика
Исход заболевания зависит от обратимости морфологических изменений слизистой ЖКТ и своевременности начатого лечения. У пациентов без сопутствующей патологии, прошедших полный курс антихеликобактерной терапии, прогноз благоприятный: возможна полная санация эпителия, нормализация кислотности. Профилактика хеликобактериоза включает соблюдение правил личной гигиены, рациональный режим питания (прием пищи 4-5 раз в день, исключение жареной, очень острой еды, копченостей), лабораторное обследование людей, которые были в контакте с инфицированным H. Pylori.