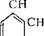
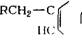Алкилсульфонат натрия что это такое
Алкилсульфат/лаурилсульфат натрия
Алкилсульфат натрия (натриевая соль алкилсульфата фракции С12-С14) является водным раствором поверхностно – активных веществ (ПАВ) анионного типа.
Сферы применения алкилсульфата /лаурилсульфата натрия
Алкилсульфаты (лаурилсульфаты натрия) активно используются в качестве компонентов при изготовлении:
Благодаря оптимальному соотношению цены и качества алкилсульфат натрия (ВЖC) С12-С14 является отличным заменителем для аналогов российского и зарубежного производаства: АБСК, Texapon, Hostapur, и т.д.
Физико-химические показатели алкилсульфатов / лаурилсульфата натрия
Нормативное значение показателя
Внешний вид при 20-25 °С
Однородная прозрачная подвижная жидкость от желтого до коричневого цвета без механических примесей
Водородный показатель (рН)
Концентрация, %, не менее
Массовая доля веществ, растворимых в петролейном эфире, %
Алкилсульфат натрия (лаурилсульфат натрия) является малоопасным веществом, относящимся к IV-му классу опасности согласно ГОСТ 12.1.007.
В ходе использования алкилсульфата натрия вторич¬ные опасные соединения не образуются.
Сброс алкилсульфата натрия (лаурилсульфата натрия) в производственные сточные воды допускается при условии разбавления его водой до предельно-допустимой концентрации ПАВ 20 мг/дм³ по активному веществу.
Важно! Работа с алкилсульфатом натрия (лаурилсульфатом натрия) предполагает обязательное использование средств индивидуальной защиты кожи и слизистой оболочки глаз. При контакте вещества с кожей или слизистыми место соприкосновения следует тщательно промыть водой.
Транспортировка и хранение
Хранение алкилсульфатов (лаурилсульфатов натрия) рекомендуется осуществлять при температуре выше 0 °С. Однако в случае неоднократного замерзания и последующего оттаивания вещество не теряет своих первоначальных слов.
Поставки осуществляются в полиэтиленовых канистрах объемом от 5 до 30 л, а также пластиковых или металлических бочках по 200—225 кг.
Срок хранения: 12 месяцев со дня изготовления при соблюдении надлежащих условий транспортировки и хранения.
Согласно классификации ГОСТ 19433 вещество не относится к опасным грузам и может транспортироваться всеми видами транспорта.
Алкилсульфаты натрия
Описание
Синонимы: Sodium alkyl sulfate, SAS
В целом, алкилсульфаты – класс органических соединений, объединенных наличием общей функциональной группы, обычно имеющих структуру R-O-SO3−. Иными словами алкилсульфаты натрия – это натриевые соли сульфоэфиров высших органических спиртов с различной длиной алкильной цепи. Первичные алкилсульфаты были и остаются одним из преобладающих типов среди синтетических анионных ПАВ. Один из наиболее известных представителей – лаурилсульфат натрия: CH3(CH2)11OSO3Na.
Основной способ получения первичных алкилсульфатов заключается в сульфатировании первичных спиртов с последующей нейтрализацией реакционной массы растворами гидроксидов натрия, аммиака или магния.
Алкилсульфаты натрия это дифильные органические соединения, которые, диссоциируя в воде, образуют анион с длинным углеводородным радикалом – носителем поверхностной активности; катион при этом не является поверхностно-активным.
Алкилсульфаты натрия выпускаются как в виде моносоединений с заданной длиной углеводородного радикала – октилсульфаты, децилсульфаты; так и в виде композиций, включающих радикалы различной длины. Алкилсульфаты натрия – малоопасное вещество. IV класс опасности по ГОСТ 12.1.007–76.
Характеристики
| Наименование | TDS | Химическое описание | Внешний вид при 20оС | Плотность при 20оС, г/см3 | Содержание активной основы, % масс. | рН 3% водного раствора |
|---|---|---|---|---|---|---|
| Syntapon O | Октилсульфат натрия | прозрачная желтоватая жидкость | 1,10 | 40,5 ± 0,5 | 9,5 – 11,5 | |
| Syntapon OD | Алкилсульфат (С8–10) натрия | прозрачная желтоватая жидкость | 1,09 | 43 ± 2 | 9,5 – 11,5 | |
| Syntapon NU | Алкилсульфат (С9–11) натрия | прозрачная желтоватая жидкость | 1,06 | 37 ± 1 | 8,0 – 10,0 | |
| Syntapon DS-P | Децилсульфат натрия | прозрачная желтоватая жидкость | 1,02 | 36 ± 1 | 8,0 – 10,0 | |
| Syntapon DS | Алкилсульфат (С10–12) натрия | прозрачная желтоватая жидкость | 1,02 | 36 ± 1 | 8,0 – 10,0 |
Упаковка:
— Полиэтиленовые бочки вместимостью до 220 литров
— Полимерные емкости вместимостью до 1000 литров или автоцистерны из нержавеющей стали
* По согласованию с потребителем допускается использование других видов тары.
Свойства алкилсульфонатов
Анализ анионоактивных ПАВ – соединений, которые в водных растворах диссоциируют с образованием анионов (отрицательно заряженных ионов), обусловливающих поверхностную активность. Методы синтеза алкилсульфонатов. Получение алкилсульфонатов сульфоокислением.
| Рубрика | Химия |
| Вид | реферат |
| Язык | русский |
| Дата добавления | 04.10.2017 |
| Размер файла | 74,5 K |
Отправить свою хорошую работу в базу знаний просто. Используйте форму, расположенную ниже
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Размещено на http://www.allbest.ru/
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
Казанский национальный исследовательский технологический университет
Кафедра «Технологии основного органического и нефтехимического синтеза»
магистрант кафедры ТООНС
Кандидат химических наук,
доцент кафедры ТООНС
Все поверхностно-активные вещества делится на четыре класса: анионоактивные, катионоактивные, неионогенные и амфолитные.
На долю анионоактивных из всех производимых ПАВ приходится более 70%. Среди них наибольшее значение имеют алкилбензолсуль-фонаты натрия, алкилсульфонаты натрия и алкилсульфаты натрия. Алкилбензолсульфонатами называются соли сульфокислот ароматических соединений, алкилсульфатами-соли сульфоэфиров спиртов и алкилсульфонатами- соли сульфокислот алканов.
Методы синтеза алкилсульфонатов:
1. Фотохимическое сульфохлорирование смеси, содержащей не менее 98,5% парафинов СП-С18, выделяемых из керосиновой фракции нефти.
2. Фотохимическое сульфоокисление парафинов смесью газов SO2 и О2:
Реакцию проводят при УФ-облучении в реакторах при непрерывном введении воды в реакционную зону для экстракции образующихся сульфокислот. Полученную смесь отделяют от непрореагировавших парафинов, непрерывно возвращаемых в реактор. Низкая конверсия парафинов (ок. 1%) обеспечивает низкое содержание побочных дисульфонатов. Полученный этим способом алкансульфонат (сульфонат-SO), содержащий 60% алкансульфонатов и 7-8% дисульфонатов, эмульгатор при синтезе полимеров.
Все алкансульфонаты малотоксичны; их биоразлагаемость ок. 100%.
Алкилсульфаты-представляют собой натровые соли сульфоэфиров высших жирных спиртов. Алкилсульфаты получают сульфатированием жирных спиртов с последующей нейтрализацией полученного сульфопродукта.
Жирные спирты получают различными способами:
1) метод гидрогенизации жирных кислот;
2) метод прямого окисления парафиновых углеводородов в присутствии борной кислоты;
3) сульфирование жирных спиртов.
Алкилсульфонаты. Представляют собой натровые соли сульфокислот жирного ряда, содержащие в цепи 12-18 углеродных атомов. Сырьем для получения алкилсульфонатов служат естественные и синтетические углеводороды, содержащие 14-22 атома углерода (фракции прямогонного нефтяного керосина или гидрированного синтина, выкипающие в пределах 240-300 С).
Алкилсульфонаты можно получить двумя способами: сульфохлорированием или сульфоокислением алифатических углеводородов. Сулоьфохлорирование производится при действии на углеводороды газообразного сернистого ангидрида и хлора. Реакция ускоряется такими катализаторами, как перекисные соединения. Для успешного течения реакции необходимо облучение реакционной смеси коротковолновым светом. Обработкой едкой щелочью (15-20%-ный раствор) образовавшиеся сульфохлориды переводят в алкилсульфонаты. Получающийся готовый продукт получил название «Сульфонат», он используется для приготовления синтетических моющих средств типа «Астра», «Новость» и др. Технология получения алкилсульфонатов сравнительно проста, характеризуется низкими капитальными затратами, а сырьевая база практически не ограничена.
Получение алкилсульфонатов сульфохлорированием н-парафинов.
Серная кислота не реагирует с парафинами. Алкилсульфохлориды и алкилсульфокислоты на основе высших парафинов получают сульфохлорированием и сульфоокислением.
CnH2n+2+ SO2 + Cl2 > CnH2n+1SO2Cl2 +HCl
CnH2n+2+ SO2 + Cl2 > CnH2n (SO2Cl)2 +2HCl
CnH2n+2+ SO2 + Cl2 > CnH2n+1Cl +HCl+ SO2
CnH2n+2+ SO2 + Cl2 > CnH2n+1SO2Cl +HCl
Для подавления реакции хлорирования парафинов процесс ведут при небольшом избытке диоксида серы (10%) и температуре 20-30єC. С повышением температуры резко увеличиваются выход хлорпарафинов. Для устранения образования нежелательных дисульфохлоридов реакцию проводят при степени превращения сырья 30-40%. Реакция сульфохлорирования сильно экзотермическая реакция и протекает по радикально-цепному механизму. Зарождение цепи происходит за счет гомолитического расщепления Cl2 при поглощении кванта света:
RSґO2 +Cl2> RSґO2Cl+Clґ
В производственных условиях цепь обрывается при столкновении радикалов со стенками реактора, а также из-за наличия примесей в сырье. Применяют непрерывное освещение реакционного пространства ртутно-кварцевыми лампами.
При сульфохлорировании н-парафинов получаются преимущественно вторичные сульфохлориды, в которых сульфогруппа находятся при любом вторичном атоме углерода. Сырьем является фракция парафинов с пределом кипения 230-320єC, 250-300єC, 250-350єC. В этих фракциях, в основном, присутствуют парафины фракции С15. Присутствие олефинов и ароматических углеводородов в сырье нежелательно, т.к. они ингибируют цепную реакцию. При этом парафины предварительно подвергают гидроочистке на сульфидных катализаторах. В качестве сульфохлорирующих агентов применяет SO2 и Cl2 с содержанием основных веществ не менее 95%.
Для получения алкилсульфонатов используют керосиновые фракции. Процесс осуществляют непрерывным способом. В стальную колонну футерованную винипластом подают сверху керосин, а снизу смесь газообразных хлора и диоксида серы. Реакцию проводят при облучении массы ртутными лампами. Сульфохлорирование ведут при 25-30єC, для съема тепла реакционную массу прокачивают через выносной холодильник. По окончании реакции массу омыляют 10%-ным раствором NаOH. Омыление проводят непрерывным способом при 95-97єC:
RSO2Cl + 2NаOH > RSO2ONа + NаCl + H2O
Неомыляемые отделяют от раствора при 95 єC. После отделения неомыляемых раствор охлаждают до 5 єС, при этом отделяют раствор поваренной соли. Раствор сульфоната после отделения NаCl упаривают при 160-170 єC и получают плавленый сульфонат в виде чешуек или пасты. Образовавшиеся алкилхлориды дегидрохлорируют в присутствии оксидных катализаторов и получают олефины. Олефины используют для получения б-олефинсульфонатов или фторалкилсульфонатов:
алкилсульфонат синтез сульфоокисление
Получение алкилсульфонатов сульфоокислением н-парафинов
Недостатком сульфохлорирования является использование хлора.
Сырьем для сульфоокисления служат те же фракции парафинов С14-С18
что и для сульфохлорирования. требование к сырью то же что и для SO2 и Cl2.
RH + SO2 + 0,5O2 > RSO2OH
В результате реакции образуются вторичные алкансульфокислоты со статическим распределением сульфогрупп по углеродной цепи. Нейтрализация приводит к образованию алкилсульфонатов натрия:
RSO2OH +NаOН > RSO2ONа+ H2O
Реакция сильно экзотермическая. Этот процесс приобретает большое значение в связи с хорошей биоразлагаемостью алкилсульфонатов. Процесс протекает по радикально-цепному механизму.
Свободный радикал, образовавшийся при зарождении цепи, начинает цепь превращений:
Сульфопероксид является стабильным. При введении в реакционную смесь воды сульфогидропероксид окисляется диоксид серы в серную кислоту, одновременно превращаясь в сульфокислоту (водно-световой метод).
RSO2OОH + SO2+ Н2O > RSO2OН + H2SO4
Суммарное уравнение реакции:
RH + 2SO2+ О2 +Н2O > RSO2OН + H2SO4
При водно-световом методе процесс ведут при 25-30єC в одну стадию при непрерывном облучении УФ светом, экстрагируя серную кислоту и сульфокислоту водой.
Существенным недостатком является большой расход световой энергии.
Другой метод-это сульфоокисление в присутствии уксусного ангидрида. Процесс протекает в две стадии. На первой стадии сульфоокисление проводят при освещении в безводной среде, но в присутсвии уксусного ангидрида, связывающего сульфогидропероксид в ацетилсульфопероксид, стабильный к разложению:
RSO2ОOН+(СН3СО)2О > RSO2OО(О)ССН3 + СH3СООН
Вторая стадия протекает без освещения и при более высокой температуре, при которой ацетилсульфопероксид распадается и инициирует радикально-цепной процесс сульфоокисления:
Одновременно протекают побочные реакции с образованием различных продуктов окисления.
При сульфоокислении Н-парафинов С12-С18 образуется смесь с равновероятным расположением сульфокислотной группы при всех вторичных атомах углерода.
Алкилсульфонаты, полученные сульфохлорированием или сульфоокислением н-парафинов, представляет собой смесь изомерных алкилсульфонатов, в которых сульфонатная группа SO3Nа занимает разные положения в углеродной цепи.
Высокоэффективный антистатик длительного действия для полистирола и его сополимеров. Они разрешены к применению в пищевой упаковке, но основное применение находят в производстве товаров народного применения.
Алкиларилсульфонаты. Представляют собой натровые соли алкиларилсульфокислот, являются наиболее распространенными моющими веществами. В нашей стране алкиларилсульфонаты производят в основном в виде алкилбензолсульфонатов (сульфонолы).
Производство сульфонола складывается из следующих стадий:
а) очистка керосина от ароматических углеводородов путем экстракции последних диэтиленгликолем;
б) фотохимическое хлорирование очищенного керосина;
г) сульфирование алкилбензола производится раствором серного ангидрида SO в жидком сернистом ангидриде SO при пониженной температуре (10С), так как процесс сульфирования протекает с большим выделением тепла;
д) нейтрализация полученных алкилбензолсульфокислот раствором каустической соды (20%-ный раствор). Температура нейтрализации не должна превышать 45-550С;
е) отделение несульфируемых и упаривание водных растворов сульфонола.
Выпускаемый в настоящее время хлорный сульфонол в виде 30%-ного раствора (по активному веществу) хорошо зарекомендовал себя для производства синтетических моющих порошков.
Смесь натриевых солей алкилсульфоновых кислот с длиной цепи алкильного радикала С11-С18, полученного из
Паста от белого до светло-желтого цвета. Однородная по составу после подогрева до температуры 50°С и перемешивания.
Эмульгатор, поверхностно-активное вещество для получения синтетических моющих средств.
Обогреваемые железнодорожные цистерны, бочки из коррозионно-стойкой стали.
Железнодорожным и автотранспортом.
Хранить в резервуарах, внутренняя поверхность которых защищена покрытием, исключающим контакт металла с продуктом.
Малотоксичен, обладает слабо выраженными раздражающими свойствами. Защищать кожные покровы.
Производство и поставка в России:
1. Торгово-Промышленная Компания «ИНФРАХИМ»
2. ООО «ВППК» Волжская Производственно Промышленная Компания
Список использованных источников
6. Кузнецов Е. В., Прохорова И. Я., Файзулина Д. Л. Альбом технологических схем производства полимеров и пластмасс на их основе. Изд. 2-е. М., Химия, 1976.
7. Лосев И. Л., Тростянская Е. Б. Химия синтетических полимеров. Изд. 3-е. М., Химия, 1971.
Размещено на Allbest.ru
Подобные документы
Особенности получения наночастиц серебра методом химического восстановления в растворах. Принцип радиационно-химического восстановления ионов металлов в водных растворах. Образование золей металла. Изучение влияния рН на величину плазмонного пика.
курсовая работа [270,7 K], добавлен 11.12.2008
Физико-химические свойства германия и его соединений. Его электродные потенциалы в водных растворах. Электроосаждение германия и его сплавов. Получение гидрида германия. Электрохимическое поведение соединений германия. Растворимость германия в ртути.
дипломная работа [53,0 K], добавлен 15.04.2008
Реакции, протекающие между ионами в растворах. Порядок составления ионных уравнений реакций. Формулы в ионных уравнениях. Обратимые и необратимые реакции обмена в водных растворах электролитов. Реакции с образованием малодиссоциирующих веществ.
презентация [1,6 M], добавлен 28.02.2012
Практические выводы теории электролитической диссоциации. Характеристика основных реакций, которые протекают в растворах электролитов. Анализ свойств амфотерных гидроксидов, образование малодиссоциированных соединений, комплексных соединений и газов.
лабораторная работа [27,6 K], добавлен 17.12.2014
Исследование зависимости выхода по току от потенциала для бромид-ионов, их концентраций в растворах при совместном присутствии. Анализ методики электрохимического окисления иодид-ионов при градуировке. Описания реактивов, растворов и средств измерения.
дипломная работа [213,7 K], добавлен 25.06.2011
Лако-красочные материалы — производство
Технологии и оборудование для изготовления красок, ЛКМ
АНИОНАКТИВНЫЕ МОЮЩИЕ ВЕЩЕСТВА
Представляют наиболее распространенные моющие вещества, к которым относятся:
1. Алкилкарбонаты (R— COONa)
А) первичные (R — S03Na)
4. Алкиларилсульфонаты (RArS03Na)
Алкилкарбонаты. Представляют собой соли жирных кислот или мыла, которые достаточно подробно описаны выше. Мыла условно можно отнести к синтетическим моющим веществам, учитывая, что сырьем для них служат синтетические жирные кислоты (СЖК).
Алкилсульфаты. Представляют собой натровые соли сульфо — эфиров высших жирных спиртов. В молекуле алкилсульфата сера связана с углеродом через кислород: н О
Различают первичные и вторичные алкилсульфаты. У первичных алкилсульфатов моющая способность возрастает с увеличением количества углеродных атомов в алкильном остатке и достигает оптимума (при температуре до 40° С) у алкилсульфатов с 12—14 атомами углерода. Алкилсульфаты с 16 и более углеродными атомами в цепи очень плохо растворимы в воде (при 20° С) и при взаимодействии с жесткой водой образуют малорастворимые кальциевые соли.
Получение алкилсульфатов. Алкилсульфаты получают суль- фатированием жирных спиртов с последующей нейтрализацией полученного сульфопродукта.
Жирные спирты получают различными способами.
В отличие от других стран, где для производства жирных спиртов, как правило, применяют кокосовое масло и животные жиры, в СССР производство жирных спиртов базируется на продуктах окисления парафина. Кроме того, в связи с расширением добычи кашалотов для производства жирных спиртов используется кашалотовый жир. Производство жирных спиртов из кашалотового жира разработано советскими учеными и проводится на Казанском химическом комбинате имени Вахитова по оригинальной технологии (омыление кашалотового жира под давлением в автоклавах, отгонка с паром образовавшихся жирных спиртов от мыла, конденсация спиртов, разложение мыла). На базе полученных жирных спиртов были синтезированы алкилсульфаты, а затем в 1953 г. впервые изготовлен отечественный синтетический моющий порошок «Новость», одобренный потребителями. В последнее время на одном из комбинатов освоен разработанный группой советских ученых и специалистов метод получения жирных спиртов из кашалотового жира путем гидрогенизации жирных кислот, находящихся в составе восков, и триглицеридов при высоком давлении (300 ат) И температуре 300° С. Применяемый цинково-хромовый катализатор способствует сохранению двойных связей, что обеспечивает максимальное содержание непредельных жирных спиртов в готовом продукте.
Методы производства жирных спиртов в СССР базируются на продуктах окисления парафина.
Метод гидрогенизации жирных кислот. Этот метод получил наибольшее распространение не только в нашей стране, но и за рубежом. Нужная фракция жирных кислот этерифицируется метиловым спиртом по схеме:
RCOOH + СН3ОН——— >- RCOOCH3 + Но О
Полученные метиловые эфиры жирных кислот подвергаются гидрогенизации в автоклавах под давлением 300 ат с применением плавающего катализатора
RCOOCH3 + 2Н2 ————— ► RCH2OH + СН3ОН
Образовавшиеся жирные спирты освобождаются от метилового спирта и катализатора, а затем дистиллируются.
Метод прямого окисления парафиновых углеводородов в присутствии борной кислоты. Этот метод впервые в мировой практике разработан в 1948 г. под руководством проф. Башкирова А. Н.
Сырьем служит синтин или мягкие парафины (фракции 275—320° С). Окисление ведется при температуре 165—170°С; борная кислота, являющаяся катализатором, связывает образующиеся спирты в виде эфиров и предохраняет их от дальнейшего окисления.
По этому методу получают в основном вторичные жирные спирты с распределением гидроксильной группы по всей длине углеводородной цепи.
Метод извлечения жирных спиртов изнеомы — ляемых-П. При окислении парафина до жирных кислот попутно образуются другие кислородсодержащие продукты, в том числе жирные спирты (в основном первичные). В неомы — ляемых-II содержится до 8% жирных спиртов от расходуемого на окисление парафина, их можно извлечь различными способами.
Сульфирование жирных спиртов. Для получения синтетических моющих веществ из жирных спиртов их подвергают сульфированию. При этом образуются не истинные суль — фокислоты, а сульфоэфиры.
Реакция сульфирования в общем виде может быть выражена следующим уравнением:
Группа — S02C1 присоединяется к любому атому углерода по всей длине цепи. Поэтому в результате реакции сульфохлорирования образуется смесь изомеров.
Обработкой едкой щелочью (15—207о-ный раствор) образовавшиеся сульфохлориды переводят в алкилсульфонаты:
Алкилсульфонаты могут быть получены и при помощи сульфо — окисления (открыто Платтом в 1940 г.)
Получающийся при указанных способах готовый продукт получил название «Сульфонат», он используется для приготовления синтетических моющих средств типа «Астра», «Новость», «Синтол». Технология получения алкилсульфонатов сравнительно проста, характеризуется низкими капитальными затратами, а сырьевая база практически неограниченна.
В течение 1961 —1962 гг. в Советском Союзе был разработан синтез и освоено промышленное производство нового синтетического моющего вещества ДНС (динатровая соль сульфоян — тарной кислоты), которое условно можно отнести к алкилсуль — фонатам. Структурная формула ДНС такова: ROCOCHo — СН —COONa
Жирные спирты (С14 — С18) реагируют с малеиновым ангидридом*, а затем обрабатываются бисульфитом натрия. При этом образуется динатровая соль моноалкилсульфоянтарной кислоты **. Процесс протекает по следующей схеме:
Производство ДНС представляет особый интерес для промышленности Советского Союза. В СССР интенсивно развивается производство высших жирных кислот и спиртов, получае-
|| о — очень реакционноспособное соединение.
** Сульфоянтарная кислота НООС—СН2—СН — СООН
Впервые получена Фелингом в 1841 г. сульфированием янтарной кислоты серным ангидридом.
Мых путем окисления твердых и жидких парафинов. Так как при этом получаются в основном вторичные спирты, то степень превращения их в алкилсульфаты при сульфировании серной кислотой не превышает 45—70%.
В отличие от весьма жестких условий сульфирования синтез ДНС осуществляется в мягких условиях с 92—95%-ным выходом продукта и практически не сопровождается побочными реакциями. Моющее действие средств на основе ДНС для хлопчатобумажных, шерстяных и шелковых тканей достаточно высоко.
Как на основе одних ДНС, так и в смеси с другими моющими веществами выпускаются такие моющие средства, как «Новость-С», «Ладога» и др.
Алкиларилсульфонаты. Представляют собой натровые соли алкиларилсульфокислот» общей формулы: R—Ar—S03Na. Алкиларилсульфонаты являются наиболее распространенными моющими веществами. В настоящее время объем мирового производства синтетических моющих веществ превысил 2 млн. т В год. Примерно три четверти из них составляют анионактив — ные вещества, среди которых первое место занимают алкиларилсульфонаты. В нашей стране алкиларилсульфонаты производят в основном в виде алкилбензолсульфонатов (суль- фонолы).
В СССР сульфонол получают двумя способами: хлорным и бесхлорным (сульфонолы нефтяной промышленности).
Сульфонол хлорный производится на основе керосиновой фракции нефти, выкипающей в пределах 200—300° С.
Производство сульфонола складывается из следующих стадий:
А) очистка керосина от ароматических углеводородов путем экстракции последних диэтиленгликолем;
Б) фотохимическое хлорирование очищенного керосина по схеме:
R-CHo———— СН2СН3 + С12 —————- RCH,————— СН2СН2С1 + НС1
В) алкилирование бензола хлорированным керосином в присутствии катализатора — безводного А1С13
R-CH2 [СГ+Н] С F C I 1-,ю-Я5° у R — С112—С ^jj СН + НС1
Г) сульфирование алкилбензола производится раствором серного ангидрида S03 в жидком сернистом ангидриде S02 при пониженной температуре (10°С), так как процесс сульфирования протекает с большим выделением тепла
Д) нейтрализация полученных алкилбензолсульфокислот раствором каустической соды (20%-ный раствор). Температура нейтрализации не должна превышать 45—55° С.
RCH2— Ci^SGH RCH2—Cif^lCH
е) отделение несульфируемых и упаривание водных растворов сульфонола.
Выпускаемый в настоящее время хлорный сульфонол в виде 30%-ного раствора (по активному веществу) хорошо зарекомендовал себя для производства синтетических моющих порошков.
Сульфонолы нефтяной промышленности (НП)—выпускают нескольких различных видов: НП-1, НП-2, НП-3, БиТ.
Рассмотрим получение сульфонола НП-1 (додецилбензол- сульфоната): С12н25
Исходным сырьем для получения сульфонола НП-1 служат пропилен и бензол. В начале производится полимеризация пропилена на фосфорнокислом катализаторе с образованием доде — цилена (тетраметра пропилена) по схеме:
Условия полимеризации: давление 75—80 ат, температура 180—235° С.
Затем производится алкилирование бензола додециленом в присутствии А1С13 при температуре 55—60° С.