Аномалия мвс что это
Аномалия мвс что это
а) Терминология:
1. Сокращения:
• Мезиальный височный склероз (МВС)
2. Синонимы:
• Склероз аммонова рога, склероз гиппокампа (СГ)
3. Определение:
• Связанная с судорожным синдромом потеря нейронов гиппокампа и смежных структур в сочетании с их глиозом
1. Общие характеристики мезиального височного склероза:
• Лучший диагностический критерий:
о Основные особенности: аномальное повышение интенсивности сигнала на Т2-ВИ от гиппокампа, уменьшение его объема/его атрофия, нечеткость его внутренней архитектоники строения о Вторичные признаки: атрофия ипсилатерального отдела свода мозга и ипсилатерального сосцевидого тела, расширение ипсилатеральных височного рога бокового желудочка и хориоидальной щели
о Дополнительные признаки: потеря пальцев головки (ножки) ипсилатерального гиппокампа, атрофия белого вещества парагиппокампальной извилины, ↑ интенсивности сигнала от белого вещества переднего отдела височной доли на Т2-ВИ
• Локализация:
о Мезиальные отделы височной доли(ей), в 10-20% случаев двустороннее поражение
о Гиппокамп > миндалина > свод мозга > сосцевидные тела
• Размеры:
о ↓ объема гиппокампа от легкой до выраженной степени
• Морфология:
о Аномальные форма, размер пораженного гиппокампа
2. КТ признаки мезиального височного склероза:
• Бесконтрастная КТ
о Обычно нормальная картина; КТ-нечувствительный для диагностики МВС метод
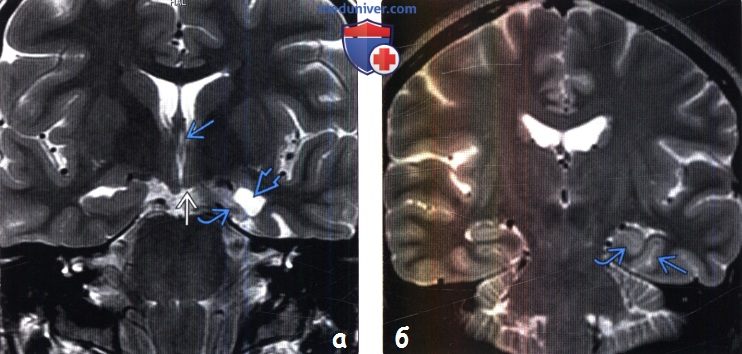
(б) МРТ, Т2-ВИ, корональный срез: у пациента с эпилепсией отмечается вертикальное расположение левой коллатеральной борозды и шарообразная форма гиппокампа Данные распространенные варианты строения могут быть ошибочно приняты за склероз гиппокампа.
3. МРТ признаки мезиального височного склероза:
• Т1-ВИ:
о ↓ размера гиппокампа
о Отсутствие нормальной дифференцировки между серым и белым веществом в гиппокампе
о ± атрофия гомолатеральных отделов свода мозга, ипсилатерального сосцевидного тела
о Волюмометрия гиппокампа: ↑ чувствительность к выявлению МВС (особенно двустороннего МВС)
• Т2-ВИ:
о Атрофия гиппокампа
о Нечеткость внутренней архитектоники строения гиппокампа
о ↑ интенсивности сигнала от гиппокампа
о ± атрофия ипсилатеральных отделов свода мозга, ипсилатерального сосцевидного тела, расширение височного рога ипсилатерального бокового желудочка
о ± аномальное повышение интенсивности сигнала, снижение объема в переднем отделе ипсилатеральной височной доли
• FLAIR:
о Повышение интенсивности сигнала от измененного гиппокампа
• ДВИ:
о ↑ интенсивности сигнала на ДВИ (эффект «Т2-просвечивания»)
о ↑ коэффициента диффузии на ИКД карте
• Постконтрастные Т1-ВИ
о Контрастное усиление отсутствует
• МР-спектроскопия:
о ↓ пика NAA в гиппокампе, височной доле
о При ↓ NAA/Cho и ↓ NAA/Cho+Cr предполагайте МВС
о ± пик лактат/липиды через 24 часа после длительного судорожного приступа
4. Ангиография мезиального височного склероза:
• Предоперационный тест Вада: нейропсихологическоетестирование после интракаротидной инъекции амобарбитала (амитала):
о Определение латерализации функции памяти и языковых/ре-чевых функций
о Позволяет прогнозировать постоперационную потерю памяти, осуществимость самой операции
о Может быть полезен для определения латерализации судорог при начале приступа
• ФМРТ-картирование заменяет тест Вада
5. Радионуклидная диагностика:
• ПЭТ с ФДГ: гипометаболизм в измененных мезиальных отделах височной доли
• ОФЭКТ: гипоперфузия (в межприступный период) или гиперперфузия (во время приступа) в эпилептогенной зоне:
о Чувствительность: во время приступа > в межприступный период
6. Рекомендации по визуализации:
• Лучший инструмент визуализации:
о Высокоразрешающая МРТ
о МР-спектроскопия, волюмометрия могут быть полезны в определении латерализации МВС в трудных случаях
• Совет по протоколу исследования:
о Тонкосрезовые корональные Т2-ВИ и FLAIR-изображении (3 мм), расположенные перпендикулярно длинной оси гиппокампа
о Тонкосрезовые корональные 3D SPGR-изображения (1-2 мм), расположенные перпендикулярно длинной оси гиппокампа
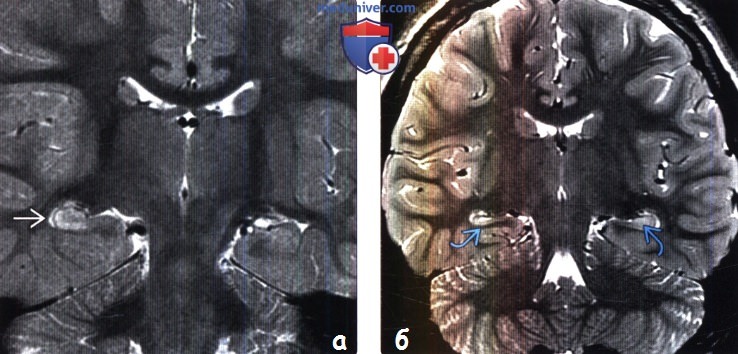
(б) МРТ, Т2-ВИ, корональный срез: у пациента с длительной сложной парциальной эпилепсией определяется повышение интенсивности сигнала от гиппокампов со снижением их объема (больше справа), что соответствует мезиальному височному склерозу.
в) Дифференциальная диагностика мезиального височного склероза:
1. Эпилептический статус:
• Множественные судорожные приступы или эпилептический статус в клиническом анамнезе
• Временное повышение интенсивности сигнала на Т2-ВИ ± гиральный характер контрастирования в пораженных участках коры, гиппокампе
2. Астроцитома низкой степени злокачественности:
• Гиперинтенсивное объемное образование в белом веществе височной доли (обычно не накапливающее контрастное вещество)
• ± характерны судорожный синдром, молодой взрослый возраст
3. Киста хориоидальной щели:
• Асимптоматическая киста хориоидальной щели, имеющая ликворную интенсивность сигнала и вызывающая изменение нормальной архитектоники строения гиппокампа:
о Округлая форма на аксиальных, корональных срезах
о Овальная форма, расположение параллельно длинной оси височной доли на сагиттальных срезах
• Отсутствие аномального повышения интенсивности сигнала от мезиальных отделов височной доли на Т2-ВИ
4. Остаток борозды гиппокампа:
• Нарушение нормальной инволюции гиппокампальной борозды →
• асимптоматическая киста между зубчатой извилиной и аммоновым рогом
• Часто встречающийся (в 10-15% случаев) вариант нормы
5. Кавернозная мальформация:
• Гетерогенное гиперинтенсивное поражение, имеющее структуру по типу «попкорна», окруженное темным замкнутым кольцом отложения гемосидерина
• ± судорожный синдром
6. Дисэмбриопластические нейроэпителиальные опухоли (ДНЭО):
• Объемное образование «пенистой» структуры с вариабельным характером накопления контраста, расположенное в коре ± регионарная кортикальная дисплазия
• Сложные парциальные судорожные приступы
7. Кортикальная дисплазия:
• Наиболее частая сочетанная патология, связанная с МВС
• Повышение интенсивности сигнала на Т2-ВИ от белого вещества передних отделов височных долей
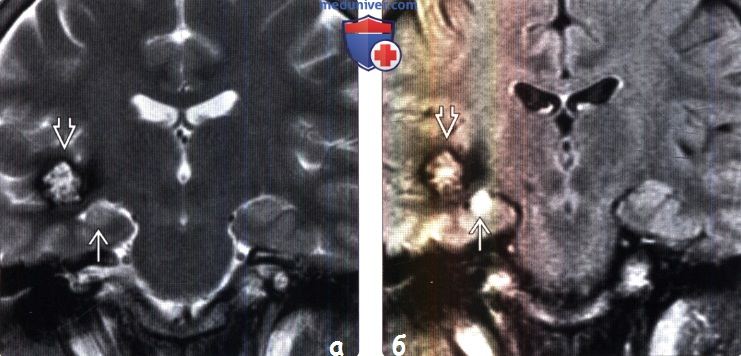
(б) МРТ, FLAIR, корональный срез: у того же пациента с кавернозной мальформацией в правой височной доле лучше визуализируются признаки склероза гиппокампа. Повышение интенсивности сигнала обычно более заметно на FLAIR, в то время как Т2-ВИ позволяет более информативно оценить внутреннюю архитектонику строения гиппокампа.
г) Патология мезиального височного склероза:
1. Общие характеристики мезиального височного склероза:
• Этиология:
о Противоречивые данные о том, является ли данное состояние приобретенным или формируется в процессе развития:
— Приобретенный генез: возникает после сложных фебрильных судорог, эпилептического статуса, энцефалита
— Формирование в процессе развития: в 15% случаев обнаруживается сопутствующее нарушение развития
— Гипотеза «двойного удара»: первый-изначально провоцирующее повреждение (такое как сложный судорожный приступ), второй повышенная восприимчивость (такая как генетическая предрасположенность, аномалии развития)
— В большинстве случаев МВС является исходом как приобретенных, так и связанных с развитием процессов
о Фебрильные судороги (ФС) наиболее часто наблюдаются среди детей (2-5%):
— Продолжительные ФС могут приводить к острому повреждению гиппокампа → с последующей его атрофией
• Генетика:
о Имеются сообщения о семейных случаях мезиальной височной эпилепсии (ВЭ), ФС
о Недавние исследования предполагают, что взаимосвязь между ФС и поздним дебютом эпилепсии может быть генетически детерминированой
о Связь с синдром-специфичными генами ФС (каналопатии) наблюдается в небольшом количестве случаев ФС
• Ассоциированные аномалии:
о Сопутствующее нарушение развития (15%)
2. Макроскопические и хирургические особенности:
• У гиппокампа в норме анатомически выделяют головку (ножку), тело и хвост:
о Подразделяются на аммонов рог, зубчатую извилину, гиппокампальную борозду, бахромку, лоток, основание, парагиппокампальную извилину, коллатеральную борозду
• Атрофия мезиального отдела височной доли: тело (88%), хвост (61 %), головка (51 %) гиппокампа, миндалина (12%)
• Отсутствие кровоизлияния или некроза
3. Микроскопия:
• Хронический астроглиоз с густой фибриллярной сетью ядер астроцитов и сниженное количество сохранных нейронов
• Аммонов рог, cornu ammonis (СА) содержит четыре зоны гранулярных клеток: СА1, СА2, САЗ, СА4:
о Слои пирамидных клеток в зонах СА1, СА4 наиболее подвержены ишемии
о Во всех областях гиппокампа может наблюдаться вариабельная потеря нейронов
д) Клиническая картина:
1. Проявления мезиального височного склероза:
• Наиболее частые признаки/симптомы:
о Сложные парциальные судорожные приступы, автоматизмы:
— Простые в более молодом возрасте с нарастанием сложности и дискретности приступов с возрастом
• Другие признаки/симптомы:
о Возможно прогрессирование до генерализованных тонико-клонических судорог
• Клинический профиль:
о Часто имеются анамнестические данные о фебрильных или резистентных к медикаментозной терапии судорогах в детском возрасте
— При наличии сложных или продолжительных фебрильных судорог в анамнезе ↑ риск развития повреждения гиппокампа, МВС
о Поверхностная электро- (ЭЭГ) или магнитоэнцефалография (МЭГ) полезна для определения локализации эпилептогенного очага (60-90%)
о Интракраниальная ЭЭГ (субдуральная или с глубоким расположением электродов) может быть показана в случае противоречивых результатов неинвазивных исследований
2. Демография:
• Возраст:
о Заболевание детей более старшего возраста, молодых взрослых
• Пол:
о Отсутствие гендерной предрасположенности
• Эпидемиология:
о МВС наблюдается у большинства пациентов, которым по поводу эпилепсии была выполнена височная лобэктомия
3. Течение и прогноз:
• Передняя височная лобэктомия эффективна в 70-95% случаев, если поданным МРТ наблюдаются признаки МВС
• Передняя височная лобэктомия эффективна в 40-55% случаев, если поданным МРТ наблюдается нормальная картина
• ↓ эффективности хирургического лечения при вовлечении в патологический процесс миндалины
е) Диагностическая памятка:
1. Обратите внимание:
• Наиболее частая причина сложной парциальной эпилепсии у взрослых
• Двустороннее поражение наблюдается в 10-20% случаев; трудно обнаружить без волюмометрии, за исключением тяжелых случаев
2. Советы по интерпретации изображений:
• Корональные Т2-ВИ, FLAIR-изображения с высоким разрешением наиболее чувствительны для диагностики МВС
• Двойная сочетанная патология в 1 5%
• У детей новообразования низкой степени злокачественности и кортикальная дисплазия являются наиболее частой причиной возникновения сложной парциальной эпилепсии (по сравнению с МВС)
ж) Список литературы:
1. Azab М et al: Mesial Temporal Sclerosis: Accuracy of NeuroQuant versus Neuroradiologist. AJNR Am J Neuroradiol. ePub, 2015
2. HamelinSetal: Revisiting hippocampal sclerosis in mesial temporal lobe epilepsy according to the «two-hit» hypothesis. Rev Neurol (Paris). 171 (3 ):227—3 5, 2015
3. French JA et al: Can febrile status cause hippocampal sclerosis? Ann Neurol. 75(2): 173—4, 2014
4. Thom M: Review: Hippocampal sclerosis in epilepsy: a neuropathology review. Neuropathol Appl Neurobiol. 40(5):520—43, 2014
5. Blumcke I et al: Defining clinico-neuropathological subtypes of mesial temporal lobe epilepsy with hippocampal sclerosis. Brain Pathol. 22(3):402—1 1, 2012
6. Malmgren К et al: Hippocampal sclerosis-origins and imaging. Epilepsia. 53 Suppl 4:19-33, 2012
Редактор: Искандер Милевски. Дата публикации: 2.5.2019
ВРОЖДЕННЫЕ АНОМАЛИИ РАЗВИТИЯ МОЧЕВЫДЕЛИТЕЛЬНОЙ СИСТЕМЫ — ОСНОВА ДЛЯ РАЗВИТИЯ ИНФЕКЦИИ МОЧЕВЫХ ПУТЕЙ
Д.К. Жумадиллаева
ГКП на ПХВ Городская поликлиника №4, врач педиатр
Целью работы было выявление удельного веса врожденных пороков развития мочевой системы у детей, состоящих на диспансерном учете с диагнозом хронический пиелонефрит. Из 30 диспансерных больных ВПРМВС составили 26.8%, все случаи ВПРМВС выявлены при обращении по поводу ИМС. Пиелонефриты на фоне ВПРМВС имели более тяжелое, рецидивирующее и хроническое течение. Выявлены основные причины: позднее обращение, низкий уровень санитарно-просветительной работы среди населения. Библиографий: 4
Ключевые слова: ИМВП, ВПРМВС, ПМР, гидронефроз
Аномалии развития почек и мочевыводящих путей являются основой для развития микробно-воспалительных заболеваний мочевыделительной системы. ( 2).
Целью нашего исследования было выявление удельного веса врожденных пороков развития мочевой системы среди детей, состоящих на диспансерном учете с хроническим обструктивным пиелонефритом. Анализ проведенный в течение последних 3 лет показал, что удельный вес детей с врожденной почечной патологией составил 26.8% из числа обследованных больных. Структура врожденных пороков составила: нефроптоз 50%, пузырно-мочеточниковый рефлюкс (ПМР) – 30.1%, гидронефроз- 9.4%,, агенезия, немая почка 2.1%, поликистоз — 1.6%, полное и неполное удвоение ЧЛС 0.56%.
Для диагностики применяли основные методы исследования (4): общий анализ крови и мочи, анализ мочи по Нечипоренко, бакпосев мочи, биохимический анализ крови, УЗИ и рентгеноурологические методы исследования, при «немой» почке, показаны ретроградная пиелография, почечная ангиография. Данные обследования показали, что более 50% детей имели нефроптоз. Наиболее часто встречающимися пороками развития мочевыделительной системы являются: пузырно-мочеточниковый рефлюкс и гидронефроз почек. Возраст обследованных детей от 1.5 месяцев до 15 лет. Все они обследованы в стационарах при поступлении впервые с диагнозом ИМВП, повторные исследования проводились при повторных госпитализациях и частично амбулаторно.
Пузырно-мочеточниковый рефлюкс (ПМР) – это аномалия развития пузырно-мочеточникового соустья, приводящая к ретроградному току мочи из нижних в верхние отделы мочевого тракта составила у наблюдаемых нами детей 30.1%. У новорожденных без признаков аномалии развития обычно диагностируется 1-2 степень ПМР. Данное состояние носит транзиторный характер и может подвергаться регрессии в течение первого года жизни. При 3-4-5 степени ПМР при раннем начале правильного комплексного лечения регрессия отмечается только в 40% случаях (3).
В зависимости от степени заброса рентгеноконтрастного вещества и дилатации полостей МВС ПМР делится на 5 степеней: 1 степень – заброс контрастного вещества только в мочеточник; 2 степень – заброс контрастного вещества в мочеточник, лоханку и чашечки без дилатации и изменений со стороны форниксов; 3 степень – незначительная или умеренная дилатация мочеточника и лоханки при отсутствии или склонности к образованию прямого угла форниксами; 4 степень – умеренная дилатация мочеточника, его извилистость, умеренная дилатация лоханки и чашечек, обусловленность острого угла форниксами; 5 степень – выраженная дилатация и извилистость мочеточника, выраженная дилатация лоханки и чашечек, у большинства чашечек сосочковость не прослеживается.
ПМР не имеет характерной клинической картины, выявляется в 100% случаях на фоне инфекции мочевыводящих путей, часто сочетается с гидронефрозом, поликистозом, аплазией и гипоплазией почки. Комплексная консервативная терапия является эфективной при ПМР 1-2 степени, 3-5 степени — являются показанием для оперативного лечения.
Гидронефроз (1) – обструктивная уропатия, стойкое, прогрессирующее расширение почечной лоханки и чашечек на почве нарушения оттока мочи в пиелоуретеральном сегменте за счет стеноза, сдавливания добавочным сосудом, клапаном слизистой мочеточника – чаще врожденного характера. К приобретенным причинам гидронефроза относятся: мочекаменная болезнь, опухоли, рубцевание мочеточника в результате воспалительного процесса. У наблюдаемых нами детей удельный вес гидронефроза составила 9.4%.
При гидронефрозе различают 4 стадии патологического процесса (1,2): 1 стадия – прегидронефроз – пиелоэктазия; 2 и 3 стадия – это собственно гидронефроз с большим или меньшим сохранением функций почки; 4 стадия – гидронефроз с резким истончением ткани паренхимы и полной потерей функциональной способности пораженного органа. При 1 стадии лечение комплексное, консервативное: стимуляция оттока мочи, лечение пиелонефрита, физиолечение, массаж. Если нет эффекта – хирургическое лечение. При 2-3-4 стадиях – органосохраняющие операции, направленные на восстановление пиелоуретерального сегмента, иногда нефрэктомия. У 100% детей гидронефроз диагностируется на фоне инфекции мочевыводящих путей.
1.Врожденные пороки развития мочевыделительной системы не редкая патология у детей и составляет 26.8% среди детей с ИМВП состоящих на диспансерном учете.
2.Микробно–воспалительные заболевания у детей на фоне ПМР и гидронефроза имели более тяжелые, рецидивирующие и хронические течения, осложнились хронической почечной недостаточностью у двоих (6.6%), оперативному лечению подверглись 3 детей (10%).
3.Учитывая высокую частоту врожденных пороков развития мочевой системы и частое наслоение инфекции, участковым педиатрам и родителям необходимо быть внимательнее к неоднократным жалобам ребенка на боли в животе, пояснице, утомляемость, наличие субфебрильной температуры без катаральных явлений, особенно в семьях с отягощенным нефроурологическим анамнезом.
4.Необходимо проводить таким детям анализ мочи и УЗИ исследования органов брюшной полости с целью раннего выявления и лечения врожденных пороков развития и наслоившейся инфекции мочевыделительной системы, а также для профилактики осложнений.
5.Низок уровень санитарно-просветительной работы среди населения по патологии мочевыделительной системы.
1 Садыкова В.Б., Лобанова Р.П., Аманбаева Л.А., Алпысбаева С.Д. Гидронефроз почек у детей. В материалах научно-практической конференции «Проблемы педиатрии: Стратегия развития и перспективы». – Алматы:2002. — C. 138-139
2 Столова Э.Н. Частота парциальной обструкции при врожденных аномалиях почек и мочевыводящих путей. Материалы Международной научно-практической конференции «Актуальные вопросы детской нефрологии и урологии» (13-14 октября 1998 г). — Алматы: 1998. – 65 c.
3 Папаян А.В., Аничкова И.В. «Пузырно-мочеточниковый рефлюкс и рефлюкс – нефропатия» Руководство для врачей «Клиническая нефрология детского возраста». –СПб.: Сотис,1997. — С. 529-544.
4 Кенжебаева К.А. и др. «Ранняя диагностика врожденных пороков развития мочевыделительной системы у новорожденных детей». Материалы научно-практической конференции «Актуальные вопросы детской нефрологии и урологии» (13-14 октября 1998 г.). – Алматы: С. 38-40.
5 Автор: Жумадиллаева Д.К. ГКП на ПХВ Городская поликлиника №4, врач педиатр.
Факторы риска и вероятность возникновения острой почечной недостаточности у детей с врожденными пороками развития мочевыделительной системы

В статье представлен ретроспективный анализ анамнестических и клинико-лабораторных данных 42 историй болезни детей пролеченных в отделении патологии новорожденных с 2015 по 2019 г. Исследуемая группа новорожденных имела врожденные пороки развития мочевыде
Abstract. The article presents a retrospective analysis of anamnestic and clinical and laboratory data of 42 case histories of children treated in the neonatal pathology department from 2015 to 2019. The study group of newborns had congenital malformations of the urinary system (CAKUT), the rest of the children made up the control group. The study was carried out on the basis of the regional perinatal center in Kursk. A comprehensive assessment of risk factors for the occurrence of malformations of the urinary system in newborns, a study of renal function in this group of patients using physical, laboratory and instrumental examinations, indicating the presence or absence of acute renal failure (ARF), was carried out. All newborns from the moment of birth to discharge from the hospital were under dynamic observation, the data of which were studied retrospectively from the records in the clinical history of the disease. The main indicators that were most thoroughly studied during the analysis were those that reflect the condition of the child in the presence of congenital malformations of the urinary system and satisfy the criteria for the diagnosis of acute renal failure. The data of obstetric and gynecological history of mothers, the presence of concomitant pathology in newborns, Apgar score at birth, clinical manifestations of renal failure (presence of pastiness, edema, microcirculation disorders, etc.), birth weight, general blood test data were analyzed urine, biochemical blood test, acid-base state for the first 7 days of life. The study identified the main risk factors leading to the development of congenital malformations in CAKUT (chorioamnionitis, intrauterine infection in early gestation, gestational arterial hypertension, toxoplasmosis, rubella, transferred during pregnancy), and also assessed the likelihood of developing acute renal failure in this category of newborns.
Резюме. В статье представлен ретроспективный анализ анамнестических и клинико-лабораторных данных 42 историй болезни детей пролеченных в отделении патологии новорожденных с 2015 по 2019 г. Исследуемая группа новорожденных имела врожденные пороки развития мочевыделительной системы (ВПР МВС), остальные дети составили группу контроля. Исследование проводилось на базе областного перинатального центра г. Курска. Проведены комплексная оценка факторов риска в возникновении пороков развития мочевыделительной системы у новорожденных, исследование функции почек у данной группы пациентов с помощью физикального, лабораторного и инструментального обследования, указывающих на наличие или отсутствие острой почечной недостаточности (ОПН). Все новорожденные с момента рождения до выписки из стационара находились под динамическим наблюдением, данные которого изучались ретроспективно по записям в клинической истории болезни. Основными показателями, наиболее тщательно изучаемыми в процессе анализа, были те, которые отражают состояние ребенка при наличии у него ВПР МВС и удовлетворяют критериям диагноза ОПН. Были проанализированы данные акушерско-гинекологического анамнеза матерей, наличие сопутствующей патологии у новорожденных, оценка по шкале Апгар при рождении, клинические проявления почечной недостаточности (наличие пастозности, отеков, нарушений микроциркуляции и т.д.), масса тела при рождении, данные общего анализа крови, мочи, биохимического анализа крови, кислотно-щелочного состояния за первые 7 суток жизни.
В ходе исследования были выявлены основные факторы риска, приводящие к развитию ВПР МВС (хориоамнионит, внутриутробное инфицирование на ранних сроках гестации, гестационная артериальная гипертензия, токсоплазмоз, краснуха, перенесенные во время беременности), а также оценена вероятность развития ОПН у данной категории новорожденных.
Врожденные пороки развития (ВПР) мочевыделительной системы (МВС) – это устойчивые анатомические аномалии развития органа, возникшие под действием тератогенных факторов или генетических мутаций. Данная патология составляет 15–17% в структуре пренатально диагностируемых ВПР [1, 8].
При наличии ВПР почек и обструктивных уропатий, входящих в состав CAPUT-синдрома, возможно снижение почечной функции, которая в настоящее время обозначается терминами «хроническая болезнь почек» (ХБП) или «терминальная почечная недостаточность». В случае возникновения острого повреждения почек (ОПП) при наличии ХБП необходимо использовать формулировку «ОПП на фоне ХБП» [9].
Из-за отсутствия должного уровня функциональных возможностей почек у новорожденных с ВПР МВС существует высокая вероятность развития у них острой почечной недостаточности (ОПН) [7].
ОПН – полиэтиологический синдром, проявляющийся резким снижением почечной функции, способствующий накоплению продуктов азотистого обмена, нарушению водно-электролитного и кислотно-щелочного состояния [9]. К основным причинам развития ОПН у новорожденных детей относят артериальную гипотензию, асфиксию, тяжелые инфекционные заболевания, применение нефротоксических препаратов, тромбоз почечных сосудов [2, 9].
Существует три основных патогенетических механизма развития ОПП: преренальный, ренальный и постренальный [4].
В основе преренального повреждения лежат снижение системного кровотока при кровотечениях вследствие отслойки плаценты и кровоизлияниях во внутренние органы, обеднение большого круга кровообращения при наличии ВПР сердца, тяжелые асфиксии, оперативные вмешательства.
Ренальное ОПП возникает при нарушении структуры и функциональных возможностей почечной паренхимы под действием нефротоксических средств, а также при длительном сохранении преренального или постренального повреждения.
При постренальном механизме повреждения существует ВПВ МВС (сужение уретры, пузырно-мочеточниковый рефлюкс и т. д.), за счет которого возникает обструкция и повышение гидростатического давления в нефронах с последующим повреждением паренхимы почек [4].
Целью данного исследования было проведение комплексной оценки факторов риска возникновения пороков развития МВС у новорожденных; исследование функции почек у данной группы пациентов с помощью физикального, лабораторного и инструментального обследования, указывающих на наличие или отсутствие ОПН.
Материалы и методы исследования
Исследование проводилось на базе областного перинатального центра г. Курска. Объектом анамнестического и клинико-лабораторного исследования были 42 истории болезни детей, пролеченных в отделении патологии новорожденных с 2015 по 2019 г. Ультразвуковое исследование органов МВС проводилось на аппарате Toshiba Xario.
Пациенты, включенные в исследование в зависимости от клинического диагноза, были разделены на 2 группы: первая – 21 ребенок с ВПР МВС, вторая – группа контроля. Критерием включения в группу контроля стало отсутствие у новорожденных каких-либо ВПР.
Все новорожденные с момента рождения до выписки из стационара находились под динамическим наблюдением, данные которого изучались ретроспективно по записям в клинической истории болезни.
Основными показателями, наиболее тщательно изучаемыми в процессе анализа, были те, которые отражают состояние ребенка при наличии у него ВПР МВС и удовлетворяют критериям диагноза ОПН [4].
Так, в обеих группах анализировали данные акушерско-гинекологического анамнеза матерей, наличие сопутствующей патологии у новорожденных, оценки по шкале Апгар при рождении, клинические проявления почечной недостаточности (пастозность, отеки, нарушения микроциркуляции и т. д.), массу тела при рождении, данные общего анализа крови, мочи, биохимического анализа крови, кислотно-щелочного состояния за первые 7 суток жизни.
В соответствии с поставленными целями обе группы пациентов сопоставлялись по представленным выше данным.
Статистическая обработка полученных результатов проводилась с помощью программы Statistica 10: были определены p-значения для двух и более сравниваемых групп с использованием критерия χ2 Пирсона, вычислены средние значения.
Результаты и их обсуждение
По данным результатов УЗИ (аппарат Toshiba Xario) в первой группе исследуе-мых детей зарегистрированы следующие ВПР МВС: гипоплазия и гиперплазия почек, атрезия, агенезия, удвое-ние почки, субкапсулярные кисты, L-образная почка, кистозная дисплазия, пиелэктазия, гидронефроз, мегауретер (рис.).
У четырех новорожденных (18%) выявлены сочетанные пороки развития МВС, у двух (9%) ВПР МВС сопровождались ВПР желудочно-кишечного тракта, центральной нервной системы (ЦНС), костно-мышечной и сердечно-сосудистой системы. Частота встречаемости патологии ЦНС оказалась высокой как в исследуемой группе, так и в группе контроля. Так, церебральная ишемия 1–2 степени выявлена в обеих группах и составила 20 (95%) и 15 (71,43%) соответственно; синдром двигательных нарушений 12 (57,14%) и 8 (66%). Наличие внутриутробной пневмонии отмечено в обеих группах и равно 12 (57,14%).
Для выявления факторов риска, которые могли повлиять на возникновение ВПР МВС, проведен сравнительный анализ акушерско-гинекологического анамнеза матерей детей из двух исследуемых групп (табл. 1): достоверных различий в количестве беременности и родов не выявлено. В группе 1 отмечено 8 случаев внутриутробного инфицирования плода на ранних сроках гестации (38%), по 5 случаев хориоамнионита, синдрома задержки развития плода (СЗРП) и гестационной артериальной гипертензии (АГ) (23%) как возможных факторов риска развития ВПР МВС. Обнаружено, что перенесенный токсоплазмоз и краснуха (TORCH-инфекция) также являются ключевыми факторами, приводящими к появлению ВПР у детей.
.gif)
При анализе массы тела отмечено, что в группе с ВПР МВС доля детей, у которых этот показатель был низким, выше, чем в группе контроля. Средняя масса тела в первой группе составила 2750,3 г, в контрольной – 3437 г.
При оценке диуреза у новорожденных с ВПР МВС выявлена олигурия и, как ее следствие, – пастозность и периферические отеки у 19 (90%) исследуемых детей из группы с пороками развития. Зависимость частоты случаев возникновения периферических отеков от наличия пороков развития МВС статистически значима.
Проанализированы лабораторные показатели: анализ крови, мочи, биохимический анализ крови и кислотно-щелочное соотношение (табл. 2). В клиническом анализе крови явных различий между группами не было.
Из данных (табл. 2) можно отметить, что средние значения лабораторных показателей креатинина и мочевины в исследуемых группах различны. В 1-й группе уровень креатинина на 20 мкмоль/л превышает показатели в контрольной группе. Уровень мочевины у детей с ВПР МВС выше, чем во 2-й второй группе, и составляет в среднем 6,1 ммоль/л.
На основании проекта клинических рекомендаций по ОПП у новорожденных (от 29.04.2019) критериями ОПН является возрастание концентрации креатинина в сыворотке крови на 26,5 мкмоль/л в течение 48 часов или увеличение в 1,5 раза уровня креатинина от известного значения в течение 7 дней [4].
При детальном анализе показателей каждого новорожденного из группы с ВПР МВС выявлено, что вышеуказанным критериям ОПН соответствуют показатели только одного ребенка.
В первые сутки жизни уровень креатинина у него составил 41 мкмоль/л, а на седьмые сутки достиг 186 мкмоль/л, что составляет 1,5 раза от известного уровня креатинина. Концентрация креатинина у остальных новорожденных из группы с ВПР МВС повышалась на 3–4 мкмоль/л в течение 48 часов, что не удовлетворяло критериям ОПН.
Таким образом, нами проведена комплексная оценка факторов риска развития ВПР МВС у детей; исследованы функции почек в заданных группах для выявления критериев, указывающих на наличие или отсутствие ОПН.
Литература/References
И. Г. Хмелевская, доктор медицинских наук, профессор
О. Г. Бец 1
А. Г. Архипова
ФГБОУ ВО КГМУ Минздрава России, Курск, Россия
Факторы риска и вероятность возникновения острой почечной недостаточности у детей с врожденными пороками развития мочевыделительной системы/ И. Г. Хмелевская, О. Г. Бец, А. Г. Архипова
Для цитирования: Лечащий врач № 9/2020; Номера страниц в выпуске: 7-10
Теги: почечная недостаточость, мутации, тератогенные факторы
.gif)
.gif)