Что показывает узи малого таза у женщин при климаксе
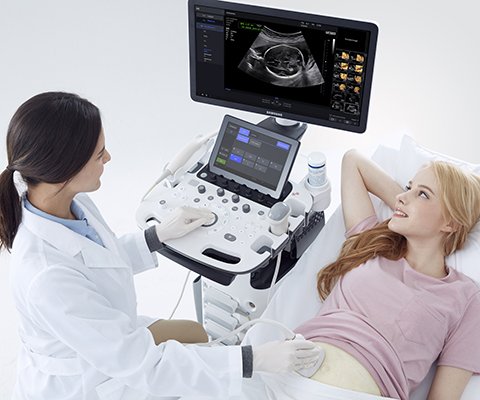
Что показывает УЗИ малого таза?
Рассказываем, о различных видах УЗИ малого таза — обследования, с помощью которого врачи ищут отклонения в работе органов мочевыделительной и половой систем.
Из-за безопасности и высокой точности ультразвуковое исследование очень часто используют для обследования органов, расположенных между тазовыми костями. В первую очередь органов мочеполовой системы. УЗИ малого таза показывает органы в динамике, что упрощает диагностику и позволяет довольно легко найти отклонения в работе.
Когда врач назначит УЗИ малого таза?
Пациенты обоих полов проходят ультразвуковые исследования малого таза при подозрениях на болезни мочевыделительной системы: мочекаменную болезнь, новообразования в мочеточниках, цистит и другие. Осмотреть органы с помощью аппарата УЗИ можно как через брюшную стенку, так и ректально. В некоторых случаях, второй способ предпочтительней: например, если из-за недержания нельзя наполнить мочевой пузырь для подготовки к осмотру.
Однако, чаще УЗИ малого таза назначают при проблемах в половой сфере: бесплодии, болях, импотенции, новообразованиях. Для пациентов разного пола врачи используют различные типы УЗИ, которые лучше всего позволяют рассмотреть больные органы.
Какие существуют типы УЗИ?
Из-за разницы в анатомии мужчин и женщин, есть несколько типов ультразвукового исследования малого таза. Одни можно применить для пациентов обоих полов, другие — только для женщин или только для мужчин.
Женщинам обычно назначают полное УЗИ малого таза, и за одно обследование они проходят и трансабдоминальный, и трансвагинальный осмотр.
Мужчины на этой процедуре обычно проверяют только простату (при помощи трансректального обследования), а для осмотра мочевого пузыря им, как правило, назначаются отдельные УЗИ.
Особенности женского УЗИ
Вариантов, когда врачи назначают УЗИ органов малого таза много:
Кроме того, УЗИ малого таза также назначают перед операциями над соседними органами — прямой кишкой, мочевым пузырём, почками, поджелудочной железой.
Наиболее точные результаты даст трансвагинальное УЗИ — оно помогает диагностировать практически все заболевания женской половой системы:
Беременные часто делают трансабдоминальное УЗИ малого таза для контроля развития плода. Это достаточно безопасное исследование, которое не сможет навредить малышу. Именно на УЗИ малого таза можно рассмотреть пол будущего ребёнка.
Особенности мужского УЗИ
Мужчинам УЗИ малого таза назначают редко. Это связано с тем, что на нём, из-за особенностей физиологии, мало что можно различить. Органы расположены достаточно далеко и их сложнее рассмотреть. В малый таз мужчин входят мочевой пузырь, прямая кишка, предстательная железа и семенные пузырьки. Наружные половые органы мужчин при УЗИ малого таза не осматривают. Часто врач рекомендует отдельное исследование мочевого пузыря или простаты, а не полный осмотр всего малого таза.
Однако, в некоторых случаях предпочтительней именно общий осмотр. Доктор назначит ультразвуковое исследование малого таза, если у вас:
Такой тип обследования будет необходим при проблемах с потенцией. А если у вас были заболевания, передающиеся половым путём, то его необходимо проходить регулярно, во избежание осложнений.
Осмотр проводится трансабдоминально и ректально. В первом случае можно рассмотреть мочевой пузырь и семенники, а во втором — предстательную железу. После получения снимков нужно провести более точные обследования: сдать кровь и анализ на мочу, сделать спермограмму и компьютерную томографию.
Что нужно знать об ультразвуковом исследовании малого таза?
Подготовка к УЗИ зависит от его типа:
Для этого можно за час-полтора до визита к врачу выпить около литра воды. Перед трансректальным УЗИ желательно сделать клизму для очищения прямой кишки.
За два-три дня до исследования следует исключить из рациона все продукты, повышающие газообразование: богатые клетчаткой овощи (капусту, лук, редис), бобовые, хлеб, каши, кисломолочные продукты. Можно за один-два дня начать принимать сорбенты и ветрогонные препараты.
Не забудьте провести гигиенические процедуры перед визитом к врачу. Захватите с собой полотенце, чтобы вытереть гель с тела, и простынь, чтобы положить её на кушетку. Для большего комфорта можно подобрать такую одежду, которую будет легко снять или отодвинуть для проведения осмотра: широкую футболку, юбку или свободные штаны. И не забудьте захватить заключения с предыдущих ультразвуковых исследований: врач сразу же сможет отследить динамику и назначить дальнейшие осмотры.
Диагностика патологии эндометрия в постменопаузе: применение 2D и 3D технологий
УЗИ аппарат HS40
Лидер продаж в высоком классе. Монитор 21,5″ высокой четкости, расширенный кардио пакет (Strain+, Stress Echo), экспертные возможности для 3D УЗИ в акушерско-гинекологической практике (STIC, Crystal Vue, 5D Follicle), датчики высокой плотности.
Введение
Трехмерное УЗИ в последние годы чаще используется в работе как врачей ультразвуковой диагностики, так и врачей акушеров-гинекологов, несмотря на то, что остается ряд дискуссионных вопросов, роль которых в диагностике гинекологической патологии еще предстоит определить 1.
В большей мере освещены вопросы патологии эндометрия в постменопаузальном возрасте. Так, S. Kupesic и соавт. определили, что трехмерная энергетическая допплерография может использоваться для раннего выявления рака эндометрия, особенно у женщин в постменопаузальном возрасте без клинической симптоматики заболевания, а также для уточнения инвазии опухоли в миометрий [4].
При обследовании пациенток постменопаузального возраста с аденокарциномой, гиперплазией, атрофией эндометрия и субмукозной миомой матки, J.L. Alcazar и R. Galv n установили, что 3D энергетическая допплерография может быть полезна в диагностике рака эндометрия, так как у этих пациенток статистически значимо повышены индекс васкуляризации (ИВ) и васкуляризационно-потоковый индекс (ВПИ) эндометрия в сравнении с пациентками других групп [5].
В свою очередь R. Galv n и соавт. при изучении стадийности эндометриального рака у пациенток в постменопаузе определили, что ИВ в малигнизированном эндометрии коррелирует с некоторыми гистологическими характеристиками опухоли [6].
G. Opolskiene и соавт. определили, что у женщин с кровотечением в постменопаузальном возрасте ИВ и ВПИ не отличались как при доброкачественных, так и при злокачественных изменениях в эндометрии [7]. К противоположным выводам пришли A.K. Makled и соавт., которые в своих исследованиях доказали, что значение ИВ является достоверным диагностическим критерием рака эндометрия в постменопаузе [8].
Как видно из изложенного выше, в последние годы увеличивается интерес к проблемам постменопаузы, что связано в первую очередь с тенденцией населения развитых стран к старению. Поэтому так актуальны вопросы патологии эндометрия в постменопаузальном периоде [9].
Кроме того, заболеваемость раком эндометрия увеличилась во всех экономически развитых странах [10, 11].
В постменопаузальном возрасте у ряда пациенток происходит полная облитерация цервикального канала, и показанием для проведения раздельного диагностического выскабливания становится расширение полости матки за счет жидкости, выявленное при УЗИ в 2D режиме. Между тем у врачей ультразвуковой диагностики нет четких критериев, позволяющих исключить злокачественную трансформацию эндометрия у таких пациенток. Следовательно, поиск путей улучшения диагностики патологических состояний эндометрия у пациенток в постменопаузальном возрасте с использованием трехмерной эхографии с опцией энергетического допплера побудил нас к исследованиям в этой области.
Целью настоящего исследования стало проведение анализа совпадений результатов рутинного двухмерного трансвагинального УЗИ у пациенток постменопаузального возраста с окончательным патоморфологическим заключением исследования биоптата эндометрия, определение возможности использования трехмерной энергетической допплерографии у пациенток с облитерацией цервикального канала в постменопаузе.
Материал и методы
Для достижения поставленной цели нами ретроспективно оценено 50 историй болезни женщин постменопаузального возраста, госпитализированных в гинекологическое отделение для проведения раздельного диагностического выскабливания и гистероскопии в плановом порядке. Показанием для госпитализации явились данные рутинного трансвагинального УЗИ (ультразвуковое заключение: патология эндометрия). Данные ультразвуковых заключений, послужившие поводом для госпитализации в стационар, были оценены ретроспективно и сопоставлены с данными гистологических заключений после раздельного диагностического выскабливания.
Пациентке с атрезией цервикального канала и скоплением жидкости в полости матки проведено трансвагинальное сканирование с использованием объемного ректовагинального датчика 4-9 МГц на стационарном ультразвуковом сканере Accuvix-V10 компании Samsung Medison в режиме 3D реконструкции с опцией энергетического допплера по методике И.А. Озерской [12], с последующим автоматическим получением ИВ, индекса потока (кровотока) (ИП), ВПИ реконструированной матки в программе Virtual Organ Computeraided AnaLysis (VOCAL).
Статистическая обработка данных осуществлялась с применением прикладного программного пакета «Statistica 6.0», адаптированного для медико-биологических исследований. Производилось вычисление относительных частот признака (%) в группе.
Результаты и обсуждение
Анализ приведенных результатов побуждает к поиску дополнительных ультразвуковых методик, которые можно применить в постменопаузальном возрасте, особенно в ситуации с атрезией цервикального канала и последующим скоплением жидкости в полости матки. Именно это состояние занимает высокий удельный вес в постменопаузальном возрасте и, не представляя трудностей в диагностике при рутинном трансвагинальном УЗИ, ведет к проведению раздельного диагностического выскабливания.
Мы попытались применить у такой категории пациенток 3D энергетическую допплерографию и приводим клинический пример.
Пациентка К., 60 лет, поступила в гинекологическое отделение для проведения раздельного диагностического выскабливания под контролем гистероскопии с диагнозом: подозрение на рак тела матки. Данные трансвагинального УЗИ, проведенного амбулаторно: тело матки нормальных размеров, контур матки ровный, миометрий однородный, полость матки расширена до 6 мм, заполнена анэхогенным содержимым. Яичники обычных размеров и эхоструктуры, свободная жидкость в позадиматочном пространстве не визуализируется. Ультразвуковое заключение: серозометра.
Анамнестические данные: постменопауз 5 лет, из гинекологических заболеваний в анамнезе пациентка отмечает эктопию шейки матки, по поводу чего была произведена диатермоэлектрокоагуляция шейки матки. В анамнезе 2 родов, в срок, без осложнений и один медицинский аборт в срок 8-9 нед, без осложнений.
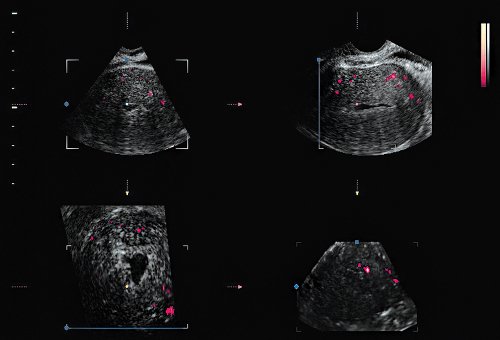
До проведения раздельного диагностического выскабливания, на стационарном ультразвуковом сканере Accuvix-V10 компании Samsung Medison после опорожнения мочевого пузыря мы провели трансвагинальное сканирование с использованием объемного ректовагинального датчика 4-9 МГц в режиме 3D реконструкции с опцией энергетического допплера и получили объемное изображение (рис. 1).
Рис. 1. Объемное изображение в режиме энергетического допплера.
Трансвагинальное ультразвуковое исследование и гормонозаместительная терапия
УЗИ сканер HS50
Доступная эффективность. Универсальный ультразвуковой сканер, компактный дизайн и инновационные возможности.
Введение
Благодаря повышению ожидаемой продолжительности жизни одна треть жизни каждой рождающейся сегодня девочки пройдет после наступления менопаузы [1]. Мы ожидаем, что здоровая 50-летняя женщина проживет в постменопаузальном периоде 30 лет или более. При этом нужно помнить, что недостаток эстрогенов вызывает вазомоторную неустойчивость, атрофию органов урогенитальной сферы, эмоциональные нарушения, остеопороз и ускорение развития атеросклероза [2].
Существуют многочисленные данные, которые указывают на то, что гормональная заместительная терапия способна эффективно ослаблять неблагоприятные симптомы менопаузы, предотвращая возникновение сердечно-сосудистых и цереброваскулярных эффектов дефицита эстрогенов [3,4], и снижать риск развития остеопороза [5]. По мнению консультантов (64%) и, реже врачей общей практики (56%), гормональная заместительная терапия должна проводиться всем женщинам, которые имеют для этого показания. В целом, консультанты больше доверяют гормональной заместительной терапия как средству профилактики [6].
При проведении гормональной заместительной терапии представляет опасность риск возникновения гиперплазии и рака эндометрия. В связи с этим для динамического контроля за проведением гормональной заместительной терапии рекомендовалось проведение биопсии эндометрия, хотя имеются данные, что применение прогестогена в течение 10-20 дней цикла может предотвращать развитие гиперплазии [7]. Добавление прогестогена вызывает атрофию эндометриальной выстилки, что снижает риск развития рака эндометрия, связанного с приемом эстрогенов. Тем не менее такие гестагенные побочные эффекты, как вздутие живота, депрессия, болезненность молочных желез могут вызывать дискомфорт [8]. Эстрогены назначают с 1 по 25 день, прогестоген добавляют на 14-ый день и продолжают принимать до 25 дня цикла. Такая схема вызывает появление кровотечений на фоне отмены препарата у 90% женщин, однако их частота снижается с возрастом, достигая к 85 годам 60% [9].
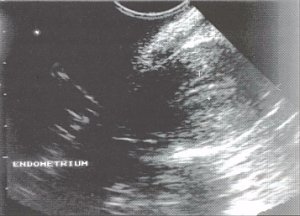
Для снижения риска возникновения нежелательных кровотечений некоторые больные принимают ежедневно эстрогены и прогестоген, который вызывает атрофию эндометрия через 3-6 месяцев. Без сомнения, целью соглашения по проведению биопсий для динамического контроля за женщинами, получающими гормональную заместительную терапию, было снижение числа излишних биопсий эндометрия и риска развития осложнений, возникающих вследствие расширения шейки матки и кюретажа [10]. Тем не менее при проведении всех вариантов биопсии и забора цитологического материала могут возникать некоторые технические проблемы, например при стенозе (постменопаузальном) шейки матки. В то же время мы рассматриваем ультразвуковое исследование как менее инвазивное (рисунок). Нормальный эндометрий после наступления менопаузы при развитии атрофии выглядит при ультразвуковом исследовании как тонкая эхогенная полоска менее 8 мм толщиной в передне-заднем направлении [11]. В 1980 г. произошел значительный прогресс в развитии ТВУЗИ, что способствовало значительному расширению клинического использования этого метода [12]. Применение ТВУЗИ дает ценную информацию при диагностике большого числа гинекологических заболеваний, исследовании половых органов [13].
Материалы и методы
У пациенток собирали детальный анамнез и проводили физикальное исследование. Всем женщинам проводилось влагалищное исследование, трансвагинальное ультразвуковое исследование (ТВУЗИ) и взятие мазков из шейки матки. 38 женщин, которые были отобраны по случайному принципу, постоянно получали перорально премарин 0,625 мг в день. Кроме того, в первые 10 дней каждого месяца назначали прогестоген (группа А). Группа Б (50 женщин) принимала премарин в течение трех недель каждого месяца, а на третьей неделе добавлялся прогестоген. В течение четвертой недели больные не получали гормональных препаратов. Терапия гормонами проводилась на протяжении двух лет.
Контрольное наблюдение включало в себя проведение обычного осмотра, исследование цервикальных мазков, ТВУЗИ и биопсию эндометрия. При невозможности или сложности проведения в гинекологическом кабинете биопсии последняя выполнялась в операционной под общей анестезией. Для ТВУЗИ использовали ультразвуковой аппарат SonoAce-1500 фирмы Medison, с трансвагинальным датчиком частотой 6,5 МГц. Исследование проводилось в положении лежа на спине. Матку осматривали в продольной плоскости для оценки состояния всей полости, регистрировалась максимальная толщина эндометрия путем измерения общей его толщины от одной границы с миометрием до другой.
Результаты исследования
Результаты работы приведены в табл. 1-8 и на рис. 1-5.
Определение толщины эндометрия при ТВУЗИ у здоровой женщины.
Что показывает узи малого таза у женщин при климаксе
Кафедра репродуктивной медицины и хирургии факультета дополнительного профессионального образования ГБОУ ВПО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова» Минздрава России, Москва, Россия
ФГБУ «Клиническая больница»
Патология эндометрия в постменопаузе: нужен ли ультразвуковой скрининг?
Журнал: Проблемы репродукции. 2019;25(2): 113-119
Адамян Л. В., Мельникова Н. С., Касян В. Н. Патология эндометрия в постменопаузе: нужен ли ультразвуковой скрининг?. Проблемы репродукции. 2019;25(2):113-119.
Adamyan L V, Mel’nikova N S, Endometrial pathology in postmenopausal women: do we need ultrasound screening?. Russian Journal of Human Reproduction. 2019;25(2):113-119.
https://doi.org/10.17116/repro201925021113
Кафедра репродуктивной медицины и хирургии факультета дополнительного профессионального образования ГБОУ ВПО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова» Минздрава России, Москва, Россия
Цель исследования — повышение эффективности диагностики и лечения патологических процессов эндометрия без кровотечения у пациенток пожилого и старческого возраста, снижение частоты рецидивов этих заболеваний и риска возникновения злокачественных новообразований. Материал и методы. В исследование включены 288 пациенток пожилого и старческого возраста с подозрением на патологию эндометрия, по данным ультразвукового скрининга, которым выполнены гистероскопия, раздельное диагностическое выскабливание стенок полости матки с последующей морфологической верификацией диагноза. Результаты. Отсутствие патологических изменений и атрофия эндометрия отмечены у 30,5% пациенток, чаще всего выявлялись полипы эндометрия — у 63,9%, субмукозные и интрамурально-субмукозные миомы матки — у 5,5%, хронический эндометрит — у 3,5%. Гиперплазия эндометрия не выявлена ни в одном случае. Аденокарцинома эндометрия обнаружена у 6 (2,1%) пациенток, заболеваемость составила 0,1 на 100 обследованных. Показатели информативности ультразвукового исследования (чувствительность и специфичность) составили 76,4 и 99,2% соответственно. В 3 (7,1%) случаях рецидивов полипов эндометрия обнаружены умеренно- и высокодифференцированные эндометриоидные аденокарциномы. При иммуногистохимическом исследовании полипов эндометрия отмечено повышение экспрессии ингибитора апоптоза bсl-2 в сочетании со снижением экспрессии индуктора апоптоза Вах, что указывает на подавление апоптоза и соответственно на риск неопластической трансформации. Выводы. Риск возникновения злокачественных новообразований эндометрия в пожилом и старческом возрасте выше общепопуляционных показателей, особенно у пациенток с рецидивами патологических процессов в эндометрии, поэтому целесообразно выполнение скринингового ультразвукового обследования в рамках первичной профилактики онкозаболеваний для активного выявления внутриматочных изменений и лечения на ранних этапах.
Кафедра репродуктивной медицины и хирургии факультета дополнительного профессионального образования ГБОУ ВПО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова» Минздрава России, Москва, Россия
ФГБУ «Клиническая больница»
Рак эндометрия занимает 6-е ранговое место среди злокачественных новообразований у женского населения в мире [1, 2]. Известно, что почти 60% аденокарцином эндометрия выявляют у женщин в постменопаузе, причем пик заболеваемости приходится на возраст 55—69 лет. В России в 2013 г. у женщин возрастной группы 55—69 лет рак тела матки занимал 2-е ранговое место [3]. Факторами риска развития рака эндометрия являются пожилой возраст пациенток (старше 50 лет), ожирение, поздняя менопауза, сахарный диабет, длительная эстрогеновая стимуляция, прием тамоксифена [2]. Ожирение с индексом массы тела (ИМТ) более 25 кг/м 2 повышает риск развития рака эндометрия на 200—400% [4] при том, что более 50% женщин в постменопаузе имеют избыточную массу тела. В связи с изложенным онконастороженность в этой возрастной группе является обоснованной.
Рак эндометрия более чем в 95% случаев манифестирует в постменопаузе кровотечением [5]. В этой ситуации первостепенной задачей врача становится исключение или подтверждение злокачественного процесса. Гистологически рак эндометрия подтверждается примерно у 10% женщин с жалобами на кровотечение в постменопаузе (1—14% по данным разных авторов). Практически в 60% случаев выявляются атрофия эндометрия и примерно с одинаковой частотой — полипы эндометрия, гиперплазия эндометрия и другие изменения эндометрия доброкачественного генеза [6, 7]. Таким образом, в большинстве случаев причиной кровотечений в постменопаузе являются изменения эндометрия доброкачественного характера.
У женщин с кровотечением в постменопаузе трансвагинальное ультразвуковое исследование (УЗИ) органов малого таза с определением толщины М-эхо служит методом скринингового обследования для исключения патологических процессов в эндометрии. Верхней границей нормы является толщина М-эха 4 мм, если она ниже этой границы, то вероятность РЭ составляет менее 1% [5, 8], в таких случаях биопсия эндометрия не требуется. Назначение гестагенов для «гормонального кюретажа» в постменопаузе признано нецелесообразным. В ряде случаев увеличение толщины эндометрия по данным ультразвукового исследования (УЗИ) выявляется у женщин в постменопаузе в отсутствие симптомов заболевания до 10—17% [7]. Однако тактика ведения в таких случаях окончательно не определена.
Цель исследования — повышение эффективности диагностики и лечения патологических процессов эндометрия без кровотечения у пациенток пожилого и старческого возраста, снижение частоты рецидивов этих заболеваний и риска возникновения злокачественных новообразований.
Материал и методы
Для оценки частоты и структуры патологических изменений эндометрия у женщин в пожилом и старческом возрасте проанализированы амбулаторные карты 3998 женщин старше 60 лет, прикрепленных к одной из ведомственных поликлиник Управления делами Президента Российской Федерации. В исследование включены 288 (7,2%) пациенток из прикрепленного контингента c подозрением на патологический процесс в эндометрии (ППЭ) по результатам ультразвукового (УЗ) скринингового обследования (М-эхо более 4 мм) без клинической симптоматики.
Все пациентки в 2008—2011 гг. находились на оперативном лечении в гинекологическом отделении ФГБУ «Клиническая больница» Управления делами Президента Российской Федерации, госпитализированы для проведения гистероскопии с раздельным диагностическим выскабливанием стенок полости матки и цервикального канала, по показаниям — гистерорезектоскопии с последующим гистологическим и иммуногистохимическим исследованием образцов ткани. УЗИ органов малого таза выполняли как с целью диагностики внутриматочных патологических процессов, так и мониторинга результатов проведенного лечения.
С целью выявления рецидивов патологических процессов в эндометрии (РПЭ) проведен ретроспективный анализ медицинской документации 288 пациенток, выполнены дополнительный сбор анамнеза, анализ результатов УЗИ органов малого таза в динамике, протоколов оперативных вмешательств, а также заключений патогистологических исследований соскобов из цервикального канала и полости матки.
Следует отметить, что принадлежность к ведомственному контингенту и четкая маршрутизация пациенток имели большое значение для преемственной работы стационарного и амбулаторного звеньев оказания медицинской помощи и повышали статистическую значимость получаемых в ходе исследования данных, так как позволяли прослеживать состояние органов репродуктивной системы пациенток на протяжении многих лет, анализировать методы лечения и оценивать отдаленные результаты.
Результаты
Возраст пациенток колебался от 60 до 87 лет (средний возраст — 67,6±5,56 года), средний возраст начала менопаузы — 44,9±6,8 года.
Частота различных ППЭ у женщин пожилого и старческого возраста, находящихся на диспансерном учете, составила 2,5% или 24,8 на 1000 человек. По данным гистологического исследования, у 88 (30,5%) пациенток в постменопаузе, имевших толщину эндометрия более 4 мм, отмечены атрофия эндометрия и отсутствие патологических изменений. У 200 (69,5%) пациенток выявлена патология, в том числе: субмукозные и интрамурально-субмукозные миомы матки — у 16 (5,5%) пациенток, хронический эндометрит — у 10 (3,5%), чаще всего выявлялись полипы эндометрия — у 184 (63,9%). Гиперплазия эндометрия не выявлена ни в одном случае. Аденокарцинома эндометрия обнаружена у 6 (2,1%) человек; заболеваемость составила 0,1 на 100 обследованных. Чувствительность и специфичность УЗИ составили 76,4 и 99,2% соответственно [9]. Риск возникновения злокачественных новообразований достаточно высок (около 1 случая на 1000 человек), что диктует важность адекватного обследования и своевременного лечения женщин этой возрастной группы.
Рецидивы ППЭ выявлены у 42 (14,6%) женщин. Впервые выявленные ППЭ в постменопаузе и их рецидивы имели место у 27 (64,3%) женщин, из них у 25 (92,6%) обнаружены железисто-фиброзные полипы эндометрия, у 2 (7,4%) — аденокарцинома. Впервые выявленные в репродуктивном возрасте или пременопаузе ППЭ с рецидивом в постменопаузе отмечены у 15 (35,7%) женщин, из них у 14 (93,3%) — железисто-фиброзные полипы эндометрия, у 1 (6,7%) — аденокарцинома эндометрия. В целом из рецидивирующих патологических процессов в эндометрии преобладали железисто-фиброзные полипы эндометрия — 39 (92,9%) случаев. В 38 (90,5%) наблюдениях, независимо от первично выявленного полипа эндометрия или его рецидива, в строме полипа выражена воспалительная (лимфомакрофагальная, с примесью лейкоцитов и/или плазмоцитов) инфильтрация.
В результате ретроспективного анализа медицинской документации сделан вывод, что одной из ведущих причин (55,6% случаев) рецидивов полипов в изученных наблюдениях явился отказ от применения гистероскопии при проведении раздельного диагностического выскабливания стенок полости матки и цервикального канала. В 40,1% наблюдений совпала локализация полипов эндометрия, обнаруженных впервые и при их рецидиве. Анализ лечения рецидивов патологических процессов в эндометрии при повторных госпитализациях выявил преимущества применения индивидуального подхода в профилактике дальнейших рецидивов: в соответствии с показаниями больным проводили гистерорезектоскопию или прицельное удаление полипов эндоскопическими щипцами, электроаблацию эндометрия. В последующем периоде наблюдения от 3 до 6 лет рецидивов не было. Данные нашего исследования и результаты О.В. Хитрых и соавт. [9, 10] свидетельствуют в пользу пересмотра оперативной техники и преимущественного использования микроинструментов или резектоскопии, а также выполнения обязательной контрольной гистероскопии перед завершением операции.
Аденокарцинома выявлена у 3 (7,1%) пациенток, гиперплазия эндометрия не обнаружена, случаев рака в полипе не выявлено. Полученные данные превышают частоту аденокарцином эндометрия в общей популяции женщин (около 0,01%), а нарушения дифференцировки эпителия желез в полипах отмечены в 100% таких наблюдений. На основании полученных данных можно сделать вывод о том, что больных пожилого и старческого возраста с рецидивирующей патологией эндометрия следует отнести к группе риска развития аденокарциномы эндометрия.
С целью изучения патогенеза железисто-фиброзных полипов эндометрия у пациенток в пожилом и старческом возрасте нами изучено 19 образцов железисто-фиброзных полипов эндометрия: 9 пациенток в период постменопаузы (основная группа) и 10 пациенток в репродуктивном возрасте (группа сравнения). Применяли иммунопероксидазный метод, используя 6 первичных специфических моноклональных антител к рецепторам эстрогенов, прогестерона, белку Ki-67, ингибитору апоптоза bсl-2, индуктору апоптоза Вах и ферменту ароматазе цитохрома Р450. Результаты иммуногистохимических реакций оценивали с помощью одного из общепринятых полуколичественных морфометрических методов, вычисляя коэффициенты экспрессии того или иного антигена.
В результате иммуногистохимического исследования показано, что в ткани железисто-фиброзных полипов эндометрия у пациенток в постменопаузе статистически значимо ниже экспрессия рецепторов эстрогенов и прогестерона. Разницы в экспрессии маркера пролиферации Ki-67 не выявлено (кроме ее повышения в стромальных клетках), но повышение экспрессии bcl-2 в сочетании со снижением Вах указывает на подавление апоптоза. Кроме того, появление экспрессии АЦР450 указывает на возможность локального повышения концентрации эстрогенов, усиливающих пролиферацию клеток. В условиях подавления апоптоза это повышает риск неопластической трансформации.
Обсуждение
В последние годы авторитетные американские и европейские общества акушеров-гинекологов (AAGL, ESGE, SCOG) указывают на отсутствие необходимости в скрининговом УЗИ органов малого таза в постменопаузе в связи с высокой частотой выявления ложноположительных результатов, низкой прогностической ценностью и, как следствие, неоправданными инвазивными вмешательствами у «бессимптомных» пациенток пожилого возраста. Считается, что злокачественные заболевания эндометрия достаточно рано манифестируют маточными кровотечениями [6, 11—13].
Так, в исследовании A. Lev-Sagie и соавт. [14] под наблюдением находились 82 женщины в постменопаузе со случайно выявленным при УЗИ утолщением эндометрия, всем выполнена гистероскопия с выскабливанием стенок полости матки. По результатам гистологического исследования, у 67 (82%) пациенток выявлены неактивные полипы, у 7 — субмукозные узлы, у 6 — атрофия эндометрия, у 1 — простая гиперплазия, еще у 1 — полип с простой гиперплазией. Ни одного случая сложной гиперплазии или рака эндометрия не было. При этом обращает на себя внимание частота осложнений оперативного вмешательства — 3,6%: 2 перфорации матки, 1 осложнение интубации.
M. Breijer и соавт. [8] проанализировали 32 статьи и обнаружили 10 исследований с участием 3049 пациенток, не принимавших гормонотерапию, без клинических проявлений. Показано, что у обследованных женщин средняя толщина эндометрия составила 2,9 мм, а распространенность рака эндометрия и атипической гиперплазии эндометрия — 0,62 и 0,59% соответственно. Авторы считают, что проведение трансвагинального УЗИ имеет диагностическую ценность только у женщин в постменопаузе при наличии кровотечения в связи с клинически последовательным снижением вероятности заболевания по мере приближения к нормативным значениям толщины эндометрия по данным УЗИ. Для рака эндометрия такое снижение составляет от 10 до 1%, при этом большинство клиницистов настаивают на перепроверке диагноза. Для женщин, не имеющих симптомов заболевания, распространенность рака эндометрия также близка к вышеуказанным параметрам. По мнению авторов обзора, определение толщины эндометрия в этой популяции малоинформативно и не является методом скрининга с целью выявления рака эндометрия и атипической гиперплазии эндометрия.
W. Wolfman и соавт. [15] изучили материалы публикаций, вышедших с 1970 по 2009 г., о результатах обследования женщин в постменопаузе без аномальных маточных кровотечений, у которых при УЗИ обнаружено утолщение эндометрия. При детальной оценке информативности, рисков и стоимости диагностического выскабливания авторы пришли к выводу, что применение инвазивных методов исследования только на основании увеличения показателя М-эхо является излишней (неоправданной) процедурой.
Некоторые исследователи придерживаются иной точки зрения. Целью исследования M. Genc и соавт. [16] было уточнение частоты внутриматочной патологии у 283 женщин в постменопаузе, госпитализированных в гинекологическое отделение для проведения гистерэктомии по причинам, не связанным с патологией эндометрия. По результатам гистологического исследования, у 75,6% из 209 пациенток, не имевших кровотечения в постменопаузе, обнаружена патология полости матки, о которой не подозревали на этапе предоперационной подготовки (гиперплазия эндометрия, полипы, миома матки, аденомиоз, 1 (0,5%) случай аденокарциномы). У 87,8% из 74 женщин с кровотечением в постменопаузе обнаружена внутриматочная патология, в том числе 13 (17,6%; p=0,0001) случаев рака эндометрия. Таким образом, патология полости матки может иметь место и у женщин в постменопаузе, не имеющих симптомов заболевания, поэтому авторы настаивают на ежегодном скрининге и консультировании пациенток пожилого и старческого возраста, не дожидаясь у них эпизода кровотечения.
В нашем исследовании у пациенток в постменопаузе с подозрением на ППЭ по данным УЗИ органов малого таза (М-эхо более 4 мм) в отсутствие клинической симптоматики чаще всего выявляли полипы эндометрия (63,9%), атрофию эндометрия (30,5%), которая подтверждена гистологически; частота аденокарциномы составила 2,1%. Риск возникновения злокачественных новообразований достаточно высок, что свидетельствует о важности адекватного обследования и своевременного лечения женщин этой возрастной группы, а также о необходимости скринингового обследования с применением УЗИ.
По данным литературы, как и в нашем исследовании, у пациенток в постменопаузе без клинических проявлений, но с утолщением М-эха (по данным УЗИ) при гистероскопии и гистологическом исследовании выявляются полипы эндометрия. Логичным является вопрос: нужно ли удалять полипы эндометрия у всех пациенток в постменопаузе? Насколько эта доброкачественная патология с низким риском озлокачествления в популяции в целом опасна для женщин пожилого и старческого возраста? Насколько важно еще на этапе предоперационной подготовки уточнить наличие полипа эндометрия для выбора оптимальной хирургической тактики с целью снижения риска рецидива? Данные литературы [17] достаточно противоречивы, частота рака эндометрия у женщин с полипами эндометрия составляет 0,3—4,8%.
Большинство исследователей настаивают на обращении особого внимания на пациенток в постменопаузе с полипами, проявляющимися маточным кровотечением. Так, E. Ricciardi и соавт. [18] изучали распространенность полипов с атипией у женщин в постменопаузе. В ретроспективном исследовании проанализированы данные 1027 женщин с полипами эндометрия, средний возраст составил 45,8±10,8 года. Доброкачественные полипы выявлены в 95,8% случаев, предраковые — в 2,67% и с атипией — в 1,54% случаев. У женщин в постменопаузе (старше 60 лет) и старческом возрасте риск развития рака эндометрия был выше (ОШ 3,05; 95% ДИ 1,54—6,19; p 2 соответственно). Основным статистически значимым фактором риска развития рака эндометрия было наличие кровотечения (ОШ 13,7; 95% ДИ 1,48—126,28). Таким образом, при подозрении на полип эндометрия по данным УЗИ органов малого таза именно пожилой и старческий возраст и наличие кровотечения четко ассоциируются с риском развития рака эндометрия. Большое число женщин в постменопаузе без симптомов заболевания с подозрением на полип по данным УЗИ направляют на гистероскопию, хотя риск неоплазии в таких случаях крайне невысок.
E. Ferrazzi и соавт. [20] наблюдали 1152 женщины без симптомов заболевания в постменопаузе, у которых по данным УЗИ и соногистерографии выявлены полипы эндометрия, все женщины прооперированы (гистероскопия + кюретаж). По данным гистологического исследования, выявлен 1 (менее 0,1%) случай рака эндометрия в полипе диаметром более 4 мм, при этом частота неоплазии была в 10 раз ниже, чем у пациенток с кровотечением (р