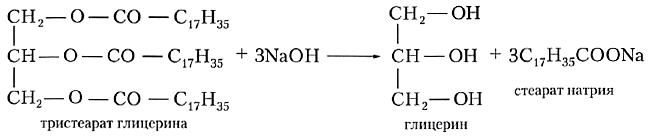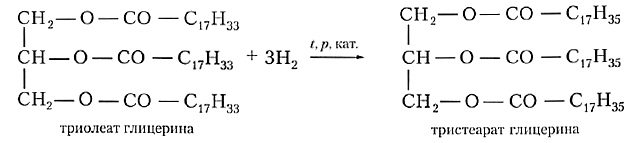Что представляют жиры по химической природе
Что представляют жиры по химической природе
Жир свиной топлёный
Пищевые жиры предназначаются для пищевых целей. Получают пищевые жиры из жировой ткани, молока, костного мозга животных или из семян, а иногда из плодов масличных и некоторых других культур растений. К сопутствующим веществам относятся фосфатиды (состоящие из глицерина, жирных кислот и веществ, содержащих азот и фосфор), липохромы (красящие вещества), эфирные масла (обусловливающие запах растительных масел), стерины, витамины A, D, Е. Присутствие этих веществ повышает ценность жира (масла) как продукта питания и способствует нормальному развитию организма. Количество этих веществ зависит от вида жира (масла), способа его получения и обработки. Сопутствующие вещества присутствуют в жире в растворенном виде или во взвешенном состоянии и находятся в нём как естественная примесь либо переходят в него из растительного или животного сырья при получении.
Жиры пищевые язляются одним из важных источников энергии для организма человека. Как пищевые вещества они ценны тем, что организм с небольшим (по весу и объёму) количеством пищи получает значительное количество энергии. Жиры приблизительно в 2½ раза более калорийны, чем углеводы.
Норма жиров в суточном рационе взрослого человека колеблется в зависимости от характера выполняемой работы, возраста, состояния здоровья, условий окружающей среды и может колебаться от 52 до 120 г. Более высокая норма жиров в пище предназначается для людей, занятых тяжёлым физическим трудом. В то же время как обязательная составная часть пищи жиры в значительном количестве должны входить в рацион больных туберкулезом. Это обусловлено тем, что больные туберкулезом, имея повышенный расход энергии, в то же время обладают пониженным аппетитом. С другой стороны, при некоторых заболеваниях, например болезни печени, жиры являются противопоказанными к употреблению.
Пищевые жиры не всасываются в неизмененном виде в желудочно-кишечном тракте, а предварительно расщепляются на свободные жирные кислоты и глицерин. В желудке расщепляется небольшая часть жиров, перевариваются они главным образом в тонких кишках, где предварительно эмульгируются (разбиваются на мельчайшие капельки). Наиболее сильное эмульгирующее действие оказывают соли желчных кислот. Хорошо эмульгируются жиры только в жидком состоянии. Поэтому, чем ниже температуpa плавления, тем лучше жиры усваиваются. Так, температуpa плавления свиного жира колеблется в пределах 28—48° и соответственно усвояемость его равна 96—98%; для говяжьего жира температуpa плавления 42—52°, усвояемость 80—94%; для бараньего жира температура плавления 44—50°, усвояемость 80—90%.
Сливочное масло имеет низкую температуру плавления (27—34°), усвояемость его равна 98,8%. Этим и объясняется столь широкое применение для диетического и детского питания сливочного масла и наиболее схожего с ним по пищевым качествам, вкусу, запаху, консистенции и усвояемости сливочного маргарина.
Продукты расщепления жиров (глицерин и жирные кислоты) всасываются организмом неодинаково: глицерин всасывается без дальнейших изменений; жирные кислоты соединяются с желчными кислотами в растворимые комплексы — соли холеиновых кислот, и в таком состоянии всасываются стенками кишечника, затем эти соединения снова распадаются на желчные и жирные кислоты, из которых уже синтезируются жиры, свойственные данному организму. При избыточном поступлении жиров в организм часть их может откладываться в жировой ткани (так называемое жир-депо) и впоследствии расходоваться организмом при недостаточном питании. Жир является также пластическим материалом, входящим в состав различных тканей организма.
В зависимости от свойств и особенностей пищевых жиров применение их очень разнообразно.
Жиры в кулинарии
В кулинарии жиры в зависимости от консистенции при обычной температуре и особенностей использования подразделяются на плотные (твёрдые) и жидкие (столовые или салатные масла).
В СССР к первой подгруппе относились различные виды сливочного масла (солёное, несолёное, вологодское, любительское, шоколадное, медовое, фруктовое, с сахаром и т.д.), маргарин сливочный, животный, столовый, реже свиной топленый жир высшего сорта. Используются для приготовления различных блюд; сливочное масло употребляется для намазывания на хлеб и изготовления бутербродов.
Во вторую подгруппу входят различные растительные масла: подсолнечное, арахисовое, кунжутное, а также рафинированное хлопковое и соевое. Применяются для приготовления винегретов, салатов и т. п., а также для различных соусов к холодным блюдам (сельдь, осетрина и т. д.). Использование для холодных блюд и закусок растительных масел объясняется не только их вкусовым соответствием, но и тем, что они не застывают при обычной температуре.
Что представляют жиры по химической природе
Процесс получения сложных эфиров носит название реакции этерификации. Эта реакция с использованием общих формул описывается уравнением
Именно реакцией этерификации в 1759 г. в результате взаимодействия уксусной кислоты с этиловым спиртом был получен первый сложный эфир — этиловый эфир уксусной кислоты:
Обратите внимание на то, как строится название сложного эфира. Оно состоит из четырёх слов, указывающих на название углеводородного радикала и исходной кислоты. Например, продукт взаимодействия муравьиной кислоты с метиловым спиртом — метиловый эфир муравьиной кислоты:
Катион водорода в схеме реакции указывает на то, что реакция этерификации протекает в присутствии кислоты в качестве катализатора.
Сложные эфиры с небольшой молекулярной массой представляют собой легковоспламеняющиеся жидкости с характерным, часто приятным запахом. Они нерастворимы в воде, но прекрасно растворяют различные органические вещества.
Реакции этерификации обратимы. В присутствии кислот сложные эфиры разлагаются водой — гидролизуются, что можно рассматривать как реакцию, обратную их получению:
В присутствии щелочей гидролиз сложных эфиров необратим, так как образующаяся кислота связывается щёлочью с образованием соли, неспособной вступать в реакцию со спиртом:
Нахождение в природе и применение сложных эфиров
Сложные эфиры широко распространены в природе. Неповторимый аромат цветов и фруктов часто обусловлен присутствием веществ именно этого класса. Сложные эфиры с большой молекулярной массой представляют собой твёрдые вещества — воски. Пчелиный воск — это смесь сложных эфиров, образованных карбоновыми кислотами и спиртами с длинными углеводородными цепями.
Синтетические сложные эфиры используют в пищевой промышленности в качестве добавок для придания фруктовых запахов напиткам и кондитерским изделиям. Благодаря хорошей растворяющей способности сложные эфиры входят в состав растворителей лаков и красок.
Жиры, их строение и свойства
Люди стали использовать жиры в повседневной жизни значительно раньше, чем задумались об их химическом строении. Животные и растительные жиры — важные компоненты пищи. Жиры необходимы для построения клеточных мембран и как источник энергии, поскольку калорийность жиров в 2 раза выше, чем других питательных веществ — углеводов и белков. У позвоночных животных жиры откладываются в жировой ткани, сосредоточенной в основном в подкожной жировой клетчатке и сальнике. В растениях жиры содержатся в сравнительно небольших количествах, за исключением семян масличных растений, в которых содержание жиров может быть более 50%.
Жиры используют не только в пищевой промышленности. Их используют в качестве смазки, косметических и лекарственных средств, для приготовления масляных красок и олифы.
В 1779 г. шведский химик К. Шееле получил из оливкового масла вязкую жидкость, сладкую на вкус, — простейший трёхатомный спирт глицерин. Вскоре выяснилось, что глицерин входит в состав молекул любых жиров. Позднее французский химик М. Шеврёль доказал, что, помимо глицерина, при нагревании жиров в присутствии кислоты образуются и карбоновые кислоты.
| Жиры представляют собой сложные эфиры трёхатомного спирта глицерина и высших карбоновых кислот. |
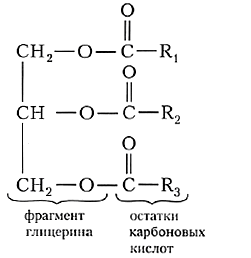
Общую формулу жиров можно представить в следующем виде:
В состав жиров чаще всего входят остатки карбоновых кислот, содержащих чётное число атомов углерода и неразветвлённую углеродную цепь. Наиболее часто в составе жиров встречаются остатки пальмитиновой, стеариновой и олеиновой кислот. В одной молекуле кислотные остатки могут быть различными, поэтому в общей формуле жиров углеводородные радикалы R обозначены разными цифрами.
Сравните состав стеариновой (С17Н35СООН) и олеиновой (С17Н33СООН) кислот. У стеариновой кислоты углеводородный радикал отвечает формуле СnН2n+1, т. е. является предельным. Следовательно, стеариновая кислота относится к предельным карбоновым кислотам. В углеводородном радикале олеиновой кислоты на два атома водорода меньше, поскольку в нём содержится одна двойная углерод-углеродная связь. Олеиновая кислота относится к непредельным карбоновым кислотам.
Жиры животного происхождения имеют твёрдую консистенцию (есть и исключения, например жидкий рыбий жир). В состав молекул твёрдых жиров входят остатки предельных кислот. Растительные жиры, которые часто называют растительными маслами, образованы остатками непредельных кислот, имеют жидкую консистенцию (исключение — твёрдое пальмовое масло). Кстати, название олеиновой кислоты произошло от латинского слова oleum — масло.
Жиры гидрофобны, т. е. нерастворимы в воде, но хорошо растворяются в органических растворителях: этиловом спирте, гексане, тетрахлорметане.
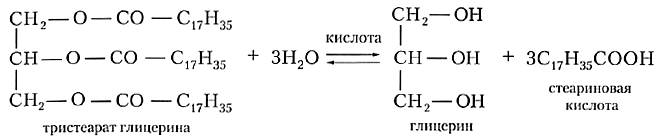
Жиры проявляют все характерные для сложных эфиров химические свойства. Главное из них — это гидролиз. Молекулы воды атакуют связи между кислотным остатком и фрагментом глицерина, в результате чего происходит распад молекулы жира:
Для жира, образованного стеариновой кислотой (такое вещество называют тристеаратом глицерина), уравнение реакции гидролиза выглядит следующим образом:
В качестве катализатора гидролиза жиров выступают кислоты. Такой гидролиз так и называют — кислотный гидролиз. Жирные руки трудно отмыть холодной водой, но стоит только протереть их ломтиком лимона, как они становятся заметно чище. Даже при таком непродолжительном контакте с лимонной кислотой жир частично гидролизуется.
Гидролиз жиров в присутствии щелочей называют щелочным гидролизом:
Щёлочь действует как катализатор, а также связывает образующиеся кислоты, превращая их в соли карбоновых кислот. Соли не способны вступать в реакцию этерификации с глицерином, и гидролиз становится необратимым. Неслучайно бытовые средства для удаления жира и засоров в раковинах более чем наполовину состоят из щёлочи.
Щелочной гидролиз жиров называют также омылением. Это название обусловлено тем, что образующиеся при этом натриевые и калиевые соли высших карбоновых кислот являются мылами.
Твёрдые жиры животного происхождения более ценны и дорогостоящи, чем жидкие растительные масла. Можно ли превратить жидкий жир в твёрдый химическим путём? Если вы вспомните, что растительные масла, в отличие от животных жиров, содержат остатки непредельных кислот, то нетрудно догадаться: гидрированием двойных связей С=С растительные масла превращают в аналог твёрдых жиров. Полученный продукт называют саломасом, его используют для приготовления маргарина и других продуктов питания:
Подобный процесс в больших масштабах проводят на жировых комбинатах.
Двойные связи непредельных кислот в жидких жирах сохраняют способность к реакциям полимеризации. Это свойство используют при изготовлении олифы — натуральной (на основе льняного или конопляного масла) или синтетической. При нанесении на деревянную поверхность олифа под действием кислорода воздуха полимеризуется с образованием прочной защитной плёнки. Олифу используют и при изготовлении и разбавлении масляных красок.
Справочная таблица «Сложные эфиры»
Конспект урока по химии «Сложные эфиры. Жиры». В учебных целях использованы цитаты из пособия «Химия. 10 класс : учеб, для общеобразоват. организаций : базовый уровень / О. С. Габриелян, И. Г. Остроумов, С. А. Сладков. — М. : Просвещение». Выберите дальнейшее действие:
Жиры и их свойства
Понятие жиров, их классификация, химические и физические свойства. Характеристика природных животных и растительных жиров. Продукты переработки жиров, гидролиз жиров в технике. Сложные эфиры одноосновных карбоновых кислот. Синтетические моющие вещества.
| Рубрика | Химия |
| Вид | реферат |
| Язык | русский |
| Дата добавления | 29.09.2017 |
| Размер файла | 1,2 M |
Отправить свою хорошую работу в базу знаний просто. Используйте форму, расположенную ниже
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Размещено на http://www.allbest.ru/
Размещено на http://www.allbest.ru/
2. Жиры и их классификация
4. Продукты переработки жиров
Жиры представляют собой сложные эфиры глицерина и высших жирных кислот (глицериды).В зависимости от состава ацила, содержащего преимущественно предельные или непредельные высшие кислоты, различают твердые или жидкие жиры. Химическая природа жиров была установлена в первой четверти XIX в. Шеврелем, а синтез жиров впервые осуществлен Бертло в 1854 г.
В состав твердых жиров входят предельные кислоты: масляная (С4), капроновая (С6), капрадовая (С8), каприновая (С10), лауриновая (C12), пальмитиновая (С16), стеариновая (C18) и арахиновая (С20), содержащие четное число углеродных атомов и неразветвленную углеродную цепь.
Растительные масла, содержащие непредельные кислоты с двумя и более двойными связями, легко окисляются на воздухе с образованием гидропероксидных мостиков.
В процессе пищеварения жиры под действием фермента липазы (содержится в слюне, печени, желудочном и кишечном соках) гидролизуются до свободных глицерина и кислот, которые проходят через стенки кишечника и затем снова связываются в различных комбинациях в жиры.
Жиры легко растворяются в органических растворителях: бензине, эфире, хлороформе, тетрахлориде углерода, бензоле и толуоле, но не растворяются в воде. С водой они образуют стойкие эмульсии, особенно в присутствии поверхностно-активных веществ. Примером водной эмульсии жира, стабилизованной белком, является молоко.
Смеси растительных масел с минеральными используют для приготовления некоторых смазочных масел.
На основе эфиров карбоновых кислот и многоатомных спиртов разработаны смазочные масла для металлургического оборудования, применяемые при температурах до 120° С, а со специальными присадками и до 200° С.
На основе диэфиров изготовляют консистентные смазки с температурой плавления до 185° С, обладающие высокой стойкостью к окислению, малой испаряемостью, отсутствием корродирующего действия.
Жиры используют также для фармацевтических целей и в парфюмерии (кремы, помады и др.)
Полученный твердый жир используют для технических целей, а также в производстве маргарина. При гидрировании одновременно с повышением температуры плавления достигается и другой важный результат: некоторые масла, обладающие неприятным вкусом и запахом, превращаются в высококачественные съедобные жиры.
При действии воды в присутствии кислотных или щелочных катализаторов происходит гидролиз жиров, как и всех сложных эфиров. При проведении гидролиза в щелочной среде (едким натром или содой) входящие в состав жира кислоты выделяются в виде натриевых солей, а эти соли не что иное, как мыла. Поэтому и процесс гидролиза часто называют омылением:
Одним из путей сокращения расхода пищевых, жиров на технические цели является использование в мыловарении синтетических жирных кислот. Для этой цели их получают окислением алканов, содержащихся в высших фракциях нефти:
Конечно, на самом деле молекула алкана не расщепляется точно посередине, поскольку получаются смеси кислот с разным числом атомов углерода. Эти смеси приходится разделять, выделяя из них сравнительно узкие фракции, в составе которых находятся родственные кислоты с близким числом С-атомов. Полученные таким образом смеси жирных кислот действием щелочи или соды превращают в мыла.
Начиная с 30-х годов получили применение синтетические моющие средства, которые в настоящее время призводятся во всем мире миллионами тонн.
Главной составной частью современных синтетических моющих средств являются Поверхностно-активные вещества (ПАВ), которые представляют собой серусодержащиие органические соединения.
2. Жиры и их классификация
За основу названия нитроалканов берется название соответствующего предельного углеводорода; перед основой ставится слово «нитро» и цифра, показывающая положение нитрогруппы в основной цепи:
В соответствии с нахождением нитрогруппы у первичного, вторичного или третичного атомов углерода нитросоединения классифицируют на первичные, вторичные или третичные соответственно.
По химическим свойствам двухосновные кислоты подобны одноосновные. Можно отметить лишь большую кислотность первых членов ряда, обусловленную взаимным влиянием двух карбоксильных групп, являющихся мощными электроноакцепторами:
Приведем значения рKа (показателей константы кислотности) первой ступени диссоциации для некоторых двухосновных кислот: HOOC-COOH 1,23; НООС-СН2СООН 2,80; НООС-(СН2)2СООН 4,17; НООС-(СН2)3-СООН 4,34.
Для сравнения напомним, что для уксусной кислоты рKа равно 4,75, а для пропановой 4,87.
По мере удаления карбоксильных групп друг от друга их взаимное влияние ослабевает и сила кислоты падает. Поскольку двухосновные кислоты имеют две карбоксильные группы, могут быть получены два ряда производных кислот. Например, можно синтезировать моно- и дихлорангидрид, сложные моно- и диэфир и другие производные щавелевой кислоты.
Отдельные представители дикарбоновых кислот применяют в пищевой, парфюмерной, химической промышленности; в последние годы, например, адипиновую (гексан-1,6-диовая) кислоту используют для получения полиамидных смол и волокна «найлон»; в промышленности ее получают окислением циклогексанола азотной кислотой.
Нитрилы получают, как правило, дегидратацией амидов либо действием цианидов металлов (NaCN, KCN, CuCN) на алкилгалогениды. Называют нитрилы, руководствуясь теми же принципами, что и при названии амидов, только слово «амид» заменяют на «нитрил», например:
Гидролиз нитрилов приводит к карбоновым кислотам:
При восстановлении нитрилов (водород в момент выделения или LiAlH4) или при каталитическом гидрировании с хорошими выходами образуются первичные амины:
В названии сложного эфира отражено название исходных спиртовых кислот:
Сложные эфиры получают также реакцией ангидридов либо галогенангидридов кислот со спиртами или реакцией солей карбоновых кислот с алкилгалогенидами:
Под действием воды в кислой или щелочной средах сложные эфиры расщепляются (гидролизуются) с образованием карбоновых кислот и спиртов:
Реакцию гидролиза под действием щелочей называют также омылением.
Высшие предельные (жирные) карбоновые кислоты в воде нерастворимы из-за наличия в молекуле большого углеводородного остатка, однако хорошо растворимы в растворах щелочей за счет образования солей.
Натриевые и калиевые соли высших предельных (жирных) карбоновых кислот многие столетия применяют в качестве мыла.
Рис. 1. Схема действия моющего вещества (мыла):
Обычно мыла получают гидролизом (омылением) жиров либо из синтетических высших жирных кислот.
Мыла широко используют в текстильной промышленности при подготовке к отделке различных видов тканей. Например, при отмывке шерстяных тканей, при отварке шелка и целлюлозных волокон.
Следует отметить, что обычные мыла имеют плохую моющую способность в жесткой воде, так как натриевые и калиевые соли высших жирных кислот вступают в реакцию обмена с находящимися в воде кислыми карбонатами щелочно-земельных металлов (Са, Kg, Ba):
жир гидролиз животный растительный
Приятный аромат цветов, плодов и ягод в значительной степени обусловлен присутствием в них тех или иных сложных эфиров. Это свойство эфиров находит и практическое применение.
Синтетические сложные эфиры в виде фруктовых эссенций используются наряду с другими душистыми веществами в производстве фруктовых вод, кондитерских изделий, при изготовлении духов и одеколонов. Некоторые из сложных эфиров (например, этиловый эфир уксусной кислоты) служат растворителями.
Жиры широко распространены в природе. Наряду с углеводами и белками они входят в состав всех растительных и животных организмов и составляют одну из основных частей нашей пищи.
Животные жиры, как правило, твердые вещества. Растительные жиры чаще бывают жидкими, их называют еще маслами.
Все жиры легче воды. В воде они нерастворимы, но хорошо растворяются во многих органических растворителях (дихлорэтане, бензине).
Химические свойства. Важнейшим химическим свойством сложных эфиров является взаимодействие их с водой. Если какой-либо эфир, например этиловый эфир уксусной кислоты, нагревать с водой в присутствии неорганической кислоты, то образуются уксусная кислота и этиловый спирт:
Такая реакция называется гидролизом. Она противоположна реакции образования сложного эфира. Поэтому если нагревать смесь спирта и карбоновой кислоты, то происходит не только этерификация, но и гидролиз образующегося эфира. Это значит, что реакция этерификации обратима. Скорость обратного процесса при этерификации возрастает по мере того, как увеличивается количество эфира и воды в смеси. Наконец, скорости реакций этерификации и гидролиза становятся равными. Наступает химическое равновесие, и количество эфира в смеси практически более не увеличивается.
В общем виде уравнение выглядит так:
Чтобы сместить равновесие этой реакции в сторону образования сложного эфира, нужно помешать образующимся веществам реагировать друг с другом, например отгонять эфир из смеси веществ или связывать выделяющуюся воду водоотнимающими веществами.
Если же, наоборот, требуется гидролизовать эфир, т. е. разложить его водой на кислоту и спирт, можно проводить реакцию в присутствии щелочи. Она будет превращать кислоту в соль и тем самым устранять возможность ее реакции со спиртом. Далее из соли легко получить нужную кислоту.
Ненасыщенные карбоновые кислоты ведут себя как насыщенные карбоновые кислоты и как алкены. В то же время сочетание в молекуле карбоксильной группы и сопряженной двойной связи приводит к появлению определенных специфических свойств. Алкеновые карбоновые кислоты образуют все обычные производные кислот (соли, галогенангидриды, ангидриды, эфиры) и вступают практически во все реакции присоединения, свойственные алкенам, легко окисляются.
Однако присоединение несимметрично построенных реагентов таких как HBr, HC1, HI, Н2О к алкеновым кислотам, у которых двойная связь расположена рядом с карбоксильной группой, проходит против правила Марковникова, с промежуточным образованием продукт том присоединения.
4. Продукты переработки жиров
Гидролиз жиров в технике. Реакция гидролиза используется в технике для получения из жиров глицерина, карбоновых кислот, мыла.
Глицерин и кислоты образуются при нагревании жира с водой в автоклавах.
Гидрирование жиров. Для получения мыла и других веществ требуются преимущественно твердые жиры. Между тем они являются весьма ценным продуктом питания. Поэтому давно возникла мысль превращать более дешевые растительные масла в твердые жиры, которые затем можно было бы подвергать той или иной технической переработке.
Сущность способа заключается в том, что через нагретую смесь масла с тонко измельченным катализатором (никелевым или медно-никелевым) пропускают водород под давлением. Водород присоединяется по месту двойных связей в углеводородных радикалах, и масло превращается в твердый жир, например:
В промышленности процесс гидрирования осуществляют в ряде последовательно соединенных автоклавов по непрерывному методу. Проходя через систему автоклавов, жир подвергается все большему гидрированию; в результате получается масса, похожая по своей консистенции на сало. Поэтому гидрированное масло называют еще саломасом. От катализатора саломас отделяется при помощи фильтрования.
В состав мыла входят соли карбоновых кислот. Сейчас такие кислоты получают в промышленности окислением углеводородов, входящих в состав парафина. Процесс ведут в аппаратах колонного типа, продувая через расплавленную смесь углеводородов воздух при температуре около 120°С в присутстствии соединений марганца в качестве катализатора.
В результате образуется смесь различных кислот и других кислородсодержащих соединений, которую подвергают разделению. Нейтрализацией кислот получают соли. Эти соли (в смеси с наполнителем) идут на производство туалетного и хозяйственного мыла.
Мыла, получаемые из синтетических кислот, будучи аналогичны по своей химической природе обычным мылам, обладают и их недостатками. Например, они плохо моют в жесткой воде. Поэтому сейчас развивается производство моющих средств другого типа.
Синтетические моющие вещества входят в состав широко известных стиральных порошков «Астра», «Лотос», «Кристалл» и др.
вытапливание из жировых мускульных и соединительных тканей кашалота
для получения саломас
Для изготовления вазелина, губных помад, крема, грима.
Копытный жир (бычье сало)
Густотекущая масса белого цвета, имеет запах говяжьего сала.
Вытапливание жирных частей КРС.
Витамин Г, питательный крем и средство для укрепления волос.
Твердое вещество желтого цвета.
Вытапливание и вываривание из жиросодержащих тканей.
В лучших сортах мыла.
Мазеобразное вещество белого цвета.
Вытапливание и вываривание из жиросодержащих тканей.
Для помад, мыла, стеарина.
Метало-кристалл, тв. жирные кислоты белого цвета.
Крема для кожи, мыла, губных помад и др.
Цвет от светлого до темно-желтого, имеет легкий запах.
Из отходов переработки кур и цыплят
Для получения помад, кремов, питательных смягчающих, детской косметики.
Твердой консистенции желтого цвета
Горячее прессование мякоти кокоса.
Для дорогих сортов мыла и синтетических масло какао.
Очень нежный легко плавящийся жир
Для губных помад и кремов.
Желтого цвета с запахом миндаля
Холодное прессование горького и сладкого миндаля
Твердая крупяная масса с мелкозернистым изломом белого цвета.
Продукт жизнедеятельности пчел.
В эмульсионных кремах.
Пластичные воскообразные кристаллы белого цвета с легким запахом.
Вымораживанием спермацитового жира
В питательных кремах.
От светлого до темно-желтого цвета. Мазеобразное, запах неприятный
При мытье овечьей шерсти из промывных вод
Ценный компонент в эмульсионных кремах
Получают из бутонов розы.
Регулирует вязкость кремов и помад.
Твердый, темно-зеленого цвета
Средства для ухода за волосами и в декоративной косметике.
Твердый, хрупкий продукт темного цвета.
Из листья бразильской восковой пальмы.
Используют в туши для ресниц, гриме, помаде.
От светло-зеленого до бурого цвета с запахом керосина
Из горных пород торфа и нефти
Для парафина и переработки в целезин.
Воскообразное вещество мелкокристаллического вида. От белого до коричневого цвета.
Из ископаемых восков.
Для вазелина, крема для снятия макияжа, губной помады, туши.
твердая воскообразная консистенция цвета от белого до светло-желтого
твердая воскообразная консистенция цвета от белого до светло-желтого
Размещено на Allbest.ru
Подобные документы
Природные органические соединения, полные сложные эфиры глицерина и одноосновных жирных кислот. Применение растительных и животных жиров. Жидкие жиры растительного происхождения. Свойства, биологическая роль, промышленное производство жиров и масел.
презентация [251,9 K], добавлен 06.05.2011
Характеристика природных животных и растительных жиров. Кислоты как их составляющая, классификация, свойства, разновидности. Физические и химические свойства жиров. Химические формулы сложных липидов и строение биологических мембран, описание свойств.
курсовая работа [423,3 K], добавлен 12.05.2009
Изучение физических свойств сложных эфиров, которые широко распространены в природе, а также находят свое применение в технике и промышленности. Сложные эфиры высших карбоновых кислот и высших одноосновных спиртов (восков). Химические свойства жиров.
презентация [869,6 K], добавлен 29.03.2011
Роль жиров в здоровом питании спортсменов. Растительные и животные жиры, их физические свойства. Получение жиров по реакции глицеринового спирта с высшими карбоновыми кислотами, реакция этерификации. Особенности гидролиза жиров (омыления), гидрирование.
презентация [284,2 K], добавлен 18.09.2013
Переваривание жиров в кишечнике. Расщепление жиров в процессе пищеварения. Эмульгирование и гидролиз липидов. Полный ферментативный гидролиз триацилглицерола. Кишечно-печеночная рециркуляция желчных кислот. Причины нарушений переваривания липидов.
реферат [886,1 K], добавлен 12.01.2013
Общая характеристика состава жиров. Жирные кислоты, ненасыщенные (предельные) жирные кислоты, ненасыщенные (непредельные) жирные кислоты. Классификация жиров. Растительные, животные жиры. Применение того или иного жира. Значение жиров в кулинарии.
курсовая работа [32,1 K], добавлен 25.10.2010
Жиры и жироподобные вещества как производные высших жирных кислот, спиртов или альдегидов. Химические и физические свойства липидов. Реакция образования акролеина, компоненты жиров. Схема гидролиза. Гидролитическое прогоркание. Подлинность жирных масел.
реферат [126,5 K], добавлен 24.12.2011