Как восстанавливается эпидермис при повреждении
Как восстанавливается эпидермис при повреждении
Нарушить барьерную функцию кожи можно разными путями. Например, как сейчас, — путем нарушения структуры гидролипидной мантии обработкой органическими растворителями (спирт) или ПАВ, посредством физического разрушения рогового слоя (пилинг, дермабразия, лазерная шлифовка). Есть еще один способ ослабить барьерные свойства кожи — изменить состав поверхностных липидов, что произойдет, например, в результате длительного ограничения приема пищевых жиров или продолжительного применения большого количества косметического масла (любого!).
Сразу же после физического повреждения рогового слоя скорость испарения воды с его поверхности резко возрастает. Затем в течение нескольких часов она постепенно снижается, что говорит о том, что барьерный слой снова восстанавливается. Если проследить всю динамику восстановления барьерной функции кожи, то можно видеть, что сначала восстановление идет довольно быстро. У человека барьерная функция восстанавливается на 60% через 12 ч, но полное восстановление занимает 72 ч. Считается, что быстрое восстановление происходит за счет массового выброса из гранулярных кератиноцитов уже готовых ламеллярных телец. В медленную фазу восстановления барьера происходит усиление синтеза жирных кислот, холестерина и церамидов, а также образование новых ламеллярных гранул.
В ответ на повреждение рогового слоя кератиноциты секретируют ряд сигнальных молекул — цитокинов, факторов роста. Установлено, что сразу после повреждения рогового слоя повышается концентрация ИЛ-1а (интерлейкин 1а), TNFα (фактор некроза опухолей альфа) и некоторых других цитокинов. Точная роль этих молекул в восстановлении эпидермального барьера пока не известна, но сам факт повышения их концентрации важен. Скорее всего, они стимулируют синтез липидов и образование ламеллярных гранул в эпидермисе, но они же могут вызывать появление гиперпигментации, воспаления и эпидермальной гиперплазии. Показано, что даже незначительное, но систематическое повреждение барьерного слоя (например, частое умывание горячей водой с мылом) приводит к возникновению гиперплазии эпидермиса, что говорит о том, что цитокины, вырабатываемые кожей при повреждении рогового слоя, могут инициировать патологические процессы.
Нанесение на кожу различных веществ может помочь или, напротив, затормозить восстановительные процессы.
Полная окклюзия
Если на кожу наложить полиэтиленовую или резиновую пленку, то секреции ламеллярных телец и увеличения синтеза липидов не происходит. Более того, сейчас актуальна проблема с тем, что сама окклюзия — ношение резиновых перчаток, может стать причиной повреждения барьерной функции кожи, ведь повышенная влажность приводит к повышению проницаемости кожи.
По всей видимости, увеличение скорости испарения воды через роговой слой является главным сигналом к восстановительным работам при разрушении барьерных структур. Непроницаемая пленка, которая не позволяет воде испаряться, блокирует ответ клеток эпидермиса на повреждение.
Частичная окклюзия
Если кожу с разрушенным роговым слоем покрыть слоем вазелина, то в первые часы после повреждения наблюдается замедление восстановления. На электронных микрофотографиях в гранулярном слое эпидермиса можно видеть деформированные (словно поеденные молью) ламеллярные тельца. Это говорит о том, что вазелин в какой-то мере проникает в гранулярный слой эпидермиса и нарушает формирование ламеллярных телец. Тем не менее тонкий слой вазелина не препятствует газообмену, как это делает полиэтиленовая пленка. И некоторое количество трансдермальной воды через нее испаряется, а кислород и углекислый газ нормально проходят.
Поэтому в итоге под слоем вазелина восстановление барьера завершается быстрее, чем без него. Временный барьер, который создает вазелин, защищает кожу от сильного обезвоживания и проникновения токсических веществ. Поэтому клетки могут успешнее работать над восстановлением барьера, не отвлекаясь на борьбу с внешним стрессом.
Физиологические липиды
Если вазелин при нанесении на кожу лишь в незначительной степени проникает внутрь, то физиологические липиды (церамиды, нейтральные жиры, жирные кислоты, холестерин) ведут себя совершенно иначе. Используя флуоресцентные метки, удалось показать, что эти молекулы с легкостью преодолевают роговой слой и проникают в живые клетки эпидермиса. Поскольку в клетках кожи есть все необходимые ферменты для переработки экзогенных липидов, липидные молекулы, проникшие извне, быстро разбираются на «запчасти», из которых строятся липиды эпидермиса.
Тем не менее, если обратиться к динамике восстановления кожи, то будет видно, что эффективное восстановление ее барьерной функции наблюдается лишь при использовании смеси трех ключевых липидов кожи — церамидов, холестерина, жирных кислот, взятых в определенном соотношении. В ходе многолетних экспериментов удалось подобрать соотношение физиологических липидов в смеси, оптимальное для скорейшего восстановления барьера — 3:1:1. Обращаем внимание на то, что это молярная пропорция, отражающая соотношение числа липидных молекул в смеси и означающая, что на три молекулы одного вида липидов приходится по одной молекуле двух других видов. Примечательно, что липидную смесь следует адаптировать под конкретное состояние кожи:
1 (церамиды) : 1 (холестерин) : 3 (незаменимые жирные кислоты);
1 (церамиды) : 3 (холестерин) : 1 (незаменимые жирные кислоты);
3 (церамиды) : 1 (холестерин) : 1 (жирные кислоты).
С практической точки зрения важно, что свободные жирные кислоты можно заменить триглицеридами или фосфолипидами и все еще получить быстрое восстановление барьера. Можно заменить церамиды сфингомиелином или холестерин эфирами холестерина без какого-либо ущерба для процесса восстановления. Это подтверждает наличие в коже очень активных ферментов, с помощью которых клетки эпидермиса могут использовать экзогенные липиды для синтеза собственных липидов.
Быстрое восстановление барьерной функции наблюдается лишь в том случае, если три ключевых липида (церамиды, холестерин, жирные кислоты) присутствуют в необходимом соотношении. При этом неважно, использована концентрированная или разбавленная липидная смесь, важно, чтобы пропорция ключевых липидов в ней сохранилась.
Натуральные масла
С тех пор как была установлена исключительная роль незаменимых жирных кислот в физиологии кожи, в косметологии большую популярность приобрели натуральные масла. Зачастую их наносят на кожу в чистом виде. С одной стороны, казалось бы, идея хорошая. Натуральные масла не содержат никаких посторонних химических веществ, и многие из них богаты дополнительными активными компонентами, такими как фитостерины, витамин Е, каротиноиды. Однако увлекаться чистыми маслами все-таки не стоит. Напомним, что целостность липидных пластов рогового слоя поддерживается точным соотношением всех липидных компонентов — церамидов, холестерина, свободных жирных кислот. Масла являются по своей природе нейтральными жирами, в основе которых триглицериды. Хотя они могут быть разобраны на составные части с высвобождением свободных жирных кислот, сначала они должны проникнуть через липидные пласты. Если масла слишком много, оно будет разбавлять липидные пласты, временно нарушая их структуру. Обычно структура пластов быстро восстанавливается. Однако слишком обильное и частое применение масел может привести к стойкому нарушению барьерной функции кожи. Все хорошо в меру.
В составе косметических средств натуральные масла обычно содержатся в небольших количествах, поэтому они не так заметно влияют на структуру барьера.
Информацию по составу и свойствам растительных масел, использующихся в косметике и для ухода за кожей, а также нюансы, касающиеся использования физиологических липидов и средств для создания окклюзии вы найдете в наших книгах «НОВАЯ КОСМЕТОЛОГИЯ. Косметические средства: ингредиенты, рецептуры, применение», «Косметическая химия для косметологов и дерматологов» и «НОВАЯ КОСМЕТОЛОГИЯ. Основы современной косметологии. 2-е издание, переработанное и дополненное». Они все доступны в электронном виде, и вы можете познакомиться с ними уже сегодня!
Гидролипидная мантия кожи. Кожа и два ее барьера
Гидролипидная мантия кожи – одна из составляющих эпидермального барьера кожи.
Здоровье кожи в широком смысле этого слова – её качество, цвет, тонус, увлажненность и т.п. – напрямую зависит от состояния эпидермального барьера. Многие дерматологические проблемы возникают именно из-за «брешей» в его работе.
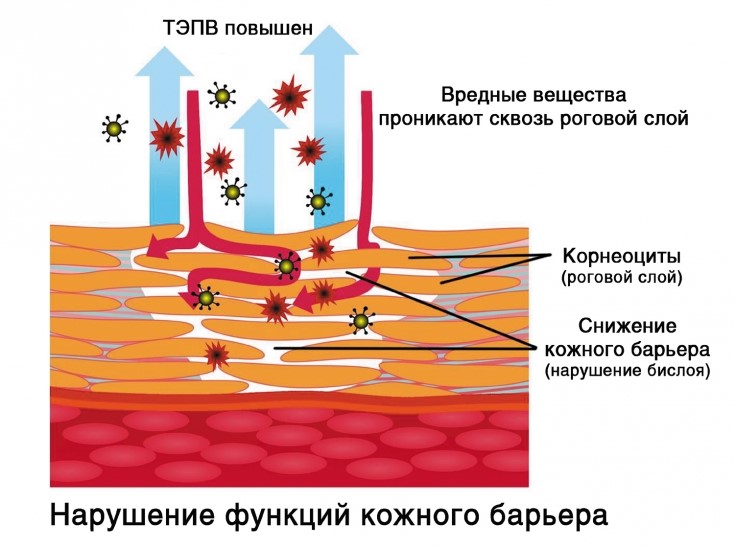
Нарушения функции и дефекты в этом барьере неизбежно провоцируют проникновение чужеродных микробов и аллергенов в кожу, активируют дегидратацию эпидермиса и вызывают сухость кожи, повышают её чувствительность к различным воздействиям окружающей среды.
Что же такое эпидермальный барьер
Кожа – самый большой орган человеческого тела. Она составляет почти 18% общего веса человека.
В составе кожи три основных слоя:
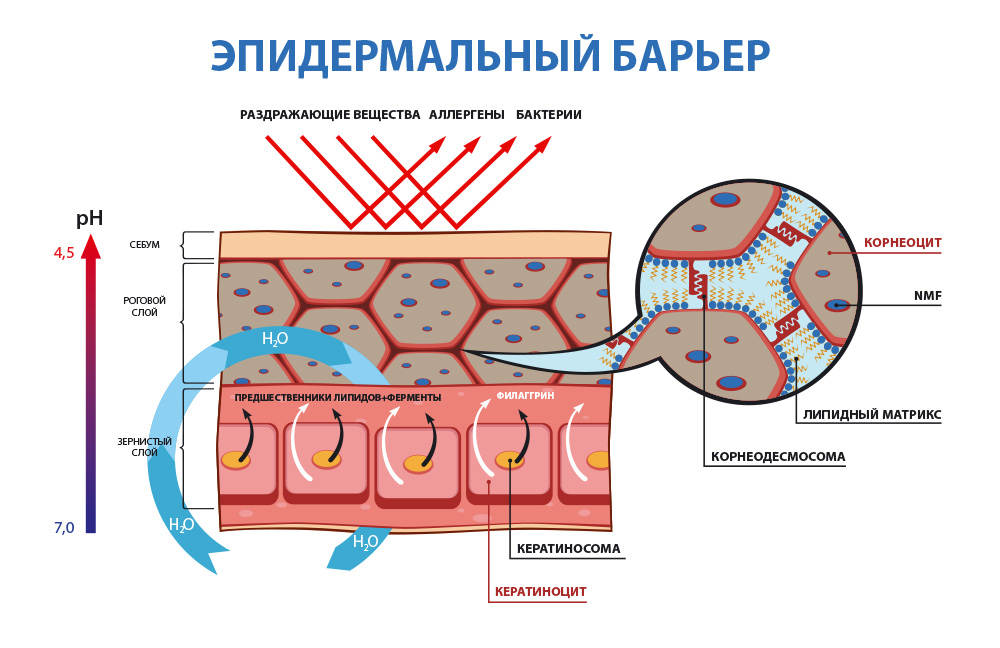
Эпидермальный барьер состоит из:
1. Гидролипидная или водно-жировая мантия
— это, некая, невидимая глазу пленка на поверхности кожи, которая образуется из смеси отслоившихся роговых чешуек, пота, кожного сала, а также органических кислот и микрофлоры.
Благодаря наличию кислой среды, в которой перестают размножаться и погибают вредоносные бактериии, гидролипидная мантия является самым первым звеном защиты кожи от большинства чужеродных микроорганизмов и агентов.
Кислотность гидролипидной мантии может нарушаться в ту или иную сторону по разным причинам (будет описано ниже). Например, при грибковых заболеваниях рН возрастает до 6, при экземе до 6,5; при угревой болезни защелачивается до 7.
Повреждённая гидро-липидная мантия кожи восстанавливается самостоятельно при правильном очищении, грамотном уходе и защите.
2. Липидо-эпидермальный барьер
– основной защитный барьер кожи. Находясь непосредственно в эпидермисе, он защищает организм и кожу от обезвоживания путем механизма транс-эпидермальной потери влаги (ТЭПВ), а также является вторым звеном защиты после гидролипидной мантии от проникновения в кожу патологических бактерий и аллергенов, различных химических соединений.
Основу липидо-эпидермального барьера составляют три вида липидов — церамиды, свободные жирные кислоты и холестерин.
Механизм ТЭПВ. По большому счету кожа увлажняется изнутри – то есть из глубоких слоёв гиподермы и дермы вода поступает к эпидермису, липиды удерживают воду в эпидермисе, обеспечивая его увлажненность. Повреждённый липидо-эпидермальный барьер является главной причиной неадекватной трансэпидермальной потери влаги и в результате сухости кожи. Поэтому, чтобы обеспечить хорошую увлажненность кожи, необходимо в первую очередь восстановить липидный барьер.
Кроме того, бреши в липидо-эпидермальном барьере приводят не только к обезвоженности кожи, но и к её повышенной чувствительности, аллергическим реакциям, раздражениям и кожным заболеваниям.
Незначительные повреждения липидо-эпидермального барьера клетки кожи восстанавливают сами. В случае выраженных нарушений – им необходимо помочь. В первую очередь это процедуры регулярного увлажнения, правильного ухода за поверхностью кожи и дермы, здоровый образ жизни и сбалансированное питание.
Внешние проявления, связанные с повреждением гидролипидной мантии
Наличие вышеперечисленных проблем – повод обратиться к дерматологу.
Факторы, повреждающие кожные барьеры
Применение при очищении кожи мыла, умывалок и др., содержащих ПАВы и щелочи; частое использование обезжиривающих и спиртовых тоников.
Щелочи и ПАВы, присутствующие в большинстве очищающих средств нарушают кислый pН гидролипидной мантии. В результате водно-жировая мантия разрушается. Открываются входные ворота для чужеродных бактерий. Повреждается липидный барьер, вода активно начинает испаряться с поверхности кожи, вызывая её сухость.
Здоровый эпидермальный барьер — залог красивого вида любого типа кожи — жирной, проблемной, сухой, чувствительной и даже увядающей.
Сохранение и восстановление эпидермального барьера один их самых ключевых принципов в профессиональных программах по уходу за любым типом кожи и омолаживающих врачебных процедурах, а также домашнего хода за кожей.
Методы восстановления и сохранения барьеров кожи
Адекватное очищение кожи.
Домашний уход. Важно правильно определить с профессиональным дерматологом свой тип кожи и использовать ежедневно очищающие средства, которые соответствуют вашему типу кожи, не нарушая при этом эпидермальный барьер.
Профессиональный уход. В условиях клиники – проведение грамотно подобранных процедур очищения и эксфолиации кожи и соблюдения режима их выполнения: химического пилинга, и лазерного пилинга,ручной чистки лица с учётом вашего типа кожи и решаемых проблем.
Регулярное увлажнение.
Домашний уход. Ежедневно наносите на кожу увлажняющие кремы и периодически маски, содержащие компоненты, удерживающие влагу: аминокислоты, гиалуроновую кислоту, коллаген, эластин, алое вера и др. Плюс, как это ни банально, пейте адекватное количество чистой воды.
Профессиональный уход в условиях клиники. Регулярно (курсами 2 раза в год) проводите процедуры биоревитализации, биорепарации, мезотерапии
Профессиональный уход в условиях клиники. При повреждении кожи и развитии патологической флоры, например при угревой болезни – применение различных медикаментозных препаратов, назначенных врачом, а также лечение акне на лазерной установке Fotona с целью инактивации патологической флоры, уменьшения воспалительного процесса и улучшения трофики тканей.
Сбалансированное питание и уход.
Домашний уход. Ежедневно используйте питательные крема, соответствующие вашему типу кожи, возрасту и времени сезона года, чередуйте их с увлажняющими средствами. Отдавайте предпочтение средствам, содержащим церамиды, липосомы и жирные кислоты – они защищают и восстанавливают повреждённый липидный слой.
Употребляйте в пищу продукты, богатые омега 3 и омега 6 жирными кислотами. Не исключайте из рациона масла и жиры.
Постоянная защита.
Подводим итоги
Здоровье кожи напрямую зависит от целостности и нормального функционирования эпидермального барьера, основу которого составляет гидро-липидная мантия и липидо-эпидермальный барьер.
Сверху эпидермальный барьер «окутан» в гидролипидную мантию. Важно бережно относиться к ней и не повреждать её. Она первая «встречает» патогенные микробы и агенты, препятствуя их проникновению вглубь кожи.
Повреждение липидо-эпидермального барьера и гидролипидной мантии является серьёзной проблемой для кожи. Как правило, это приводит к обезвоживанию эпидермиса, появлению сухости, повышенной чувствительности, раздражениям, может спровоцировать и поддерживать кожные заболевания и др.
Нарушенный эпидермальный барьер можно восстановить, если правильно подобрать домашний уход, а также проводить профессиональные процедуры у косметолога. Сбалансированный уход за кожей и правильный образ жизни обеспечат защиту, увлажнение и восстановление кожи.
Медицинские интернет-конференции
Языки
Регенерация кожи
Грамкова И.И, Максимова Е.Р.
Регенерация кожи
Грамкова И.И, Максимова Е.Р.
Научный руководитель: Уварова И.А., Романова Т.П.
ГБОУ ВПО Саратовский ГМУ им.В.И. Разумовского Минздрава России
Регенерация-это восстановление как структуры, так и функции органов и тканей после их повреждения или утраты части. Процессы регенерации могут идти на самых уровнях организации живой системы, поэтому различают внутриклеточную регенерацию; клеточную регенерацию; тканевую регенерацию; регенерацию на органном уровне, она бывает физиологическая и репаративная. Физиологическая регенерация-это регенерация биологических структур после их естественного износа при нормальном функционировании. Репаративная регенерация-восстановление биологических структур после повреждения (усиленная физиологическая регенерация). Она включает процессы распада поврежденных клеток, дифференцировку сохранивших жизнеспособность клеток, их пролиферацию, вторично дифференцировку размножившихся клеток, установление межклеточных связей и адаптационную перестройку клеток регенерата. При повреждении кожи в силу вступает ответная реакция, имеющая нервно-гуморальный механизм регулирования, направленный на восстановление целостности кожи. Скорость регенерации кожи зависит от глубины и площади повреждения,состояния иммунитет кожи и от того, как протекает микроциркуляция в сосудистом русле кожи. Результат регенерации кожи: полное заживление; гиперпигментация; депигментация;атрофичная кожа;образование физиологических рубцов; образование патологических рубцов и контрактур.
Скорость эпителизации раны зависит также и от сохранившихся остатков базальной мембраны с базальными кератиноцитами эпидермиса, клеток волосяных фолликулов, сальных желез. При поверхностном повреждении кожи без затрагивания базальной мембраны и верхушек сосочков, регенерация кожи всегда проходит без образования рубцов. Это достигается путем усиленной пролиферации базальных кератиноцитов (царапины, ссадины, ожоги II степени). При повреждении кожи с затрагиванием верхушек сосочков, вследствие которого повреждается базальная мембрана и капилляры поверхностной сосудистой сети, регенерация кожи, как правило, проходит без образования рубцов и протекает за счет сохранившихся фрагментов базальной мембраны, клеток волосяных фолликулов и эпителия сальных желез. При таком заживлении кератиноциты начинают активно делиться и устремляться на дно раны, а также переходят с краев. Сначала создается одиночный слой клеток, а затем многослойный, под которым и идет завершение этого процесса регенерации кожи. При поражениях на данной глубине кожи из-за влияния солнечных лучей могут образовываться гиперпигментации-это связано с тем, что повреждение петель капилляров, служит стимулом тучных клеток для выделения биологически активных веществ в кожу (гистамина, серотонина), стимулирующих меланоциты к выработке меланина, который затем поглощается кератиноцитами и придает им специфический темный цвет. Если при том же раскладе присоединяется инфекция, то возможна депигментация кожи или ее атрофия. При повреждении кожи ниже эпидермиса, на границе сосочкового и сетчатого слоя дермы, регенерация кожи почти всегда проходит с образования рубца (ожоги III степени). Рубцы при таком повреждении могут быть от нормотрофических и атрофических до гипертрофических и келоидных. При глубоком повреждении кожи с разрушением нижележащих тканей, таких как подкожно жировая клетчатка, мышцы, регенерация кожи протекает с формированием деформирующих рубцов.
Как восстанавливается эпидермис при повреждении
В повседневной суете кожа человека подвержена различным повреждениям. Это связано с прямым контактом ее с окружающей средой. В коже хорошо развиты процессы репаративной регенерации, в основе которых лежат механизмы миграции и митотического деления эпидермальных клеток и клеток дермы (фибробластов) [2]. Проблемой восстановления поврежденных тканей занимаются с давних пор и получены важные результаты.
Однако, в последнее время участились случаи термического поражения кожи из-за взрывов, пожаров, и это требует быстрой и качественной терапии. Целью нашего исследования явилось изучение репаративной возможности покровных тканей при термических ожогах в условиях воздействия биологически активных веществ (БАВ) пуповинной крови [1,5].
Характер течения репаративного процесса оценивали визуально в дни измерений площади ран, а также по результатам гистологического исследования кожи, иссеченной из краев раны в конце 3-й недели. На автоматизированном морфометрическом комплексе «Морфолог» оценивали толщину росткового слоя ЭП в краях эпителизации ран по результатам не менее чем 30 для каждой группы животных и клеточную плотность дермы. Статистическую обработку результатов исследований проводили с использованием t-критерия Стьюдента. Различия средних считали значимыми с уровнем вероятности не менее 95% (в таблицах отмечены звездочкой).
При аппликациях мазей с биологически активными веществами пуповинной крови рожениц [6] на раневую поверхность уже в начале 2-й недели после нанесения термического ожога имела место более выраженная в сравнении с контрольными группами животных, тенденция к уменьшению площади раневой поверхности (табл. 1, стр. 7).
Полная эпителизация раневой поверхности ранее всего наблюдалась у отдельных животных при аппликации синтомициновой эмульсией.
Одной из причин более быстрого заживления ожоговых ран при использовании аппликаций с БАВ пуповинной крови человека является, на мой взгляд, их стимулирующее влияние на клеточную пролиферацию в эпителии кожи, на что косвенно указывают результаты измерения толщины росткового слоя Эп в краях эпителизации.
Так, через 3 недели после начала эксперимента у животных без воздействия и при аппликации пуповинной крови этот показатель составил соответственно 23,8 ± 0,8 мкм и 22,2 ± 0,8 мкм. Толщина росткового слоя Эп после использования синтомициновой эмульсии в этот же период наблюдения составила 33,6 ±1,0 мкм. Вероятность различий с показателями в контрольных группах животных составила 99,9%.
Во всех случаях в зоне раны отмечены признаки воспаления: расширение сосудов дермы под раневой поверхностью и ее клеточная инфильтрация, выраженные, однако, неодинаково в различных группах. В обеих контрольных группах и у животных, получавших ВЭО, отмечалось большое количество серозно-гнойного экссудата, содержащего преимущественно нейтрофилы и локализованного под поверхностными некротическими массами и вблизи края эпителизации. При использовании синтомициновой эмульсии полнокровие сосудов было менее выражено, гнойный экссудат отсутствовал.
Результаты анализа клеточного состава дермы под раневой поверхностью через 3 недели после нанесения ран (табл. 2, стр. 7) коррелируют с указанными выше особенностями течения раневого процесса при использовании разных аппликаций.
Так, в сравнении с животными контрольных групп, суммарное число клеточных элементов в дерме, подсчитанное на поле зрения микроскопа, значимо снижается при аппликации синтомициновой эмульсией. При этом наблюдается отчетливо выраженный сдвиг в сторону клеток фибробластического ряда, что в совокупности свидетельствует о более быстром разрешении в этих условиях воспалительного процесса, развивающегося в месте ожога.
Таким образом, накожные аппликации в составе мягких лекарственных форм оказывают ранозаживляющее действие, модифицируя течение воспалительного процесса в сторону активизации фибробластической реакции [3].
Таблица 1. Динамика изменений площади ожоговых ран (в см 2 ) при использовании разных аппликаций (п=12)
Как восстанавливается эпидермис при повреждении
Несмотря на достижения молекулярной биологии, возможности лабораторного синтеза факторов роста клеток, современного уровня развития тканевой инженерии, проблема восстановления утраченного кожного покрова при повреждениях различной этиологии до сих пор по-прежнему актуальна 3. После тяжелых ранений и операций на теле остается чаще всего некрасивый и огромный шрам. Регенерация органов становится многообещающим выбором для многих пациентов, однако многие подробности о механизмах восстановления остаются неизвестными.
Цель работы: провести анализ современных исследований в сфере открытий и решений проблем регенерации кожи.
Миофибробласты рыхлой волокнистой соединительной ткани являются превалирующим типом клеток, который присутствует в грануляционной ткани стягивающихся ран, а также находятся в некоторых развивающихся или нормальных взрослых тканях. Было выявлено, что миофибробласты можно превратить в жировые клетки, перепрограммируя их. Предполагаемая функция миофибробластов заключается в изменении натяжения ткани, а жировые клетки или адипоциты находятся в коже до тех пор, пока не образуется рубцовая ткань. Логично предположить, что каким-то образом необходимо заменить миофибробласты адипоцитами, чтобы не произошло образование рубца. Рубцовая ткань отличается от эпителия отсутствием волосяных фолликулов. Ученые пришли к выводу, что волосяные фолликулы и адипоциты связаны, и если восстановить волосяные фолликулы, они индуцируют увеличение жировых клеток в ответ на сигналы от фолликула. Как регенеративные образования, волосяные фолликулы предлагают хорошую модель для изучения механизмов, связанных с регенеративной медициной. В соответствующих исследованиях основное внимание уделялось донорским клеткам, и нет данных, связанных с влиянием факторов хозяина на реконструкцию волосяного фолликула [5].
Для начала, рассмотрим восстановление волосяных фолликулов при помощи изоляции трансплантированных клеток, проверив влияние факторов клетки-хозяина, то есть понять будет ли возможно развитие волосяного фолликула без клеток хозяина. Ученые отдела Пластической и эстетической хирургии Экспериментального центра Южного медицинского университета (Китай) провели целое исследование, посвященное образованию волосяного фолликула. Для эксперимента использовали шестнадцать новорожденных мышей, меченных красным флуоресцентным белком и двадцать четыре взрослых мыши с зеленым флуоресцентным белком. Все эксперименты над животными были проведены по согласованию с Комитетом по уходу и использованию животных Южного медицинского университета. Затем последовала подготовка клеток для трансплантации. Эпидермис и дерму разделили путем инкубации в течение ночи при температуре в 4 градуса по Цельсию. Потом кожу три раза промыли фосфатно-буферным физиологическим раствором, окончательно отделяя дерму от эпидермиса. Из каждой части получили «фарш» путем измельчения дермы и эпидермиса [8].
Технология Cell-in-a-Box позволила инкапсулировать клетки в защитный, полупроницаемый шарик на основе целлюлозы. Небольшие поры в бусинах позволяют проходить обмену питательных веществ, но клетки внутри бусинок сохраняются. Бусины способны выдерживать до 6 месяцев в имплантате, иммунного ответа хозяина нет. Эти характеристики позволяют встроенным клеткам расти в течение более длительного времени, чем традиционная двумерная клеточная культура. Эта технология была выбрана, как метод исследования и анализа взаимодействия между средами-хозяина и трансплантированными клетками. Капсулы, содержащие дермальные клетки с зеленым флуоресцентным белком, которые получили от новорожденных мышат с красным флуоресцентным белком, были подкожно пересажены мышам без шерсти. Пустые капсулы пересадили как контрольную группу. Каждая группа состояла из 6 мышей, которым в целом было пересажено по 10 капсул. Клетки смесей с красным флуоресцентным белком вводили под поверхностный слой подкожных тканей мышам с зеленым флуоресцентным белком. Никаких побочных эффектов не наблюдалось после трансплантации капсулы. Это указывает на то, что трансплантированные клетки могли принимать все питание от хозяина, но при этом были изолированы от клеток-хозяев. Рана зажила без осложнений. Ученые пришли к выводу, что если инкапсулированные клетки получают достаточное количество питательных веществ от хозяина, то они могут образовывать зрелые фолликулы волос при изоляции от клеток-хозяев [4].
Волосяные фолликулы представляют собой весьма информативную модель для изучения механизмов в области регенерации. Различные исследования подтвердили, что волосяные фолликулы могут быть восстановлены путем пересадки соответствующих клеток, но механизм этого процесса не совсем ясен. Хорошо известно лишь то, что микроокружение играет важную роль в клеточной пролиферации и дифференцировке (рис. 1). Микросреда обычно состоит из следующих групп: клетки (лейкоциты, фибробласты и адипоциты), факторы роста (трансформирующий фактор роста, фактор роста эндотелия сосудов и фактор роста фибробластов), внеклеточный матрикс (ламинин, фибронектин, протеогликан), и сигнальные молекулы (например, костный морфогенетический белок).
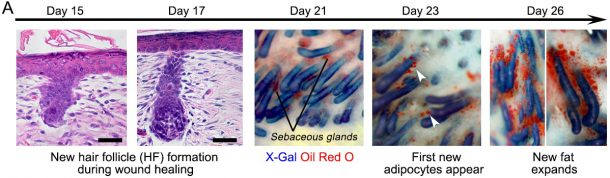
Рис. 1. Восстановление волосяных фолликулов и появление новых адипоцитов.
Ученые из Центра биологии развития RIKEN (Япония) успешно смогли создать ткань кожи, которая содержит волосяные фолликулы и сальные железы. Затем эту кожу имплантировали живым мышам, ткани образовывали связи с другими системами органов, такими как нервы и мышцы. Ученые использовали стволовые клетки для создания слоев кожи. Техническим термином для стволовых клеток, которые они использовали, являются перепрограммированные iPS-клетки. Команда доктора Цудзи взяла клетки из десен мышей и использовала химические вещества, чтобы превратить их в iPS-клетки. Затем они культивировали клетки, трансплантировав их на мышей, где они превращались в функционирующую ткань кожи. Как только клетки кожи дифференцировались, их пересаживали на разных мышей, где они начали естественным образом расти с фолликулами и железами и развивали связи с нервами и мышцами. Таким образом, биоинженерная кожа способна расти так же естественно, как и нормальная кожа без трансплантации [7].
До сих пор искусственное развитие кожи было затруднено тем фактом, что на коже не хватало волосяных фолликулов и экзокринных желез, которые играют важную роль в регуляции. Мы все ближе приближаемся к мечте о возможности воссоздания реальных органов в лаборатории для трансплантации, а также считаем, что ткань, выращенная этим методом, может быть использована в качестве альтернативы тестированию на животных химических веществ.
После того как стал понятен принцип регенерации волосяного фолликула возвратимся к начальной теме. Данное открытие было сделано при совместной работе ученых из Медицинской школы Перельмана в университете Пенсильвании и Лабораторией развития и регенеративной биологии Пликуса в Калифорнийском университете в Ирвине. Кристиан Ф. Герреро-Хуарес тесно сотрудничавший с проектом, комментировал открытие: «Как правило, миофибробласты, первичный тип клеток, обнаруженный в ранах, считались неспособными стать другими типами клеток. Однако наша команда обнаружила, что миофибробласты ран могут эффективно и стабильно превращаться в новые различные типы клеток, в частности новые адипоциты, необходимыми для здоровой кожи. В нашем исследовании установлено, что раны с волосяными фолликулами имеют факторы, которые могут перепрограммировать миофибробласты в адипоциты».
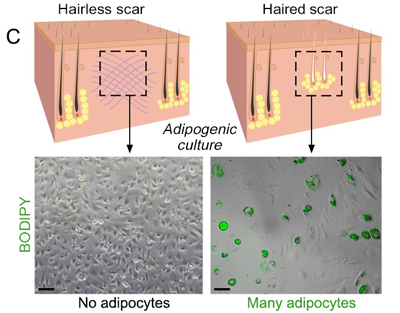
Раневым заживлением можно манипулировать, поэтому оно приводит к регенерации кожи, а не к образованию рубцов. Цель состоит в том, чтобы регенерировать волосяные фолликулы раньше. Как только это произойдет, жир будет регенерировать в ответ на сигналы, исходящие от этих фолликулов (рис. 2). Исследование также показало, что волосы и адипоциты могут развиваться отдельно, но зависимо. Сначала формируются волосяные фолликулы. Регенерирующим волосяным фолликулом образуются дополнительные факторы, которые служат для преобразования окружающих миофибробластов в жировые клетки, чтобы избежать образование шрама. Жировая ткань не образуется при отсутствии новых волос, но когда происходит восстановление волосяных фолликулов, новые клетки нельзя отличить от ранее существовавших жировых клеток. Исследователи определили, что костный морфогенетический белок инструктирует миофибробласты стать жировыми клетками [6, 9].
Рис. 2. Влияние волосяных фолликулов на преобразование адипоцитов.
Ученые разработали устройство, которое способно переключать функцию клетки только лишь одним касанием. Эта технология больше известна как тканевая нанотрансфекция, позволяющая в клетки кожи вводить генетический код, который изменяет их на другие типы клеток, необходимые для излечения. Перепрограммирование занимает несколько секунд: нужно коснуться чипом определенного места, а затем удалить его. В серии лабораторных тестов исследователи применили чип к конечностям мышей, которые практически не кровоснабжались из-за поврежденных сосудов. Исследователи перепрограммировали клетки кожи, чтобы они стали сосудистыми клетками. Через неделю начали появляться первые трансформации. Ко второй неделе образованы активные кровеносные сосуды, а к третьей неделе конечности мышей были спасены, при этом другой формы лечения не проводили [10].
Разница технологий заключается в том, как доставляется ДНК в клетки. Чип, нагруженный определенным генетическим кодом или определенными белками, помещается на кожу, а при помощи небольшого электрического тока создаются каналы в ткани. ДНК или РНК вводятся в полученные каналы и начинают перепрограммировать клетки. Этот метод эффективно работает до 98% не только на коже, но и на любом типе ткани. Ученые смогли вырастить клетки мозга на поверхности кожи мыши, собрать их, а потом перенести их в поврежденный мозг мыши. Всего через несколько недель после инсульта мозговая функция была восстановлена.
Заключение. Таким образом, регенерация эпителия без последующего образования соединительнотканного рубца вызвана функционированием миофибробластов. Регенерация ткани обусловлена ее перепрограммированием, которое вызывает сначала появление волосяных фолликулов, а они, в свою очередь, отвечают за регенерацию жировой ткани. Благодаря появлению волос на поврежденной ткани обеспечивается ее регенерация.