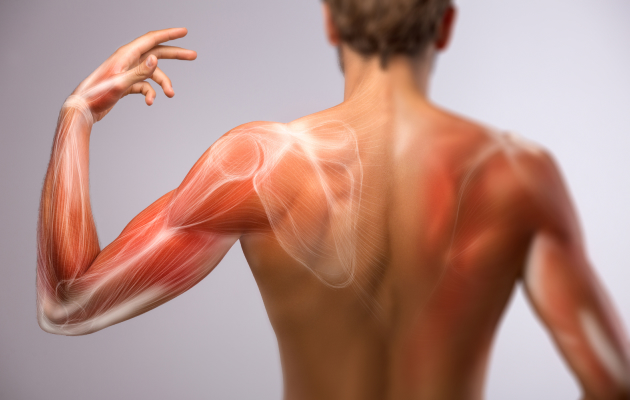
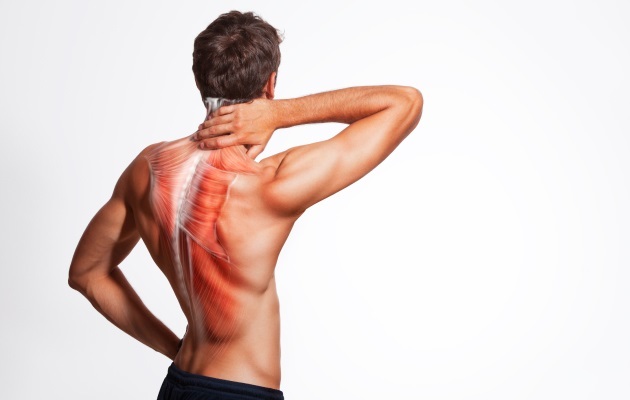
Как восстановить мышцы при атрофии
Причины развития, симптомы атрофии мышц, принципы и методы лечения
Симптомы и лечение атрофии мышц ног и рук
Атрофией мышц называют истончение их волокон и уменьшение общего мышечного объема. При этом мышечная ткань может заменяться соединительной тканью, которая не способна сокращаться. Именно так развивается атрофия мышц кисти, голени и других частей тела.
Причины развития атрофии мышц
Рассматриваемое патологическое состояние может развиться при воздействии различных провоцирующих факторов. Чаще всего атрофия мышц наблюдается у пожилых людей, что связано с естественными процессами старения: замедляется метаболизм (обмен веществ в мышечных тканях), снижается физическая нагрузка. Но есть и другие причины развития патологии:
В некоторых случаях спровоцировать проблему могут наследственные заболевания – например, причиной спинальной атрофии мышц являются генетические изменения в структурах нервной системы, которые делают невозможными произвольные сокращения мышц. Такие заболевания проявляются проблемами с мышцами уже в раннем детстве. Нередко именно атрофия мышц является единственным выраженным признаком заболевания, что нужно учесть в диагностике.
Немаловажную роль в развитии атрофии мышц играют питание и образ жизни – недостаток витаминов и микроэлементов в организме, злоупотребление алкоголем со временем приводят к рассматриваемой патологии.
Симптомы атрофии мышц
Лечению атрофии мышц ног и рук должна предшествовать диагностика патологии. Врачи подчеркивают, что необходимо обращать внимание на такие признаки:
Симптомы атрофии мышц никогда не появляются остро, они характеризуются постепенным нарастанием. Патология развивается постепенно, могут пройти годы, прежде чем она будет диагностирована. Но уменьшение объема пораженной мышцы может наблюдаться и на ранней стадии развития патологии.
Со временем атрофия мышц бедра приводит к невозможности долго и быстро ходить, подниматься по лестнице, может быть затруднен даже подъем с постели.
При атрофии сердечной мышцы пациент жалуется на неконтролируемое учащение или замедление сердцебиения, внезапные приливы жара к лицу, периодическое онемение пальцев верхних конечностей, одышку при физических нагрузках, а затем и в покое. Атрофические изменения в сердечной мышце считаются самыми опасными, так как при отсутствии адекватного лечения могут привести к летальному исходу.
Лечение атрофии мышц
Даже зная, какие заболевания сопровождаются атрофией мышц, врач должен назначить дополнительные методы обследования и только после постановки точного диагноза определит лечение. Часто после стабилизации общего состояния, остановки прогрессирования основной патологии либо переведения ее в состояние ремиссии исчезают и признаки атрофических изменений в мышечных тканях. При генетических заболеваниях полностью остановить прогрессирование описываемой патологии невозможно, но можно его замедлить.
Общие принципы лечения атрофии мышц подразумевают проведение:
Лекарственная терапия назначается в индивидуальном порядке. Это могут быть обезболивающие, нестероидные противовоспалительные средства, которые будут актуальными при сильном болевом синдроме. Индивидуальный подход особенно важен при выборе лечения патологии у детей – например, при лечении атрофии мышц голени у ребенка.
Важное значение в лечении имеют лечебная гимнастика и массаж. Упражнения для восстановления мышц при атрофии разрабатывают в индивидуальном порядке. Сначала они выполняются под контролем специалиста, дальнейшие занятия могут проводиться самостоятельно в домашних условиях.
Грамотное лечение, соблюдение всех рекомендаций врачей препятствуют прогрессированию патологии, больной может жить полноценной жизнью еще долгое время.
Более подробно о патологии, а также о том, кто из специалистов выполняет массаж при атрофии мышц нижних конечностей, можно узнать на страницах нашего сайта Добробут.ком.
Прогрессирующие мышечные дистрофии
Прогрессирующие мышечные дистрофии (ПМД) — гетерогенная группа наследственных заболеваний, характеризующихся прогрессирующей мышечной слабостью и атрофией скелетных мышц.
КЛИНИЧЕСКАЯ КАРТИНА
СИМПТОМЫ
При ПМД Дюшенна, Беккера, конечностно-поясных формах проявляется наиболее выраженная слабость в пояснично-подвздошных мышцах, мышцах бёдер, дельтовидных, дву- и трёхглавых мышцах плеча. Менее выражена слабость в дистальных мышцах конечностей. Лицевые мышцы остаются сохранными. Наряду с мышечной слабостью постепенно развиваются гипотрофии поражённых мышц вплоть до атрофии на поздних стадиях. При этом соседние мышцы могут быть полностью клинически интактны.
ЛЕЧЕНИЕ
Лечение должно производиться исключительно врачом-неврологом. Самолечение недопустимо. В настоящий момент радикального лечения ПМД не существует. Цель лечения — поддержание мышечной силы, предупреждение развития контрактур, деформаций суставов.
Немедикаментозное лечение
Чрезмерная физическая нагрузка, как и недостаточная, приводит к нарастанию мышечной слабости. Ежедневная ЛФК позволяет поддерживать мышечный тонус и препятствует развитию контрактур. Комплекс ЛФК обязательно должен включать активные и пассивные упражнения, упражнения на растяжку/предупреждение контрактур и дыхательную гимнастику. Активный массаж с разминанием мышц может усиливать мышечную слабость и утомляемость, поэтому рекомендуют щадящий массаж. Физиотерапевтическое лечение больные переносят по-разному: некоторые не ощущают улучшений или даже жалуются на усиление мышечной слабости.
Хирургическое лечение
В некоторых случаях возможно хирургическое лечение контрактур, однако при этом необходимо помнить о возможности увеличения мышечной слабости за время восстановительного лечения (вплоть до потери способности к ходьбе). В ряде случаев необходима имплантация кардиостимулятора.
Мышечные боли после коронавируса
Специалисты реабилитационного центра “Лаборатория Движения” помогут в восстановлении после перенесенной коронавирусной инфекции (COVID-19)
Большинство людей, переболевших COVID-19, сталкиваются с различными неврологическими проявлениями. При этом самыми частыми причинами обращения к врачу становятся артралгии и миалгии. Почему же после коронавируса болят мышцы и суставы, от чего зависит степень выраженности болевых проявлений и как бороться с последствиями заболевания?
Рассказывает специалист РЦ «Лаборатория движения»
Дата публикации: 29 Октября 2021 года
Дата проверки: 30 Ноября 2021 года
Содержание статьи
Распространенные осложнения после коронавируса
Еще не так давно основной постковидной проблемой считался фиброз легочной ткани. Однако сейчас уже существуют многочисленные доказательства затяжного поражения других органов и систем. Тяжелые воспалительные реакции и кислородная недостаточность влекут за собой ряд различных осложнений:
Пациентам, перенесшим заболевание, рекомендовано обращение к врачу при первых признаках тромбоза, так как отсутствие лечения вызывает необратимые последствия вплоть до ампутации конечностей или гибели.
Причины болей в мышцах после коронавируса
Суставные и мышечные боли после коронавируса обуславливаются следующими факторами:
У более, чем 55% пациентов наблюдаются локальные или диффузные мышечные боли после коронавируса, спонтанно возникающие как при напряжении, так и в состоянии покоя. В большинстве случаев их сопровождает болезненность в костях и суставах
Лечение мышц после Ковид-19
Основным направлением терапии постковидных скелетно-мышечных болей является эффективный контроль их механизмов и проявлений. Комплекс лечебных мероприятий включает:
Дополнительно может потребоваться психотерапевтическая помощь и процедуры для очищения крови.
В каких случаях требуется обратиться в больницу
Обязательным показанием к неотложной медицинской помощи является прогрессирующая мышечная слабость, ригидность или акинезия (невозможность произвольных движений) мышц. Обязательная госпитализация требуется людям, тяжело перенесшим заболевание и пациентам, у которых развивается аутоиммунная реакция на мышечную ткань (иммунно-опосредованная миопатия).
Что нужно знать о лечении мышц при коронавирусе
Лечебно-восстановительная программа, направленная на борьбу с последствиями COVID-19, для каждого конкретного пациента составляется индивидуально. В данной ситуации самолечение категорически противопоказано. А чтобы терапия действительно была эффективна, предварительно необходимо провести диагностическое обследование и выяснить истинную причину мышечно-суставных болей.
Какие осложнения могут возникнуть без своевременного лечения
Отсутствие своевременного лечения может повлечь за собой ряд серьезных последствий для здоровья:
Мышечно-тонический синдром
Специалисты реабилитационного центра “Лаборатория движения” помогут в восстановлении функций опорно-двигательного аппарата
Самым частым проявлением дегенеративных патологий позвоночника является мышечно тонический синдром. Длительное и стойкое напряжение мышц, отвечающих за поддержание стабильности позвоночных сегментов, приводит к формированию болезненных «триггерных точек». И только комплексное лечение, направленное на оптимизацию различных звеньев двигательной системы, позволяет существенно облегчить состояние пациента.
Рассказывает специалист ЦМРТ
Дата публикации: 29 Июня 2021 года
Дата проверки: 30 Ноября 2021 года
Содержание статьи
Причины мышечно-тонических болевых синдромов
Чрезмерные статические нагрузки и микротравмирование позвоночных структур влечет за собой рефлекторное напряжение мышц, ограничение их подвижности и формирование неоптимального двигательного стереотипа. Основной причиной мышечно-тонического синдрома являются дегенеративно-дистрофические заболевания позвоночника (остеохондроз, межпозвонковые грыжи) и нарушения осанки, связанные с врожденными аномалиями развития и деформацией спинного хребта.
Спровоцировать болезненный мышечный спазм может:
Под воздействием провоцирующих факторов в мышцах происходят биохимические процессы с выделением медиаторов воспаления, вызывающих рефлекторное сокращение мышц.
Симптомы мышечно-тонического синдрома
Основным признаком миотонического синдрома являются глубокие ноющие вертеброгенные боли. Болезненные спазмы, сопровождающиеся уплотнением и отечностью одной или нескольких мышц, существенно ограничивают подвижность. Из-за взаимодействия с нервными рецепторами развивается стойкая болезненность. Та, в свою очередь, усиливает сокращение мышц и замыкает порочный круг: спазм – отек – боль – спазм.
Мышечно-тонический синдром пояснично-крестцового отдела чаще всего становится следствием тяжелых физических нагрузок. Напряжение грушевидной мышцы может повлечь за собой боль в области ягодицы, тазобедренного сустава. В случае сдавливания седалищного нерва возможно онемение одной из конечностей.
Мышечно-тонический синдром шейного отдела проявляется цервикальными болями, болевыми ощущениями в шее, усиливающимися при разгибании и поворотах головы, гиперстезией 4-го и 5-го пальцев руки.
Для мышечно-тонического синдрома грудного отдела характерна болезненность между лопаток и по ходу ребер. Иногда может наблюдаться ощущение жжения и сдавленности в груди, имитирующих проявления сердечных проблем.
Классификация мышечно-тонических синдромов
Существует несколько разновидностей мышечно-тонических болевых синдромов. Они классифицируются в зависимости от локализации:
Помимо вышеперечисленных, патологическим изменениям нередко подвергается трапециевидная, широчайшая грудная, квадратная мышца поясницы, подниматель лопатки. Болевой синдром может быть первичным (охватывающим только спазмированные ткани) и вторичным, локализованным вне зоны повреждения.
Диагностика
Комплекс диагностических мероприятий включает:
Самым информативным, безопасным и безболезненным методом нейровизуализации признана магнитно-резонансная томография. Она дает максимально точную оценку состоянию позвоночника и спинного мозга, позволяет выявить протрузии и межпозвонковые грыжи, определить их размеры и локализацию.
Боковой (латеральный) амиотрофический склероз (и синдром БАС)
Боковой (латеральный) амиотрофический склероз (БАС) (также известен как болезнь моторных нейронов, Мотонейронная болезнь, болезнь Шарко, в англоязычных странах — болезнь Лу Герига) — прогрессирующее, неизлечимое дегенеративное заболевание центральной нервной системы, при котором происходит поражение как верхних (моторная кора головного мозга), так и нижних (передние рога спинного мозга и ядра черепно-мозговых нервов) двигательных нейронов, что приводит к параличам и последующей атрофии мышц.
Болезнь известна не так давно. Впервые описана Жан-Мартеном Шарко в 1869г. По статистике выявляется у 2-5 человек на 100 000 населения в год, что говорит о том, что данная патология относительно редко встречается. Всего в мире насчитывается около 70 тысяч больных боковым амиотрофическим склерозом. Обычно заболевание заявляет о себе у людей старше 50 лет.
Совсем недавно было высказано мнение, что случаи бокового амиотрофического склероза чаще регистрируются у высокоинтеллектуальных людей, профессионалов в своем деле, а также у спортсменов-атлетов, которые на протяжении всей жизни отличались крепким здоровьем.
Точная этиология БАС неизвестна.
Сущность болезни заключается в дегенерации двигательных нейронов, т.е. под воздействием ряда причин запускается процесс разрушения нервных клеток, ответственных за сокращения мышц. Этот процесс затрагивает нейроны коры больших полушарий, ядер головного мозга и нейроны передних рогов спинного мозга. Двигательные нейроны погибают, а их функции никто больше не выполняет. Нервные импульсы к мышечным клеткам больше не поступают. И мышцы слабеют, развиваются парезы и параличи, атрофия мышечной ткани.
Если в основе бокового амиотрофического склероза лежит мутация в гене супероксиддисмутазы-1, то процесс выглядит примерно следующим образом. Мутантная супероксиддисмутаза-1 накапливается в митохондриях двигательных нейронов (в энергетических станциях клетки). Это «мешает» нормальному внутриклеточному транспорту белковых образований. Белки соединятся друг с другом, как бы слипаются, и это запускает процесс дегенерации клетки.
Если причиной становится избыток глутамата, то механизм запуска разрушения двигательных нейронов выглядит так: глутамат открывает каналы в мембране нейронов для кальция. Кальций устремляется внутрь клеток. Избыток кальция, в свою очередь, активирует внутриклеточные ферменты. Ферменты как бы «переваривают» структуры нервных клеток, при этом образуется большое количество свободных радикалов. И эти свободные радикалы повреждают нейроны, постепенно приводя к их полному разрушению.
Предполагается, что роль других факторов в развитии БАС также заключается в запуске свободнорадикального окисления.
Классификация БАС, формы:
Общими симптомами, характерными для любой из форм бокового амиотрофического склероза, являются:
Начальные проявления заболевания:
•слабость в дистальных отделах рук, неловкость при выполнении тонких движений пальцами, похудание в кистях и фасцикуляции (мышечные подергивания)
•реже заболевание дебютирует слабостью в проксимальных отделах рук и плечевом поясе, атрофиями в мышцах ног в сочетании с нижним спастическим парапарезом
•возможно также начало заболевания с бульбарных расстройств – дизартрии и дисфагии (25% случаев)
•крампи (болезненные сокращения, спазмы мышц), нередко генерализованные, встречаются практически у всех больных БАС, и нередко являются первым признаком заболевания
Для БАС в большинстве случаев характерна асимметричность симптоматики.
При этой форме заболевания возможно два варианта:
Также может дебютировать двумя способами:
В руках по мере прогрессирования болезни формируется парез с атрофическими изменениями, повышением рефлексов, повышением тонуса и патологическими стопными признаками. Аналогичные изменения возникают и в ногах, но несколько позже.
Это разновидность бокового амиотрофического склероза, когда заболевание протекает с преимущественным поражением центрального мотонейрона. При этом во всех мышцах туловища и конечностей формируются парезы с повышением мышечного тонуса, патологическими симптомами.
Бульбарная и высокая формы БАС являются прогностически неблагоприятными. Больные с таким началом заболевания имеют меньшую продолжительность жизни по сравнению с шейно-грудной и пояснично-крестцовой формами. Какими бы ни были первые проявления заболевания, оно неуклонно прогрессируют.
Парезы в различных конечностях приводят к нарушению способности самостоятельно передвигаться, обслуживать себя. Вовлечение в процесс дыхательной мускулатуры приводит вначале к появлению одышки при физической нагрузке, затем одышка беспокоит уже в покое, появляются эпизоды острой нехватки воздуха. В терминальных стадиях самостоятельное дыхание просто невозможно, больным требуется постоянная искусственная вентиляция легких.
Продолжительность жизни больного БАС составляет по разным данным от 2 до 12 лет, однако более 90% больных умирают в течение 5 лет от момента постановки диагноза. В терминальную стадию болезни больные полностью прикованы к постели, дыхание поддерживается с помощью аппарата искусственной вентиляции легких. Причиной гибели таких больных может стать остановка дыхания, присоединение осложнений в виде пневмонии, тромбоэмболии, инфицирования пролежней с генерализацией инфекции.
Среди параклинических исследований наиболее существенное диагностическое значение имеет электромиография. Выявляется распространенное поражение клеток передних рогов (даже в клинически сохранных мышцах) с фибрилляциями, фасцикуляциями, позитивными волнами, изменениями потенциалов двигательных единиц (увеличивается их амплитуда и длительность) при нормальной скорости проведения возбуждения по волокнам чувствительных нервов. Содержание КФК в плазме может быть незначительно повышено
Боковой амиотрофический склероз нужно заподозрить:
•при развитии слабости и атрофий, а возможно и фасцикуляций (мышечных подергиваний) в мышцах кисти
•при похудания мышц тенара одной из кистей с развитием слабости аддукции (приведения) и оппозиции большого пальца (обычно асимметрично)
•при этом наблюдается затруднение при схватывании большим и указательным пальцами, затруднения при подбирании мелких предметов, при застегивании пуговиц, при письме
•при развитии слабости в проксимальных отделах рук и плечевом поясе, атрофий в мышцах ног в сочетании с нижним спастическим парапарезом
•при развитии у пациента дизартрии (нарушений речи) и дисфагии (нарушений глотания)
•при появлении у пациента крампи (болезненных мышечных сокращений)
Диагностические критерии БАС:
Критерии подтверждения БАС:
Диагноз БАС подьверждается:
Дифференциальный диагноз БАС (синдромы похожие на БАС):
•Спондилогенная шейная миелопатия.
•Опухоли краниовертебральной области и спинного мозга.
•Краниовертебральные аномалии.
•Сирингомиелия.
•Подострая комбинированная дегенерация спинного мозга при недостаточности витамина В12.
•Семейный спастический парапарез Штрюмпеля.
•Прогрессирующие спинальные амиотрофии.
•Постполиомиелитический синдром.
•Интоксикации свинцом, ртутью, марганцем.
•Недостаточность гексозаминидазы типа А у взрослых при ганглиозидозе GM2.
•Диабетическая амиотрофия.
•Мультифокальная моторная невропатия с блоками проведения.
•Болезнь Крейцтфельдта-Якоба.
•Паранеопластический синдром, в частности при лимфогранулематозе и злокачественной лимфоме.
•Синдром БАС при парапротеинемии.
•Аксональная нейропатия при болезни Лайма (Лайм-боррелиозе).
•Синдром Гийена-Барре.
•Миастения.
•Рассеянный склероз
•Эндокринопатии (тиреотоксикоз, гиперпаратиреоз, диабетическая амиотрофия).
•Доброкачественные фасцикуляции, т.е. фасцикуляции, продолжающиеся годами без признаков поражения двигательной системы.
•Нейроинфекции (полиомиелит, бруцеллез, эпидемический энцефалит, клещевой энцефалит, нейросифилис, болезнь Лайма).
•Первичный боковой склероз.
Диагностические исследования при синдроме БАС.
Для уточнения диагноза и проведения дифференциального диагноза при синдроме БАС рекомендутся следующее обследование больного:
Анализ крови (СОЭ, гематологические и биохимические исследования)
Рентгенография органов грудной клетки
Исследование функций щитовидной железы
Определение содержания витамина В12 и фолиевой кислоты в крови
Креатинкиназа в сыворотке
МРТ головного мозга и при необходимости, спинного мозга
Эффективного лечения заболевания не существует. Единственный препарат, ингибитор высвобождения глутамата рилузол (Рилутек), отодвигает летальный исход на 2 – 4 месяца. Его назначают по 50 мг два раза в день.
Основу лечения составляет симптоматическая терапия:
•Физическая активность. Пациент должен по мере своих возможностей поддерживать физическую активность По мере прогрессирования заболевания возникает необходимость в кресле-каталке и других специальных приспособлениях.
•Диета. Дисфагия создаёт опасность попадания пищи в дыхательные пути • Иногда возникает необходимость в питании через зонд или в гастростомии.
•Применение ортопедических приспособлений: шейного воротника, различных шин, устройств для захвата предметов.
•При крампи (болезненным мышечных спазмах): карбамазепин (Финлепсин, Тегретол) и/или витамин Е, а также препараты магния, верапамил (Изоптин).
•При спастичности: баклофен (Баклосан), Сирдалуд, а также клоназепам.
•При слюнотечении атропин, или гиосцин (Бускопан).
•При невозможности приема пищи вследствие нарушения глотания накладывают гастростому или вводят назогастральный зонд. Раннее проведение чрезкожной эндоскопической гастростомии продлевает жизнь пациентов в среднем на 6 месяцев.
•Церебролизин в высоких дозах (10-30 мл в/в капельно 10 дней повторными курсами). Существует ряд небольших исследований, показывающих нейропротективную эффективность церебролизина при БАС.
•Антидепрессанты: Серталин или Паксил или Амитриптилин (часть больных БАС предпочитает именно его как раз из-за побочных действий – он вызывает сухость во рту, соответственно уменьшает гиперсаливацию (слюнотечение), часто мучающую больных БАС).
•При появлении дыхательных нарушений: искусственная вентиляция легких в условиях стационаров, как правило, не проводится, но некоторые больные приобретают портативные приборы ИВЛ и проводят ИВЛ в домашних условиях.
•Ведутся разработки к применению гормона роста, нейротрофических факторов при БАС.
•Последнее время активно ведутся разработки лечения стволовыми клетками. Этот метод обещает быть перспективным, но все же пока находится на стадии научных экспериментов.
•Боковой амиотрофический склероз является фатальным заболеванием. Средняя продолжительность жизни больных БАС 3 – 5 лет, тем не менее, 30% больных живут 5 лет, а около 10 – 20% живут более 10 лет от начала заболевания.
•Неблагоприятные прогностические признаки – пожилой возраст и бульбарные нарушения (после появления последних больные живут не более 1 – 3 лет).