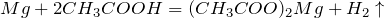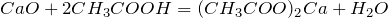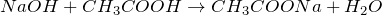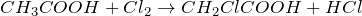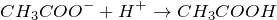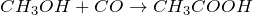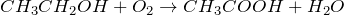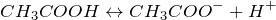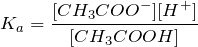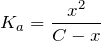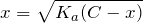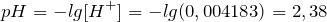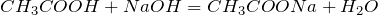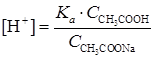Как выглядит формула уксусной кислоты
Уксусная кислота: химическая формула, свойства и применение
Этановая кислота больше известна как уксусная. Она представляет собой органическое соединение с формулой CH3COOH. Относится к классу карбоновых кислот, молекулы которых содержат функциональные одновалентные карбоксильные группы COOH (либо одну, либо несколько). О ней можно представить много информации, но сейчас вниманием стоит отметить лишь самые интересные факты.
Формула
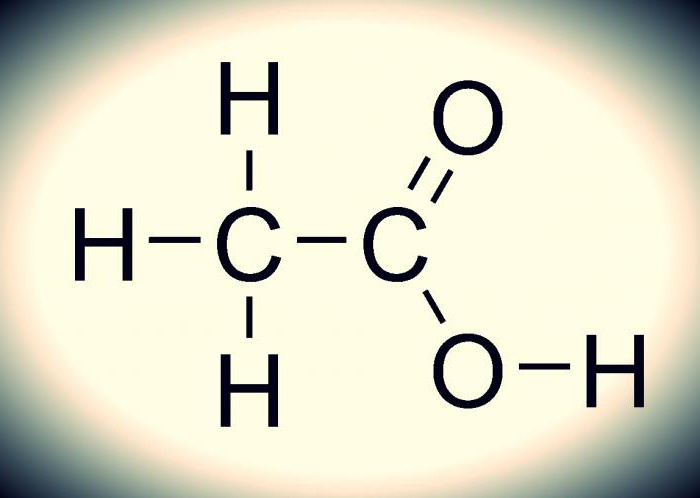
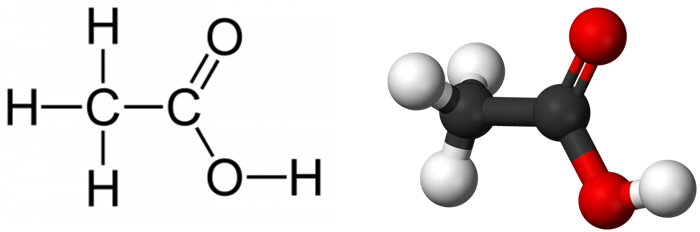
Как она выглядит, можно понять по приложенному ниже изображению. Химическая формула уксусной кислоты несложная. Это обуславливается многим: само соединение является одноосновным, да и относится оно к карбоксильной группе, для которой характерно легкое отщепление протонов (стабильная элементарная частица). Данное соединение – типичный представитель карбоновых кислот, поскольку оно обладает всеми их свойствами.
Качественный анализ
Он основан именно на диссоциации уксусной кислоты. Качественный анализ, также называемый реакцией, представляет собой совокупность физических и химических методов, которые применяются для обнаружения соединений, радикалов (независимые молекулы и атомы) и элементов (совокупности частиц), которые входят в состав анализируемого вещества.
С помощью данного способа удается обнаружить соли уксусной кислоты. Выглядит все не так сложно, как может казаться. В раствор добавляют сильную кислоту. серную, например. И если появляется запах уксусной кислоты, то ее соль в растворе присутствует. Как это работает? Остатки уксусной кислоты, которые образуются из соли, связываются в тот момент с катионами водорода от серной. Каков результат? Появление большего количества молекул уксусной кислоты. Диссоциация так и происходит.
Реакции
Следует отметить, что обсуждаемое соединение способно взаимодействовать с активными металлами. К таковым относится литий, натрий, калий, рубидий, франций, магний, цезий. Последний, кстати, является наиболее активным. Что происходит в момент таких реакций? Выделяется водород, и происходит образование пресловутых ацетатов. Вот как выглядит химическая формула уксусной кислоты, вступившей в реакцию с магнием: Mg + 2СН3СООН → (СН3СОО)2Mg + Н2↑.
Есть способы получения дихлоруксусной (CHCl2COOH) и трихлоруксусной (CCl3COOH) кислот. В них атомы водорода метильной группы замещены хлорными. Способа их получения всего два. Один заключается в гидролизе трихлорэтилена. И он менее распространен, чем другой, основанный на способности уксусной кислоты хлорироваться действием газообразного хлора. Данный метод проще и эффективней.
Вот как этот процесс выглядит в виде химической формулы уксусной кислоты, взаимодействующей с хлором: СН3СООН + Cl2 → СН2CLCOOH + HCL. Только стоит уточнить один момент: так получается просто хлоруксусная кислота, две вышеупомянутые образуются с участием красного фосфора в небольших количествах.
Другие превращения
Стоит отметить, что уксусная кислота (CH3COOH) способна вступать во все реакции, которые являются характерными для пресловутой карбоновой группы. Ее можно восстановить до этанола, одноатомного спирта. Для этого необходимо воздействовать на нее алюмогидридом лития – неорганическим соединением, которое является мощным восстановителем, часто применяемым в органическом синтезе. Его формула – Li(AlH4).
Кристаллизация
Ледяная уксусная кислота – нередко рассматриваемое соединение называют именно так. Дело в том, что она при охлаждении всего до 15-16 °C переходит в кристаллическое состояние, как будто бы замерзает. Визуально это действительно очень похоже на лед. При наличии нескольких ингредиентов можно провести эксперимент, результатом которого станет превращение уксусной кислоты в ледяную. Все просто. Из воды и льда нужно приготовить охлаждающую смесь, а потом опустить в нее подготовленную заранее пробирку с уксусной кислотой. Через несколько минут она кристаллизуется. Кроме соединения, для этого нужен химический стакан, штатив, термометр и пробирка.
Вред вещества
Последствия
Логично, что чем выше концентрация уксусной кислоты, тем больший вред она окажет в случае попадания ее на кожу или внутрь организма. К общим симптомам отравления относят:
Степени тяжести
Принято выделять три:
Отравление парами уксусной кислоты тоже возможно. Оно сопровождается сильным насморком, кашлем и слезотечением.
Оказание помощи
Если человек отравился уксусной кислотой, то очень важно быстро действовать для минимизирования последствий от случившегося. Рассмотрим, что надо делать:
Важно оказать первую помощь в течение двух часов после случившегося. По истечении данного срока слизистые оболочки сильно отекают, и уже уменьшить боль человека будет сложно. И да, ни в коем случае нельзя использовать соду. Сочетание кислоты и щелочи даст реакцию, в ходе которой выработается углекислый газ и вода. А такое образование внутри желудка может привести к летальному исходу.
Применение
Водные растворы этановой кислоты широко используются в пищевой промышленности. Это уксусы. Для их получения кислоту разводят водой, чтобы получился 3-15-процентный раствор. Как добавка они обозначаются маркировкой Е260. Уксусы входят в состав различных соусов, а еще их используют для консервирования продуктов, маринования мяса и рыбы. В быту они широко применимы для удаления накипи, пятен с одежды и посуды. Уксус – прекрасный дезинфектор. Им можно обработать любую поверхность. Иногда его добавляют при стирке, чтобы смягчить одежду.
Также уксус применим в получении душистых веществ, лекарственных средств, растворителей, в производстве ацетона и ацетилцеллюлозы, например. Да, и в крашении и книгопечатании уксусная кислота принимает непосредственное участие.
Кроме всего, ее используют как реакционную среду для проведения окисления самых разных органических веществ. Примером из промышленности можно считать окисление параксилола (углеводород ароматического ряда) кислородом воздуха в терефталевую ароматическую кислоту. Кстати, так как пары этого вещества имеют резкий раздражающий запах, его можно использовать как замену нашатырного спирта для выведения человека из обморочного состояния.
Синтетическая уксусная кислота
Это легковоспламеняющаяся жидкость, которая относится к веществам третьего класса опасности. Она используется в промышленности. При работе с ней применяются индивидуальные средства защиты. Хранят это вещество в особых условиях и только в определенной таре. Как правило, это:
Если жидкость хранят в полимерной таре, то это как максимум месяц. Также категорически не допускается совместное хранение данного вещества с такими сильными окислителями, как перманганат калия, серная и азотная кислоты.
Состав уксуса
О нем тоже стоит сказать пару слов. В состав традиционного, всем привычного уксуса входят следующие кислоты:
И конечно же, этановое соединение в состав уксуса тоже входит – это основа данного продукта.
Как разбавить?
Это часто задаваемый вопрос. Все видели в продаже уксусную кислоту 70 %. Ее покупают, чтобы готовить смеси для народного лечения, или для использования в качестве приправы, маринада, добавки в соус или закатку. Но нельзя применять такой мощный концентрат. Поэтому появляется вопрос о том, как развести до уксуса уксусную кислоту. Для начала нужно себя обезопасить – надеть перчатки. Затем следует подготовить чистую воду. Для растворов различных концентраций понадобится определенное количество жидкости. Какое? Что ж, смотрим на приведенную ниже таблицу и разводим уксусную кислоту с учетом данных.
Начальная концентрация уксуса 70 %
1:1,5 (соотношение – одна часть уксуса на энную часть воды)
Химические свойства уксусной кислоты

Всего получено оценок: 537.
Всего получено оценок: 537.
Этановая или уксусная кислота – это слабая карбоновая кислота, которая широко применяется в промышленности. Химические свойства уксусной кислоты определяет карбоксильная группа COOH.
Физические свойства
Уксусная кислота (CH3COOH) – это концентрированный уксус, знакомый человечеству с давних времён. Его изготовляли путём брожения вина, т.е. углеводов и спиртов.
По физическим свойствам уксусная кислота – бесцветная жидкость с кислым вкусом и резким запахом. Попадание жидкости на слизистые оболочки вызывает химический ожог. Уксусная кислота обладает гигроскопичностью, т.е. способна поглощать водяные пары. Хорошо растворима в воде.
Основные физические свойства уксуса:
В уксусе растворяются неорганические вещества и газы, например, бескислородные кислоты – HF, HCl, HBr.
Получение
Способы получения уксусной кислоты:
Уравнение брожения выглядит следующим образом – СН3СН2ОН + О2 → СН3СООН + Н2О. В качестве сырья используется сок или вино, кислород и ферменты бактерий или дрожжей.
Химические свойства
Уксусная кислота проявляет слабые кислотные свойства. Основные реакции уксусной кислоты с различными веществами описаны в таблице.
Формула уксусной кислоты
Химическая и структурная формулы уксусной кислоты
Химическая формула: CH3COOH
Молярная масса: 60,05 г/моль.
Уксусная кислота – предельная одноосновная карбоновая кислота. Образует соли – ацетаты.
Физические свойства уксусной кислоты
Уксусная кислота — бесцветная жидкость с резким характерным запахом, кислым вкусом. Гигроскопична, неограниченно растворяется в воде. Существует в виде димеров. Безводная уксусная кислота называется ледяной, поскольку при замерзании образует льдовидную массу.
Химические свойства уксусной кислоты
Уксусная кислота проявляет все основные свойствами карбоновых кислот.
Качественной реакцией на соли уксусной кислоты является взаимодействие с сильными кислотами. Уксусная кислота слабая и вытесняется сильными кислотами из растворов солей, при этом появляется ее характерный запах:
Получение. Наиболее экономически выгодный промышленный способ получения уксусной кислоты – карбонилирование метанола моноксидом углерода, катализатор – соли родия, промотор – иодид-ионы:
Биохимический способ – окисление этанола:
Водные растворы уксусной кислоты используются в пищевой промышленности (пищевая добавка E260), бытовой кулинарии, и консервировании. Уксусную кислоту применяют для получения лекарственных и душистых веществ, в качестве растворителя.
Концентрированная уксусная кислота (с концентрацией более 30%) способна вызывать химические ожоги. Пары уксусной кислоты раздражают слизистые оболочки верхних дыхательных путей
Примеры решения задач
Константа диссоциации кислоты:
Обозначим за х концентрацию ионов водорода х = [H + ], тогда выражение для константы диссоциации примет вид:
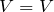
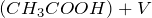
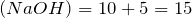
При сливании растворов протекает реакция:
Рассчитаем количества вещества уксусной кислоты и гидроксида натрия:
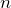
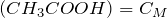
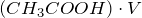
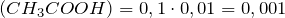
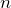
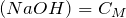
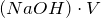
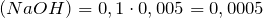
По уравнению реакции n(CH3COOH) = n(NaOH), а в нашем случае n(CH3COOH) > n(NaOH), следовательно, уксусная кислота взята в избытке. После протекания реакции в растворе будут находиться уксусная кислота и ацетат натрия, т.е. мы получили буферную систему.
Рассчитаем концентрацию ацетата натрия в полученном растворе:
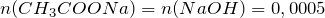
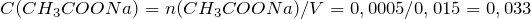
Концентрация уксусной кислоты в растворе будет равна:
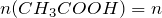
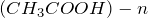
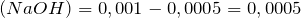
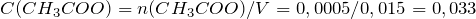
Концентрация ионов водорода в буферном растворе рассчитывается по формуле:
где Ka – константа диссоциации уксусной кислоты.
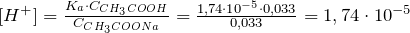
Уксусная кислота

Что такое уксусная кислота
Уксусная кислота – это органический продукт со специфическим запахом и вкусом, представляет собой результат брожения спиртовых и углеводных компонентов либо скисания вин.
Это вещество в форме винного уксуса было известно еще в Древней Греции и Древнем Риме. В более поздние времена алхимики научились производить более чистую субстанцию в результате перегонки. Кислота в виде кристаллов была выведена в 1700 году. Приблизительно в это же время химики определили ее формулу и выявили способность вещества к воспламенению.
В природе уксусная кислота редко встречается в свободном виде. В составе растений она представлена в форме солей или эфиров, в теле животных найдена в составе мышечной ткани, селезенки, а также в моче, поте, экскрементах. Легко образуется вследствие брожения, гниения, в процессе распада сложных органических соединений.
Синтетическую форму уксусной кислоты получают после реакции воздействия углекислотой на натрий-метил либо же при воздействии на метилат натрия, нагретый до 160 градусов, окисью углерода. Есть и другие способы создания этой субстанции в лаборатории.
Чистая уксусная кислота – это прозрачная жидкость с удушливым запахом, вызывающая ожоги на теле и слизистых даже при контакте с ними паров. Если зажечь пары вещества, они дадут светло-голубое пламя. Растворяясь в воде, кислота выделяет тепло.
Ацетилкофермент А образовывается при участии уксусной кислоты, которая также необходима для биосинтеза стеринов, жирных кислот, стероидов и других веществ. Химические свойства уксусной кислоты делают ее незаменимой во многих процессах и реакциях. Соединение помогает образовывать соли, амиды, сложные эфиры.
Но помимо полезных свойств, вещество является опасным, легковоспламеняющимся. Поэтому работая с ним, необходимо максимально соблюдать технику безопасности, избегая прямого контакта с кожей, не дышать кислотными парами.
Формы уксусной кислоты:
Виды уксуса
Уксусная кислота в чистом виде – вещество агрессивное, способное нанести вред здоровью.
Поэтому в быту используется ее водный раствор разной концентрации. Существуют два способа создания уксуса:
Продукт промышленного производства может содержать в себе 3, 6 или 9 % уксусной кислоты. Концентрация домашнего уксуса еще ниже, что делает его безопаснее для применения. Также продукт домашнего производства содержит в себе витамины и другие полезные вещества. Спектр нутриентов зависит от продукта, из которого был изготовлен уксус. Наиболее часто применяют яблочное и виноградное сырье. Существует еще так называемый бальзамический уксус, сделанный из виноградного с добавлением пряных трав.
Суточная норма
Говорить о суточной норме потребления уксусной кислоты не приходится. Несмотря на высокую популярность уксуса в быту, широкое применение в кулинарии, ученые так и не рассчитали, сколько этого вещества можно или нужно потреблять человеку. Правда, и современная медицина не знает случаев, когда бы у кого-либо возникли проблемы со здоровьем из-за недостаточного употребления этого продукта.

Помимо этой очевидной причины для отказа от уксуса, существует еще одна. У некоторых людей встречается индивидуальная непереносимость вещества. Во избежание неприятных последствий, таким лицам также не следует потреблять пищу, приправленную уксусом.
Передозировка
Воздействие уксусной кислоты на человеческий организм схоже с влиянием соляной, серной или азотной кислот. Отличие – в более поверхностном воздействии веществ.
Примерно 12 мл чистой уксусной кислоты является смертельной для человека. Эта порция аналогична стакану столового уксуса или 20-40 мл уксусной эссенции. Пары вещества, попадая в легкие, вызывают пневмонию с осложнениями. Среди других возможных последствий передозировки – некроз тканей, геморрагия печени, нефроз с отмиранием почечных клеток.
Взаимодействие с другими веществами
Уксусная кислота быстро вступает в реакцию с протеинами. В комбинации с уксусом белки из пищи легче усваиваются организмом. Аналогично кислый водный раствор воздействует на углеводы, делая их более легкими для переваривания. Эта биохимическая способность делает продукт «правильным» соседом для мясной, рыбной или овощной пищи. Это правило работает только при условии здоровой пищеварительной системы.
Уксус в народной медицине
Альтернативная медицина применяет уксусную кислоту, а точнее ее водный раствор, в качестве лекарства от многих болезней.
Пожалуй, наиболее известный и потребляемый прием – снижение высокой температуры с помощью уксусных компрессов. Однако стоит учитывать, что при таком использовании вещество всасывается в кровь через кожу, что может стать причиной отравления у маленьких детей.
Не менее известное применение этой жидкости при укусах комаров, пчел и других насекомых. С помощью водного раствора кислоты народные целители лечат ангины, фарингиты, артрит, ревматизм, а также грибок стоп и молочницу. Для уменьшения симптомов простуды в комнате, где лежит больной, распыляют уксус. А если участок кожи, обгоревший под солнцем или обожженный медузой, смазать кислым раствором, получится уменьшить неприятные симптомы.

Также он важен для снижения холестерина, стабилизации сахара в крови (у диабетиков), избавления от лишнего веса (за счет ускорения метаболизма). Камни в почках альтернативная медицина также выводит уксусной кислотой из яблок.
Всегда стоит учитывать возможный вред в виде развития гастрита, язвы, отравления.
Кислота для красоты
В косметологии уксусная кислота используется широко. Об эффективности этого вещества в борьбе с целлюлитом и лишними сантиметрами рассказывают весьма вдохновляющие истории. Курс обертываний с использованием уксуса – и можно забыть об «апельсиновой корке». Так, по крайней мере, гласят отзывы на форумах худеющих женщин.
Также известно применение уксусной кислоты для лечения перхоти и прыщей. Результат достигается благодаря антибактериальным способностям вещества. Вернуть волосам блеск и силу также по силам уксусу. Достаточно после каждого мытья ополаскивать чистые кудри легким кислотным раствором. А защитить от облысения поможет уксус с корнем аира и листьями крапивы.
Использование в промышленности
Уксусная кислота – компонент с широким спектром применения. В частности, в фармацевтически токсичной для человека.
Также это вещество – важный компонент в парфюмерии. Ее добавляют в косметические средства в качестве консерванта.
Соли уксусной кислоты используются в качестве протрав и как средство против сорняков.
Пищевые источники
Первым и наиболее концентрированным источником кислоты являются разного вида уксусы: яблочный, винный, столовый и другие.
Также это вещество содержится в меде, винограде, яблоках, финиках, инжире, свекле, арбузе, бананах, солоде, пшенице и других продуктах.
Уксусная кислота – субстанция весьма противоречивая. При правильном использовании она может послужить на пользу человеку. Но если не соблюдать технику безопасности, то последствия могут быть плачевными.
Больше свежей и актуальной информации о здоровье на нашем канале в Telegram. Подписывайтесь: https://t.me/foodandhealthru