Как вылечить клебсиеллу в кишечнике
Клебсиелла
Темой нынешнего разговора будет, с точки зрения автора, королева внутрибольничных инфекций любого стационара — Klebsiella pneumonia (или палочка Фридлендера).
Автор: Трубачева Е.С., врач – клинический фармаколог
Темой нынешнего разговора будет, с точки зрения автора, королева внутрибольничных инфекций любого стационара — Klebsiella pneumoniae (или палочка Фридлендера). Да-да, автор не ошибся, именно она, а не синегнойки или ацинетки, а именно ее величество — клебсиелла, практически абсолютная убийца тяжелых и крайне тяжелых пациентов. Почему это именно так, мы сегодня и поговорим.
Микробиологические аспекты
Первое и главное, о чем надо знать, — Klebsiella pneumonia — это представитель нормальной микрофлоры кишечника. Еще раз и большими буквами — НОРМАЛЬНОЙ! Не надо ее там лечить (как и стафилококк в носоглотке) — она там живет, и это ее естественный ареал обитания.
А все остальные локации, где она может быть обнаружена: нижние дыхательные пути, мочевыводящий тракт, секрет простаты или содержимое полости матки (анальный сексуальный акт без презерватива — зло, имейте это в виду при сборе анамнеза, особенно у женщин с послеродовым эндометритом, автор такого навидался в достатке… мужчин это тоже касается, и обнаружение подобной зверюшки в секрете простаты должно навести на определенные мысли и вопросы, и пока пациент не закончит данную практику, простатит вы ему при всем желании не вылечите), кровь и в раны при раневых инфекциях после хирургического вмешательства на брюшной полости — могут указывать на возбудителя текущего состояния.
Что вызывает:
Общим у всех этих патологий является одно — они все тем или иным образом связаны с вмешательством, и чаще всего (опуская уже упомянутые анальные сексуальные акты) это вмешательство носит ятрогенный характер. Клебсиелла не умеет ни летать, ни ходить, ни даже ползать, в очаг ее приносят либо неправильно вымытые руки, либо плохо обработанное медицинское оборудование.
Эпидемиологические аспекты
Как мы уже обсуждали в статье о синегнойной палочке, при некотором желании и упертости эпидемиологической службы или клинического фармаколога (или команды из оных, так как каждый знает свое звено), извести неферментеров из стационара — не самая сложная задача. Было бы желание у администрации этим заняться. Что касается лечащих врачей и среднего персонала, то это тот случай, когда достаточно обработать перчатки и далее, на уровне ЦСО и утилизации отходов, правильно избавиться от контаминированого материала, и если инструментарий не одноразовый, то очистить и простерилизовать его. То есть даже на уровне обработанных (или стерильных) перчаток, касающихся только одной области пациента (другая область, если необходимо, требует смены перчаток, либо обработки рук с полным выдерживанием экспозиции, а не чуть-чуть антисептиком помазал-растер-побежал), вы уже снижаете риск контаминации оным зверьем с последующим развитием синегнойной инфекции. Про ацинетобактер будет отдельная глава в разделе «неферментеры».
С клебсиеллой все намного сложнее. Эта, не побоюсь громкого слова, зверища, живет в кишечниках всего персонала медицинских учреждений. И в первую очередь, как понятно из ее названия, поражает нижние дыхательные пути. А если персонал работает с антибиотиками, то клебсиелла еще и устойчивая ко всему арсеналу применяемых препаратов (это к вопросу о разумном ограничении доступа к препаратам резерва). Так как сама клебсиелла не имеет ножек и крылышек, то попадает в оные пути она двумя способами: или в случае аспирации, или на руках персонала и с оборудования. Иного не дано. При аспирации это будет личная дикая зверюшка пациента, в случае грязных шаловливых ручек или оборудования (например, эндоскопов) — клебсиелла, высеваемая в отделении в процессе микробиологического мониторинга. А если этот мониторинг углубленный, то напрямую покажет, какая именно хрюшка, выйдя из туалетной комнаты, не соизволила помыть руки, понадеявшись на перчатки. И нет, перчатки, даже стерильные в данном случае, не спасают, они не презерватив. Руки надо мыть и обрабатывать правильно, обязательно соблюдая технологию и экспозицию.
Как вы понимаете, истребить медицинский персонал мы не можем, поэтому и полностью очистить стационар от данной проблемы не получится. И она обязательно выскочит, стоит на секунду расслабиться, и выскочит на самом тяжелом больном, где еще умудрится смутировать в такого урода, которого не достанешь никаким антибиотиком.
На общемировом клебсиеллу тоже очень сильно боятся, и когда в 2010 году вдруг в Великобритании обнаружили штамм NDM (он устойчив вообще ко всему набору существующих антибиотиков и обозван абсолютным убийцей), паника была знатной. В результате проведенного эпидемиологического расследования, по итогам которого большая группа видных ученых стала персонами non-grata в Индии, было установлено, что данный штамм привезен оттуда и из Пакистана. Присутствие в сточных водах возбудителей, имеющих карбапенемазы (то есть это уже не внутрибольничная флора, это то, что там живет на улице) на момент проведения расследования составляла 90% по CTX-M15 и 36% по NDM. С чем связан сей факт? С безрецептурным масштабным использованием карбапенемов и… проблемами с проточной канализацией. Ее либо нет, либо ей не пользуются, а делают все по старинке. А так как земной шар оказался очень маленьким, теперь NDM-штаммы обнаруживаются по всей планете. У нас, например, очень быстро данным штаммом заселились клиники Санкт-Петербурга. И медицина перед ними бессильна. До тех пор, пока не налажен эпиднадзор, а персонал не моет руки после каждого посещения туалета.
Так как любого врага надо знать в лицо, то наиболее часто встречаемые портреты у автора тоже есть.
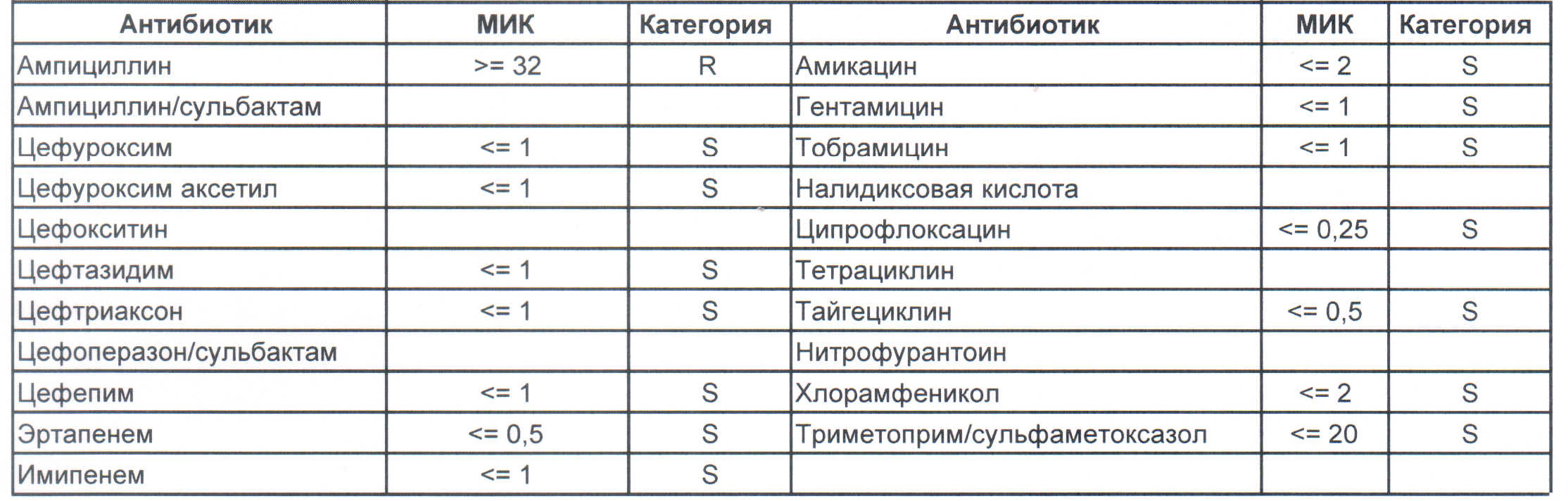
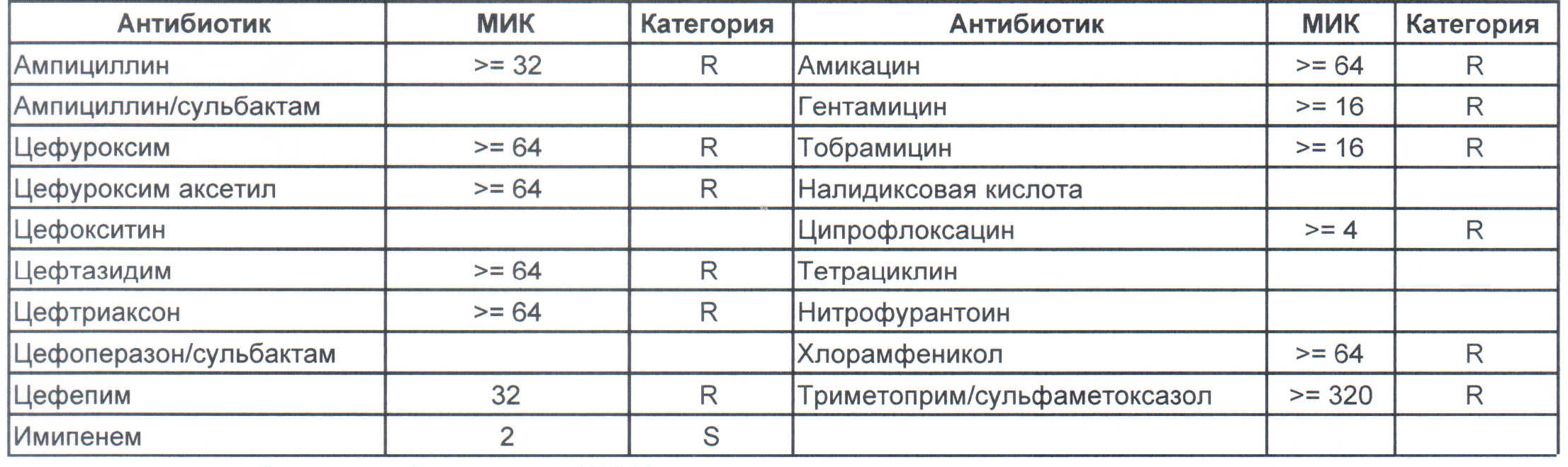
Итак, дикая и ничем ни разу не пуганная клебсиелла выглядит вот так:
Где встречается? Те самые послеродовые эндометриты, как результат плотских утех, простатиты, а также раневые инфекции после оперативных вмешательств на брюшной полости у ранее не леченных пациентов.
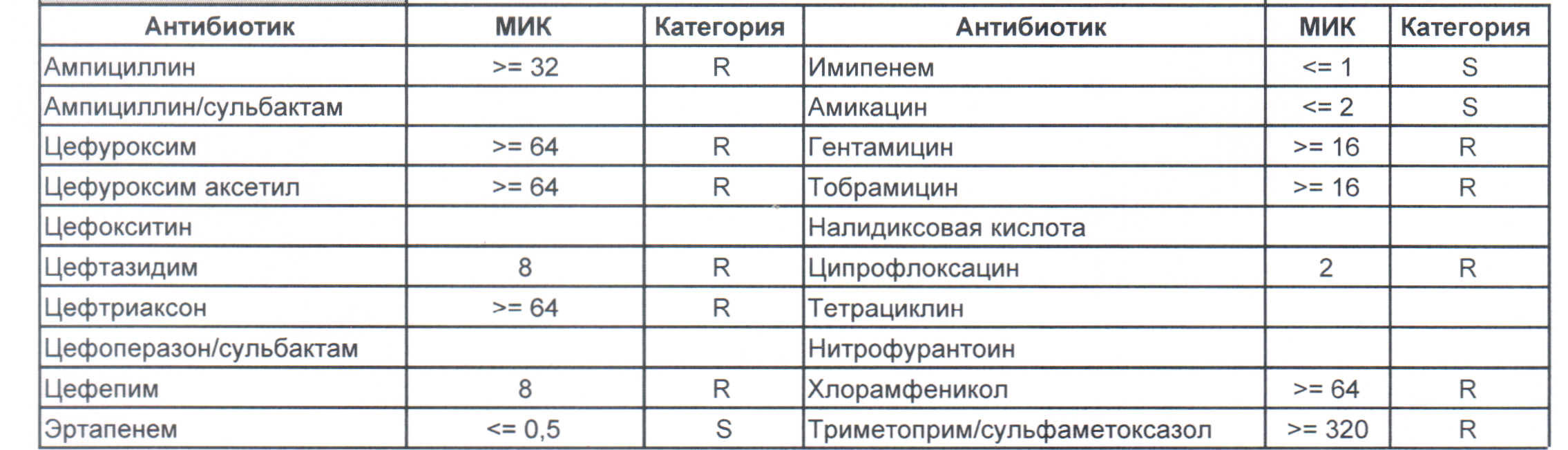
— вы можете увидеть устойчивый внутрибольничный штамм, который еще можно чем-то полечить, но это будет тяжело и дорого, проще персонал научить руки мыть и бороды брить (фекальной микрофлоры в мужских бородах в таком достатке, что единственный вариант для тех, кто хоть как-то соприкасается с ранами, данное украшение не носить или не оперировать).
На следующей картинке:
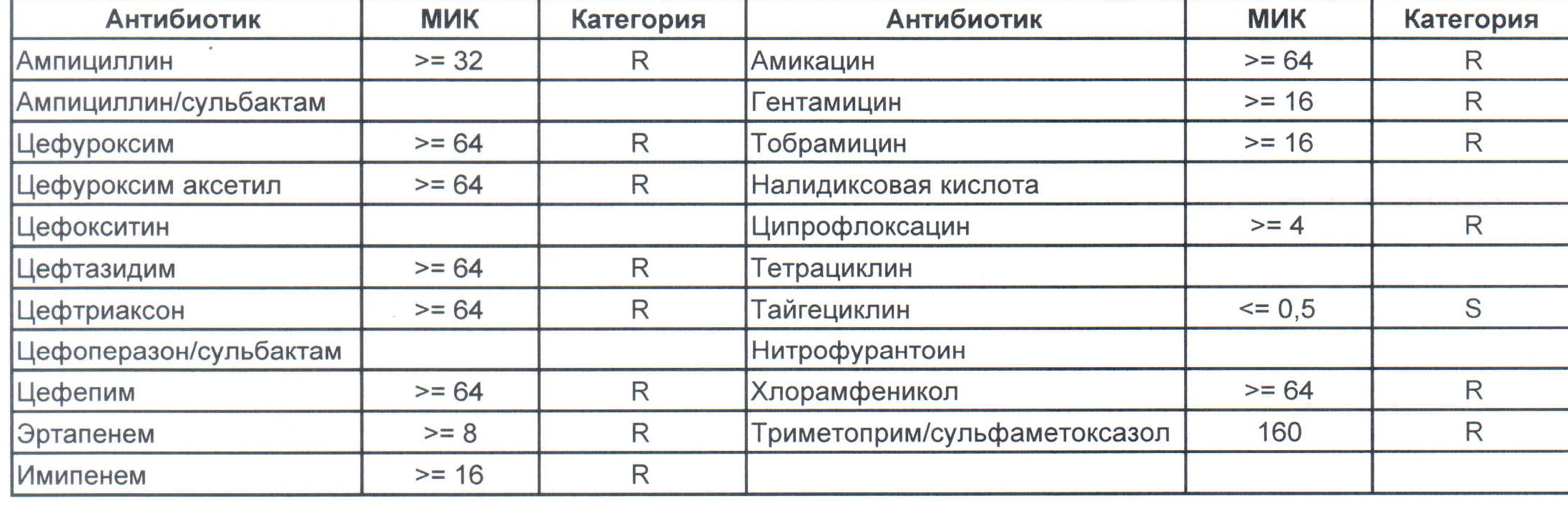
— мы видим практически неубиваемого зверя, который сам по себе вбивает тот самый последний гвоздь в гроб пациента. Но как же Тигециклин, спросите вы. Отвечу — тигацил является бактериостатиком, и пока он наберет необходимую силу, пациента уже отнесут и закопают. Но даже это еще не предел. Предел на следующем рисунке, и нет, Имипенем при указанной MIC уже бессилен:
Как вы понимаете — эти два зверя являются абсолютными убийцами, против которых в данный момент медицина бессильна полностью. И именно такое зверье живет в стационарах без микробиологического мониторинга и систем противостояния в виде эпидемического надзора. Именно эти звери убивают самых тяжелых пациентов, если каким-то образом (руки персонала или плохо обработанное оборудование) в них попали. Но что хуже всего, эти штаммы способны передавать свои факторы устойчивости другой грамотрицательной флоре, например, кишечным палочкам, а потому пациенты, инфицированные такими клебсиеллами, должны быть полностью изолированы и карантинизированы. Спасти их, скорее всего, не получится, но хотя бы всех остальных оградите от инфицирования и последующего летального исхода, да и сами такую зверюшку не подцепите (как вы помните «врач — это диагноз», так не будем его себе усложнять).
Чем лечить?
Дикая клебсиелла отлично лечится препаратами группы цефалоспоринов третьего ряда.
А вот внутрибольничную можно побороть, только четко понимая, с чем вы имеете дело, и обычный диско-дифузионный метод диагностики тут не поможет. Нужны автоматизированные системы с определением MIC. Но во главе угла все равно стоит инфекционная безопасность пациентов. Коллеги! Автор понимает, что выглядит «городской сумасшедшей», коим в свое время был объявлен Земмельвейс, но он вас умоляет — мойте руки после посещения туалета и мойте их правильно. Вам это ничего не стоит, а пациенты выживут. Ничего более эффективного против внутрибольничных клебсиелл пока не придумано. А эпидемиологи ваших учреждений будут проводить свои работы по контролю и дезинфекции отделений и целых зданий. Так получилось, что именно эту королеву ВБИ мы, врачи, медсестры и младший персонал, носим исключительно в себе. Берегите себя, своих близких и своих пациентов, тем более в это нелегкое для отечественной медицины время, с угрозой введения врачебных статей в УК. Клебсиелла — это почти всегда чистая ятрогения. Повторюсь — берегите себя и мойте руки.
Клебсиелла у детей
Клебсиеллезная инфекция известна также как клебсиеллез или клебсиелла (по названию возбудителя) — группа инфекционных болезней, которые вызываются условно-патогенными микроорганизмами, широко распространенными у новорожденных и детей раннего возраста.
Клебсиеллы часто вызывают внутрибольничные вспышки. У детей болезнь в основном возбуждает К. pneumoniae. К ней очень чувствительны новорожденные и младенцы. Способствуют развитию заболевания гипотрофия и врожденные пороки сердца, недоношенность, ОРВИ, иммунодефицитные состояния. Клебсиеллы вызывают групповую и спорадическую заболеваемость, приблизительно равную во всех сезонах.
Что провоцирует / Причины Клебсиеллы у детей:
Клебсиеллы являются грамотрицательными неподвижными капсульными палочками. Их размер 0,3—1,5×0,6—6 мкм. Располагаются по одиночке, парами или группируясь короткими цепочками. На питательных средах при температуре 35—37 ˚С наблюдается рост клебсиелл, которые формируют слизистые блестящие колонии, похожие на купола.
Обработка бактерицидным мылом зачастую не убивает возбудителя клебсиеллезной инфекции. То же касается и дезинфицирующих средств.
Болезнь у человека возбуждают три вида клебсиелл: К. pneumoniae, К. rhino-scleromatis и К. ozaenae.
Патогенез (что происходит?) во время Клебсиеллы у детей:
Некоторые штаммы К. pneumoniae производят довольно сильный энтеротоксин, который вызывает в разных органах и системах тяжелые морфологические изменения. Данный энтеротоксин приводит к диссеминированному внутрисосудистому свертыванию.
В то же время в области первичных очагов быстро образуются иммунные комплексы, которые оказывают на ткани патогенное влияние. Энтеротоксин приводит к гемодинамическим нарушениям в очагах поражения: в бронхиальной ткани, в стенке кишечника. В легких под влиянием энтеротоксина происходит разложение сурфактанта и образование ателектазов.
Симптомы Клебсиеллы у детей:
Клебсиелла у детей бывает таких видов:
Это деление по локализации патологического процесса.
Клебсиеллезная пневмония известна также как пневмония Фридлендера. По симптоматике они похожа на пневмонии другой бактериальной природы – на пневмококковую, например. Болезнь имеет острое начало, температура тела достигает примерно 39 °С, но может быть и выше. Ребенка знобит, появляется кашель (упорный, с отделением кровянисто-слизистой вязкой мокроты).
Аускультация показывает ослабление дыхания над воспалительными очагами и влажные хрипы. С помощью рентгена выявляют мелкоочаговые, крупноочаговые, захватывающие несколько сегментов, а также долевые пневмонии. Течение болезни в основном тяжелое. Клебсиеллезная пневмония в большинстве случаев сочетается с другими инфекциями – например, респираторно-вирусными.
При клебсиеллезной пневмонии патологический процесс переходит на альвеолы, наблюдается экссудация с геморрагическим компонентом. Пневмония имеет склонность к абсцедированию; есть случаи, при которых развивается гангрена легкого.
Клебсиеллезная кишечная инфекция по симптоматике и течению сходна с гастроэнтероколитом, энтероколитом, гастроэнтеритом и энтеритом. Начало заболевания характеризуется повышением температуры до уровня 37—39 °С, рвотой или повторными срыгиваниями (у младенцев), жидким стулом. Стул имеет обильный, водянистый характер, оттенок желто-зеленый, в испражнениях наблюдаются непереваренные частицы пищи. У 10—12% больных детей в испражнениях бывает кровяная примесь.
От детей могут поступать жалобы на боли в животе, которые имеют приступообразный характер. У младенцев и дошкольников родители наблюдают приступы беспокойства, которые усиливаются при пальпации живота.
На протяжении 2-12 дней держится высокая температура (в среднем от 3 жо 5 суток). В первые 2-3 суток болезни у ребенка случается рвота 2-8 раз на протяжении дня и ночи. Далее рвота либо прекращается либо случается довольно редко. От 3 до 10 суток длится диарея. Частота стула зависит от каждого конкретного случая. Иногда стул случается около 20 раз.
Тяжелые формы заболевания происходят с развитием токсикоза с эксикозом на протяжении 3-6 дней. У половины заболевших детей наблюдается выраженность обезвоживания II степени. Рвота почти во всех случаях повторяется, случается от 3 до 7 раз за день и ночь.
Фиксируют такие симптомы:
Изменений паренхиматозных органов нет, нейротоксикоза нет. В периферической крови – умеренный лейкоцитоз, в половине случаев бывает нейтрофилез и в трети случаев фиксируют повышенную СОЭ (до 15—20 мм/ч). Кишечная инфекция вызывается множеством штаммов клебсиелл.
Особенности заболевания у новорожденных и детей 1-го года жизни. Болезнь, как правило, проявляется у детей недоношенных с явлениями пренатальной дистрофии и энцефалопатии. Инфекция может поражать разные органы и системы, но превалируют кишечная инфекция и пневмония.
Кишечная инфекция у грудничков имеет острое начало, бурно развивается кишечный синдром, гемодинамические и метоболические нарушения. Дети отказываются сосать грудь, родители замечают их вялость и срыгивания. Стул у младенцев в данном случае происходит от 8 до 20 раз в сутки. Испражнения жидкой консистенции, водянистые, желто-зеленого оттенка, есть примесь мутной слизи. У некоторых заболевших малышей кишечные расстройства проявляются недолгосрочным учащением и разжижением стула.
Большинство новорожденных, заболевших клебсиеллезом, находятся в тяжелом состоянии. За первые несколько суток болезни они теряют значительный процент массы тела (100-500 г) из-за токсикоза с дегидратацией. Кожа приобретает серовато-бледный оттенок, возникает выраженный периоральный и периорбитальный цианоз, а также адинамия, гипорефлексия, заторможенность.
Энтероколит может быть некротизирующим, из-за этого в стуле появляется кровь и возникают осложнения – перфорация кишечника. Из-за присоединения пневмонии случается дыхательная недостаточность. Когда кишечная инфекция сочетается с пневмонией, на первый план среди симптомов выходит нейротоксикоз. У детей проявляются такие симптомы клебсиеллеза:
Могут случаться такие осложнения:
В периферической крови у новорожденных и грудничков наблюдаются лейкоцитоз и гиперлейкоцитоз (35 х 10 9 /л) с появлением миелоцитов до 3—7%, а также умеренная анемия.
У новорожденных клебсиеллы могут размножаться в первую очередь на коже головы в месте прикрепления электродов для мониторного наблюдения, на участках повреждения акушерскими щипцами и в области гематомы. Развивается инфильтративно-некротический процесс вплоть до развития флегмоны и абсцессов.
Клебсиеллезный сепсис часто поражает костную и суставную ткани. Симптоматически это проявляется как припухлость припухлостью в области воспаления ткани или сустава, ограниченное движение пораженной конечности, резкое беспокойство малыша при пеленании. Температура тела в норме. Обычно патологический процесс локализуется в области бедренной, плечевой и болыпеберцовой костей.
Диагностика Клебсиеллы у детей:
Для постановки диагноза необходимо обнаружение возбудителя или обнаружение нарастания титра антител к аутоштамму. Используют бактериологические методы исследования испражнений, рвотных масс, крови, мокроты, отделяемого из воспалительных очагов на коже и видимых слизистых оболочках, мочи. Диагностическое значение имеют выделение клебсиелл от больного в количестве 10 6 микробных тел и более в 1 г фекалий и снижение количества бактерий по мере выздоровления ребенка. Вспомогательную роль играет нарастание титров антител каутоштамму клебсиеллы в процессе болезни. Титры противоклебсиеллезных агглютининов колеблются от 1:20 до 1:80 или от 1:8 до 1:64.
Лечение Клебсиеллы у детей:
Для лечения необходима правильная диета и своевременная оральная регидратация. Для лечения среднетяжелых и тяжелых форм болезни необходимы антибактериальные препараты. Врачи назначают обычно гентамицин (антибиотик группы аминогликозидов широкого спектра действия), нитрофурановые препараты, 5-НОК (препарат группы оксихинолинов).
Профилактика Клебсиеллы у детей:
Для предотвращения заражения клебсиеллами нужно строго соблюдать противоэпидемичесий режим в родильных домах, в соматических и хирургических стационарах, в отделениях для новорожденных. Активную профилактику проводят с помощью клебсиеллезной бесклеточной вакцины, оказывающей протективное действие в отношении различных сероваров К. pneumoniae.
К каким докторам следует обращаться если у Вас Клебсиелла у детей:
Klebsiella pneumoniae (клебсиелла пневмонии)
Клебсиелла пневмонии является разновидностью грамотрицательных бактерий условно-патогенного типа. Они присутствуют в нормальной микрофлоре у человека на уровне кожи, кишечника, ротовой полости. Внешне она напоминает округлую небольших размеров палочку до 1-2 мкм, остается неподвижной, образует капсулы, споры. Расположение – скоплениями или одиночно.
В ЖКТ
Klebsiella образует колонии в кишечнике после рождения человеке в первую неделю жизни. Это нормально, лечение не требуется. Стандартно в 1 г кала выделяется около 10 5 бактерии. Этот показатель повышается при нарушении или болезнях, инфицировании ЖКТ. Прием антибиотиков ведет к подавлению патогенной флоры и нормальной, нужной человеку. Активно размножаются сапрофиты с патогенным действием. Клабсиелез в кишечнике появляется в результате:
У пациента прогрессирует гастродуоденит, гастрит, кишечная инфекция с резким началом и выраженными симптомами. Длительность тяжелого состояния – до 5 дней.
Часто Klebsiella становится причиной внутрибольничных инфекций, когда происходит массовое заражение стойкими к антибиотикам штаммами всех пациентов, персонала. Сильное поражение отмечается при слабом иммунитете, курсах химиотерапии.
Описываемая бактерия пневмонии вызывает поражения мочеполовых путей, т.к. для них всегда остается патогенной флорой. Она часто поражает влагалищную среду, особенно если пройдет курс антибиотикотерапии, нарушивший нормальную микрофлору.
Отдельного внимания заслуживает клебсиелла риносклеромы, она же – палочка Фриша-Волковича. Она влечет развитие склеромы как инфекционной болезни, охватывающей дыхательные верхние пути и слизистую носа, бронхов. Появляются инфильтраты с последующим рубцеванием.
Что касается клебсиеллы озены, она обнаруживается у 80% пациентов с диагностированной озеной, так называется зловонный насморк. Болезнь сопровождается атрофией костных стенок и слизистой в носу, из-за чего появляется секрет, при засыхании дающий зловонные корки. Такая бактерия ведет к хроническому поражению:
Лечение
Терапия клебсиеллезов основана на приеме антибиотиков, лекарств с содержанием бактериофаг. Последние оказывают избирательное действие, дают меньше эффекта, но и противопоказаний не влекут. Из пробиотиков рекомендован Энтерол. Антибиотики, проявляющие активность к бактерии, представлены норфлоксацином, гентамицином, левофлоксацином, офлоксацином. Она не восприимчива к клотримазолу.
Систематика бактерий
Klebsiella относится к семейству энтеробактерий, раннее название определено палочкой Фридлендера. Это фамилия микробиолога, сумевшего в 1882 году открыть чистую культуру.
Изначально бактерия определялась микроорганизмом, провоцирующим развитие пневмонии. По сути же это микроб условно-патогенного типа, который при нормальной ситуации пребывает в симбиозе с человеком на протяжении длительного периода. Но при нарушениях и сбоях в организме, ослабленной работе иммунной системы становится возбудителем тяжелых патологий.
В ходе проведения последних исследований по систематике клебсиел к описываемому виду бактерий принято относить следующие подвиды:
Если рассматривать МКБ-10, здесь клебсиелла пневмонии отнесена в блок В95-В98 к «Вирусным, бактериальным, иным инфекционным агентам. Имеется отдельная подрубрика типа В96.1.
Упоминается клебсиелла и в «Классе Х с Болезнями дыхательных органов J00-J99.
КИШЕЧНЫЙ ДИСБАКТЕРИОЗ
Что понимают под дисбактериозом? Какие методы диагностики являются современными и достоверными? Какие лекарственные препараты применяются при дисбактериозе? Вкишечнике человека находится свыше 500 различных видов микробов, общее количество которых
Что понимают под дисбактериозом?
Какие методы диагностики являются современными и достоверными?
Какие лекарственные препараты применяются при дисбактериозе?
Нормальная микробная флора кишечника
Количество анаэробов (пептострептококки, бактероиды, клостридии, пропионобактерии) составляет около 10% в тонкой и до 20% в толстой кишке. На долю энтеробактерий приходится 1% от суммарной микрофлоры слизистой оболочки.
Кишечные палочки, энтерококки, бифидобактерии и ацидофильные палочки обладают выраженными антагонистическими свойствами. В условиях нормально функционирующего кишечника они способны подавлять рост несвойственных нормальной микрофлоре микроорганизмов.
Расщепление непереваренных пищевых веществ в толстой кишке осуществляется ферментами бактерий, при этом образуются разнообразные амины, фенолы, органические кислоты и другие соединения. Токсические продукты микробного метаболизма (кадаверин, гистамин и другие амины) выводятся с мочой и в норме не оказывают влияния на организм. При утилизации микробами неперевариваемых углеводов (клетчатки) образуются короткоцепочечные жирные кислоты. Они обеспечивают клетки кишки энергоносителями и, следовательно, улучшают трофику слизистой оболочки. При дефиците клетчатки может нарушаться проницаемость кишечного барьера вследствие дефицита короткоцепочечных жирных кислот. В результате кишечные микробы могут проникать в кровь.
Под влиянием микробных ферментов в дистальных отделах подвздошной кишки происходит деконъюгация желчных кислот и преобразование первичных желчных кислот во вторичные. В физиологических условиях от 80 до 95% желчных кислот реабсорбируется, остальные выделяются с фекалиями в виде бактериальных метаболитов. Последние способствуют нормальному формированию каловых масс: тормозят всасывание воды и тем самым препятствуют излишней дегидратации кала.
Дисбактериоз
В понятие дисбактериоза кишечника входит избыточное микробное обсеменение тонкой кишки и изменение микробного состава толстой кишки. Нарушение микробиоценоза происходит в той или иной степени у большинства больных с патологией кишечника и других органов пищеварения. Следовательно, дисбактериоз является бактериологическим понятием. Он может рассматриваться как одно из проявлений или осложнение заболевания, но не самостоятельная нозологическая форма.
Крайней степенью дисбактериоза кишечника является появление бактерий желудочно-кишечного тракта в крови (бактериемия) или даже развитие сепсиса.
Состав микрофлоры кишечника нарушается при болезнях кишечника и других органов пищеварения, лечении антибиотиками и иммунодепрессантами, воздействиях вредных факторов внешней среды.
Клинические проявления дисбактериоза зависят от локализации дисбиотических изменений.
Дисбактериоз тонкой кишки
При дисбактериозе тонкой кишки численность одних микробов в слизистой оболочке тонкой кишки увеличена, а других уменьшена. Отмечается увеличение Eubacterium (в 30 раз), α-стрептококков (в 25 раз), энтерококков (в 10 раз), кандид (в 15 раз), появление бактерий рода Acinetobacter и вирусов герпеса. Уменьшается от 2 до 30 раз количество большинства анаэробов, актиномицетов, клебсиелл и других микроорганизмов, являющихся естественными обитателями кишечника.
Причиной дисбактериоза могут быть: а) избыточное поступление микроорганизмов в тонкую кишку при ахилии и нарушении функции илеоцекального клапана; б) благоприятные условия для развития патологических микроорганизмов в случаях нарушения кишечного пищеварения и всасывания, развития иммунодефицита и нарушений проходимости кишечника.
Повышенная пролиферация микробов в тонкой кишке приводит к преждевременной деконъюгации желчных кислот и потере их с калом. Избыток желчных кислот усиливает моторику толстой кишки и вызывает диарею и стеаторею, а дефицит желчных кислот приводит к нарушению всасывания жирорастворимых витаминов и развитию желчнокаменной болезни.
Бактериальные токсины и метаболиты, например фенолы и биогенные амины, могут связывать витамин В12.
Некоторые микроорганизмы обладают цитотоксическим действием и повреждают эпителий тонкой кишки. Это ведет к уменьшению высоты ворсинок и углублению крипт. При электронной микроскопии выявляется дегенерация микроворсинок, митохондрий и эндоплазматической сети.
Дисбактериоз толстой кишки
Состав микрофлоры толстой кишки может меняться под влиянием различных факторов и неблагоприятных воздействий, ослабляющих защитные механизмы организма (экстремальные климатогеографические условия, загрязнение биосферы промышленными отходами и различными химическими веществами, инфекционные заболевания, болезни органов пищеварения, неполноценное питание, ионизирующая радиация).
Клинические особенности дисбактериоза
Особенностей клинического течения заболевания у больных с различными вариантами дисбактериоза толстой кишки, по данным бактериологических анализов кала, в большинстве случаев установить не удается. Можно отметить, что больные хроническими заболеваниями кишечника чаще инфицируются острыми кишечными инфекциями по сравнению со здоровыми. Вероятно, это связано со снижением у них антагонистических свойств нормальной микрофлоры кишечника и, прежде всего, частым отсутствием бифидобактерий.
Особенно большую опасность представляет псевдомембранозный колит, развивающийся у некоторых больных, длительно лечившихся антибиотиками широкого спектра действия. Этот тяжелый вариант дисбактериоза вызывается токсинами, выделяемыми синегнойной палочкой Clostridium difficile, которая размножается в кишечнике при угнетении нормальной микробной флоры.
Основным симптомом псевдомембранозного колита является обильная водянистая диарея, началу которой предшествовало назначение антибиотиков. Затем появляются схваткообразные боли в животе, повышается температура тела, в крови нарастает лейкоцитоз. Эндоскопическая картина псевдомембранозного колита характеризуется наличием бляшковидных, лентовидных и сплошных «мембран», мягких, но плотно спаянных со слизистой оболочкой. Изменения наиболее выражены в дистальных отделах ободочной и прямой кишок. Слизистая оболочка отечная, но не изъязвлена. При гистологическом исследовании обнаруживают субэпителиальный отек с круглоклеточной инфильтрацией собственной пластинки, капиллярные стазы с выходом эритроцитов за пределы сосудов. На стадии образования псевдомембран под поверхностным эпителием слизистой оболочки возникают экссудативные инфильтраты. Эпителиальный слой приподнимается и местами отсутствует; оголенные места слизистой оболочки прикрыты лишь слущенным эпителием. На поздних стадиях болезни эти участки могут занимать большие сегменты кишки.
Очень редко наблюдается молниеносное течение псевдомембранозного колита, напоминающее холеру. Обезвоживание развивается в течение нескольких часов и заканчивается летальным исходом.
Таким образом, оценка клинической значимости дисбиотических изменений должна основываться прежде всего на клинических проявлениях, а не только на результатах исследования микрофлоры кала.
Методы диагностики
Диагностика дисбактериоза представляет собой сложную и трудоемкую задачу. Для диагностики дисбактериоза тонкой кишки применяют посев сока тонкой кишки, полученного с помощью стерильного зонда. Дисбактериоз толстой кишки выявляют с помощью бактериологических исследований кала.
Микробная флора образует большое количество газов, в том числе водорода. Это явление используют для диагностики дисбактериоза. Концентрация водорода в выдыхаемом воздухе натощак находится в прямой зависимости от выраженности бактериального обсеменения тонкой кишки. У больных с заболеваниями кишечника, протекающими с хронической рецидивирующей диареей и бактериальным обсеменением тонкой кишки, концентрация водорода в выдыхаемом воздухе значительно превышает 15 ppm.
Для диагностики дисбактериоза применяют также нагрузку лактулозой. В норме лактулоза не расщепляется в тонкой кишке и метаболизируется микробной флорой толстой кишки. В результате количество водорода в выдыхаемом воздухе повышается (рис. 1).
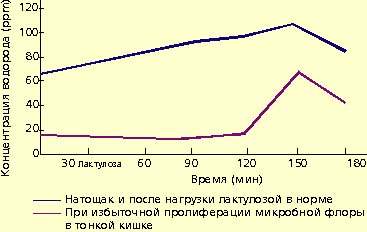 |
| Рисунок 1. Концентрация водорода в выдыхаемом воздухе |
Наиболее частыми бактериологическими признаками дисбактериоза толстой кишки являются отсутствие основных бактериальных симбионтов — бифидобактерий и уменьшение количества молочнокислых палочек. Увеличивается количество кишечных палочек, энтерококков, клостридий, стафилококков, дрожжеподобных грибов и протея. У отдельных бактериальных симбионтов появляются патологические формы. К ним относятся гемолизирующая флора, кишечные палочки со слабо выраженными ферментативными свойствами, энтеропатогенные кишечные палочки и т. д.
Углубленное изучение микробиоценоза показало, что традиционные методы не позволяют получить истинную информацию о состоянии микрофлоры кишечника. Из 500 известных видов микробов в целях диагностики обычно изучаются лишь 10-20 микроорганизмов. Важно, в каком отделе — в тощей, подвздошной или толстой кишках — исследуется микробный состав. Поэтому перспективы разработки клинических проблем дисбактериоза в настоящее время связывают с применением химических методов дифференциации микроорганизмов, позволяющих получить универсальную информацию о состоянии микробиоценоза. Наиболее широко для этих целей используются газовая хроматография (ГХ) и газовая хроматография в сочетании с масс-спектрометрией (ГХ-МС). Этот метод позволяет получить уникальную информацию о составе мономерных химических компонентов микробной клетки и метаболитов. Маркеры такого рода могут быть определены и использованы для детектирования микроорганизмов. Главным преимуществом и принципиальным отличием этого метода от бактериологических является возможность количественного определения более 170 таксонов клинически значимых микроорганизмов в различных средах организма. При этом результаты исследования могут быть получены в течение нескольких часов.
Проведенные нами исследования микробиоценоза в крови и биоптатов слизистой оболочки тонкой и толстой кишок у больных с синдромом раздраженного кишечника позволили обнаружить отклонения от нормы до 30-кратного увеличения или уменьшения многих компонентов. Существует возможность оценки изменений микрофлоры кишечника на основании данных анализа крови методом ГХ-МС-микробных маркеров.
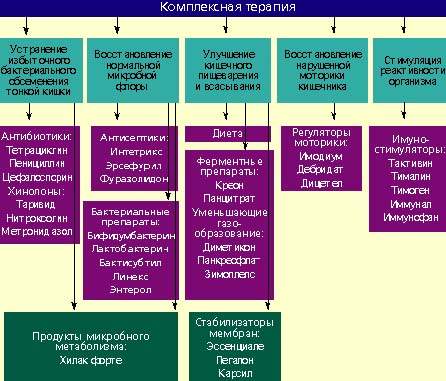 |
Лечение
Лечение дисбактериоза должно быть комплексным (схема) и включать в себя следующие мероприятия:
Антибактериальные препараты
Антибактериальные препараты необходимы в первую очередь для подавления избыточного роста микробной флоры в тонкой кишке. Наиболее широко применяются антибиотики из группы тетрациклинов, пенициллинов, цефалоспорины, хинолоны (таривид, нитроксолин) и метронидазол.
Однако антибиотики широкого спектра действия в значительной степени нарушают эубиоз в толстой кишке. Поэтому они должны применяться только при заболеваниях, сопровождающихся нарушениями всасывания и моторики кишечника, при которых, как правило, отмечается выраженный рост микробной флоры в просвете тонкой кишки.
Антибиотики назначают внутрь в обычных дозах в течение 7–10 дней.
При заболеваниях, сопровождающихся дисбактериозом толстой кишки, лечение лучше проводить препаратами, которые оказывают минимальное влияние на симбионтную микробную флору и подавляют рост протея, стафилококков, дрожжевых грибов и других агрессивных штаммов микробов. К ним относятся антисептики: интетрикс, эрсефурил, нитроксолин, фуразолидон и др.
При тяжелых формах стафилококкового дисбактериоза применяют антибиотики: таривид, палин, метронидазол (трихопол), а также бисептол-480, невиграмон.
Антибактериальные препараты назначают в течение 10–14 дней. В случае появления в кале или кишечном соке грибов показано применение нистатина или леворина.
У всех больных с диареей, ассоциированной с антибиотиками, протекающей с интоксикацией и лейкоцитозом, возникновение острой диареи следует связывать с Cl. difficile.
В этом случае срочно делают посев кала на Cl. difficile и назначают ванкомицин по 125 мг внутрь 4 раза в сутки; при необходимости доза может быть увеличена до 500 мг 4 раза в день. Лечение продолжают в течение 7-10 суток. Эффективен также метронидазол в дозе 500 мг внутрь 2 раза в сутки, бацитрацин по 25 000 МЕ внутрь 4 раза в сутки. Бацитрацин почти не всасывается, в связи с чем в толстой кишке можно создать более высокую концентрацию препарата. При обезвоживании применяют адекватную инфузионную терапию для коррекции водно-электролитного баланса. Для связывания токсина Cl. difficile используют холестирамин (квестран).
Бактериальные препараты
Живые культуры нормальной микробной флоры выживают в кишечнике человека от 1 до 10% от общей дозы и способны в какой-то мере выполнять физиологическую функцию нормальной микробной флоры. Бактериальные препараты можно назначать без предварительной антибактериальной терапии или после нее. Применяют бифидумбактерин, бификол, лактобактерин, бактисубтил, линекс, энтерол и др. Курс лечения длится 1-2 месяца.
Возможен еще один способ устранения дисбактериоза — воздействие на патогенную микробную флору продуктами метаболизма нормальных микроорганизмов. К таким препаратам относится хилак форте. Он создан 50 лет назад и до настоящего времени применяется для лечения больных с патологией кишечника. Хилак форте представляет собой стерильный концентрат продуктов обмена веществ нормальной микрофлоры кишечника: молочной кислоты, лактозы, аминокислот и жирных кислот. Эти вещества способствуют восстановлению в кишечнике биологической среды, необходимой для существования нормальной микрофлоры, и подавляют рост патогенных бактерий. Возможно, продукты метаболизма улучшают трофику и функцию эпителиоцитов и колоноцитов. 1 мл препарата соответствует биосинтетическим активным веществам 100 млрд. нормальных микроорганизмов. Хилак форте назначают по 40–60 капель 3 раза в день на срок до 4 недель в сочетании с препаратами антибактериального действия или после их применения.
Совсем недавно появились сообщения о возможности лечения острой диареи, ассоциированной с антибактериальной терапией и Cl. difficile, большими дозами пре- и пробиотиков.
Регуляторы пищеварения и моторики кишечника
У больных с нарушением полостного пищеварения применяют креон, панцитрат и другие панкреатические ферменты. С целью улучшения функции всасывания назначают эссенциале, легалон или карсил, т. к. они стабилизируют мембраны кишечного эпителия. Пропульсивную функцию кишечника улучшают имодиум (лоперамид) и тримебутин (дебридат).
Стимуляторы реактивности организма
Для повышения реактивности организма ослабленным больным целесообразно применять тактивин, тималин, тимоген, иммунал, иммунофан и другие иммуностимулирующие средства. Курс лечения должен составлять в среднем 4 недели. Одновременно назначаются витамины.
Профилактика дисбактериоза
Первичная профилактика дисбактериоза представляет очень сложную задачу. Ее решение связано с общими профилактическими проблемами: улучшением экологии, рациональным питанием, улучшением благосостояния и прочими многочисленными факторами внешней и внутренней среды.
Вторичная профилактика предполагает рациональное применение антибиотиков и других медикаментов, нарушающих эубиоз, своевременное и оптимальное лечение болезней органов пищеварения, сопровождающихся нарушением микробиоценоза.