R nh2 что это
Характерные химические свойства азотсодержащих органических соединений. Важнейшие способы получения аминов и аминокислот
Содержание:
Азотсодержащие соединения – это молекулы, имеющие в строении атомы азота. С помощью инертного газа образуются различные классы органических соединений:
Амины
Амины – аммиачные производные, которые рассматриваются как замещенный продукт водородных атомов на органические радикалы (R).
У аминов так же как и в растворе аммиака проявляются слабые основные свойства. Классифицируются по числу катионов водорода, которые заместили, на:
Амины разделяют по характеру органических заместителей:
Когда аминогруппа в ароматических аминах связана с ароматическим ядром, то амины являются более слабыми снованиями по сравнению с аммиаком. Так как неподеленная электронная пара атома азота смещается в сторону ароматической π-системы бензольного кольца, таким образом электронная плотность на атоме азота снижается. Бензольное ядро, обладающее большей энергией ионизации, оттягивает на себя электронную плотность молекулы. В результате основные свойства снижаются в реакциях, например взаимодействия с водой. Так, анилин реагирует только с сильными кислотами, а с водой практически не реагирует.
Способы получения аминов
Амины сохраняют многие особенности аммиака – запах, растворимость в воде, сильные основные свойства.
Химические реакции аминов
Химические свойства определяются реакционными центрами (РЦ):
У непредельных аминов роль первого РЦ незначительна, т.к. ароматическое кольцо смещает на себя плотность и неподеленная пара электронов азота в проявлении основных свойств не принимает участия.
I. Основные свойства
Атом азота в амине принимает участие в образовании ковалентной связи, выступая как донор, благодаря внешней паре электронов. Т.о. амины присоединяют катион водорода и проявлять свойства основания.
По сравнению с основностью аммиака, амин проявляет большие основные свойства. Это связано с тем, что индуктивный эффект направлен на аминогруппу и азот становится более активным, т.е. прочнее связывает протон.
Степень проявления основных свойств зависит от величины частичного отрицательного заряда на азоте. Чем он выше, тем сильнее основные свойства.
Предельные первичные амины реагируют с азотистой кислотой с образованием спиртов, азота N2 и воды. Например:
Вторичные амины дают при похожих условиях маслянистые жидкости с характерным запахом, поэтому и название N-нитрозаминами.
Третичные амины с азотистой кислотой не взаимодействуют.
Сгорание любых аминов приводит к образованию углекислого газа, воды и азота:
II. Слабые кислотные свойства
Первичным и вторичным аминам характерен разрыв связи N-H и замещение атома водорода на другие функциональные группы.
III. Качественная реакция на амины
Она осуществляется с помощью азотистой кислоты, которую необходимо получить непосредственно в момент реакции.
Амины широко применяют в фармакологической промышленности в препаратах с упрощенной адреналиновой структурой, а также в строительной отрасли в качестве компонента полимерных материалов.
Аминокислоты
Аминокислоты – это органические вещества, которые включают в себя аминогруппу (-NH2) и карбоксигруппу (-COOH). Единая формула аминокислот – (NH2)xR(COOH)y, где x и y принимают значения больше одного.
Аминокислоты – это элементарная структура белков, из которых состоят структуры животного тела. В состав белков входят только α-аминокислоты. На планете Земля 20 аминокислот, общая формула которых H2N-CH(R)-COOH. Эта двадцатка содержит в себе радикалы – углеводородные, кислородсодержащие, серосодержащие, азотсодержащие и ароматические.
Способы получения аминокислот
Аминокислоты – это бесцветные кристаллы, плавящиеся при 200°C. Они способны растворяться в воде, но нерастворимы в эфирах.
Микроорганизмы при нарушении нормальной жизнедеятельности начинают синтезировать аминокислоту, вместо того, чтобы накапливать белок.
Химические свойства аминокислот
В составе аминокислот две функциональные группы, поэтому с одной группой веществ они ведут себя как амины, с другой как карбоновые кислоты, а с третьей – проявляют все свойства сразу.
I. Карбоксильная группа – ее химические реакции
Многие химические свойства, характерные для спиртов, встречаются и у аминокислот. Реакции задействуют только группу –COOH.
II. Аминогруппа – ее химические реакции
Многие химические свойства, характерные для аминов, встречаются и у аминокислот. Реакции задействуют только группу ––NH2.
III. Реакции по обеим группам
Ряд химических свойств связан с действием реактивов на все функциональные группы.
Аминокислоты – это звенья, из которых составляются нити белка. Из них строятся живые ткани на планете. Почти все аминокислоты организм использует для построения органики тела. Некоторые играют роль медиаторов в нервных импульсах, другие используются в химической промышленности для проведения синтезов, третьи – в пищевой отрасли.
Амины
Классификация аминов
По числу углеводородных радикалов амины подразделяются на первичные, вторичные и третичные.
Запомните, что основные свойства аминов выражены тем сильнее, чем больше электронной плотности присутствует на атоме азота. Однако, у третичных аминов три углеводородных радикала создают значительные затруднения для химических реакций.
Таким образом, у третичных аминов основные свойства выражены слабее, чем у вторичных аминов. Основные свойства возрастают в ряду: третичные амины (слабые основные свойства) → первичные амины → вторичные амины (основные свойства хорошо выражены).
Номенклатура и изомерия аминов
Названия аминов формируются путем добавления суффикса «амин» к названию соответствующего углеводородного радикала: метиламин, этиламин, пропиламин, изопропиламин, бутиламин и т.д. В случае если радикалов несколько, их перечисляют в алфавитном порядке.
Общая формула предельных аминов CnH2n+3N. Атомы углерода находятся в sp3 гибридизации.
Для аминов характерна структурная изомерия: углеродного скелета, положения функциональной группы и изомерия аминогруппы.
Получение
В основе этой реакции лежит замещение атома галогена в галогеналканах на аминогруппу, при этом образуются амин и соль аммония.
При такой реакции нитрогруппа превращается в аминогруппу, образуется вода.
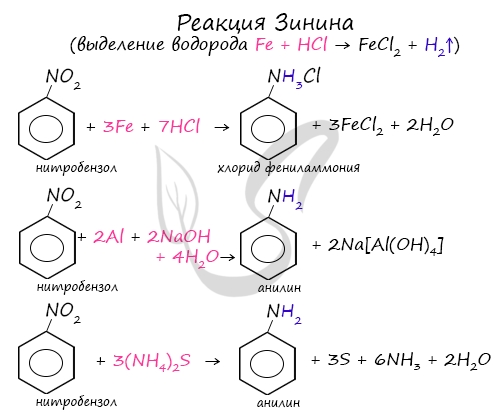
Знаменитой является предложенная в 1842 году Н.Н. Зининым реакция получения аминов восстановления ароматических нитросоединений (анилина и других). Она возможна в нескольких вариантах, главное, чтобы в начале реакции выделился водород.
Реакция сопровождается разрушением карбонильной группы и отщеплении ее от молекулы амида в виде воды.
В промышленности амины получают реакцией аммиака со спиртами, в ходе которой происходит замещение гидроксогруппы на аминогруппу.
В ходе реакции галогеналканов с аммиаком, аминами, становится возможным получение первичных, вторичных и третичных аминов.
Химические свойства аминов
Как и аммиак, амины обладают основными свойствами, их растворы окрашивают лакмусовую бумажку в синий цвет.
В реакции с водой амины образуют гидроксиды алкиламмония, которые аналогичны гидроксиду аммония. Анилин с водой не реагирует, так как является слабым основанием.
Как основания, амины вступают в реакции с различными кислотами и образуют соли алкиламмония.
Данная реакция помогает различить первичные, вторичные и третичные амины, которые по-разному с ней взаимодействуют.
При конденсации первичных аминов с альдегидами и кетонами получают основания Шиффа, соединения, которые содержат фрагмент «N=C».
Соли аминов легко разлагаются щелочами (растворимыми основаниями). В результате образуется исходный амин, соль кислоты и вода.
При горении аминов азот чаще всего выделяется в молекулярном виде, так как для реакции азота с кислородом необходима очень высокая температура. Выделение углекислого газа и воды обыкновенно при горении органических веществ.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
R nh2 что это
Окружающая нас природа удивительно многоцветна. Никто никогда не сосчитает точное число всех оттенков, передающих многообразие природной гаммы цвета.
Окраска природных объектов обусловлена присутствием веществ, способных выборочно поглощать или отражать электромагнитные волны определённой длины.
Природа научилась синтезировать окрашенные вещества гораздо успешнее, чем это делает человек. С незапамятных времён люди применяли природные красители. Например, синий краситель индиго извлекали из сока индигоносных растений. Этот краситель, только получаемый промышленным способом, до сих пор используют для окраски джинсовой ткани.
Красящие вещества содержатся и в организмах насекомых. В Мексике за 1000 лет до нашей эры открыли красный краситель кармин. Его извлекали из насекомых кошенили, обитавших на кактусах. Краситель содержится только в особях женского пола, их собирали вручную, и для приготовления 1 г красителя требовалось собрать 150 000 тлей!
Вплоть до середины XIX в. краски для тканей стоили невероятно дорого и были доступны лишь обеспеченным людям. Вполне понятно желание химиков разгадать тайну цвета и научиться синтезировать качественные и доступные красители.
Студент английского Королевского химического колледжа Уильям Перкин проводил опыты по синтезу лекарства от малярии. В качестве исходного вещества он использовал вещество, выделенное из каменноугольной смолы, — анилин. Из смеси продуктов реакции 18-летний студент выделил соединение с яркой пурпурной окраской. Пурпурный цвет в то время был в моде, и новое соединение прочно удерживалось на тканях. Так в 1856 г. был запатентован первый синтетический краситель мовеин (от франц. mauve — мальва).
Совместно с братом и отцом Перкин построил фабрику по производству мовеина. Успех был ошеломительным! Королевские особы носили одежду, окрашенную новым красителем. В течение последующих нескольких лет на основе анилина химики синтезировали десятки красителей красного, розового, зелёного и синего цветов.
Какое отношение рассказ о синтетических красителях имеет к материалу конспекта? Самое непосредственное — поскольку анилин относят к классу органических соединений, называемых аминами.
(с) Цитата из справочного издания «ХИМИЯ. Справочник в таблицах / М.: Издательство АЙРИС-пресс»
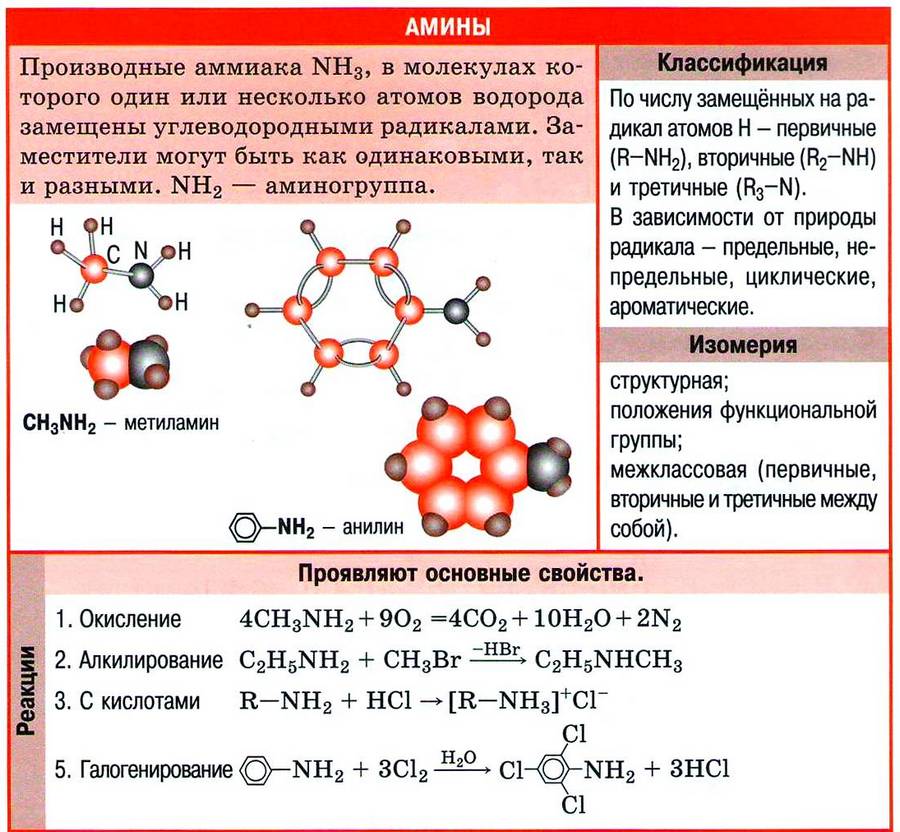
Классификация аминов
Общая формула аминов R—NH2, где R — углеводородный радикал. В зависимости от природы радикала различают предельные амины (R — остаток предельного углеводорода, т. е. алкил) и ароматические амины (R — остаток ароматического углеводорода).
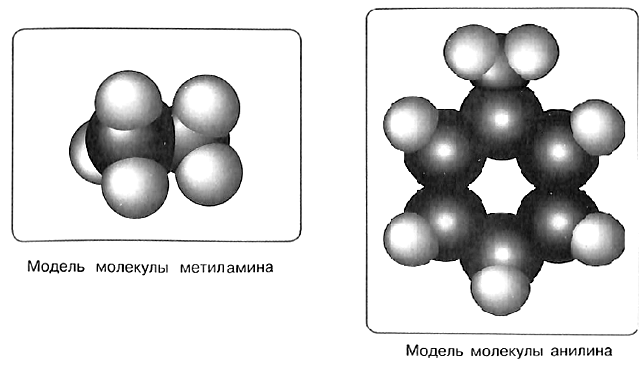
Гомологический ряд предельных аминов начинает простейший представитель класса — метиламин. Структурные формулы метиламина и его ближайших гомологов приведены ниже:
Общая формула членов данного гомологического ряда CnH2n+1NH2, или CnH2n+3N.
Представителем ароматических аминов является уже упомянутый нами анилин. В молекуле этого вещества аминогруппа —NH2 связана с остатком ароматического углеводорода бензола — фенильным радикалом С6Н5—. Следовательно, химическая формула анилина С6Н5—NH2:
Физические свойства и получение важнейших аминов
Метиламин — бесцветное газообразное вещество с резким аммиачным запахом, хорошо растворимое в воде. Анилин представляет собой бесцветную жидкость, которая на воздухе приобретает красно-бурую окраску вследствие окисления; он также обладает резким запахом и плохо растворим в воде.
Промышленное производство метиламина основано на взаимодействии метилового спирта с аммиаком:
Вторым удобным способом получения аминов заданного строения служит реакция галогеналканов с избытком аммиака:
Производство анилина в промышленных масштабах связано с именем выдающегося русского учёного-химика Николая Николаевича Зинина. В 1841 г., проводя опыты с нитробензолом, он нашёл способ восстановления нитрогруппы до аминогруппы:
Эту реакцию назвали в честь учёного — реакция Зинина. Современник Н. Н. Зинина немецкий химик Август Гофман по достоинству оценил вклад русского коллеги в развитие органической химии: «Если бы Зинин не сделал ничего более, кроме превращения нитробензола в анилин, то и тогда его имя осталось бы записанным золотыми буквами в истории химии».
Химические свойства аминов
Химические свойства аминов определяются в первую очередь наличием в их молекулах аминогруппы.
Амины рассматривают как продукты замещения в молекуле аммиака атомов водорода аминогруппами. Логично предположить, что химические свойства, характерные для аммиака, будут характерны и для его органических производных. Так оно и есть.
Аммиак характеризуется основными свойствами за счёт неподелённой электронной пары атома азота. Его водный раствор имеет щелочную реакцию, аммиак легко реагирует с кислотами с образованием солей аммония:
Амины представляют собой органические основания. Водный раствор метиламина, подобно аммиаку, изменяет окраску индикаторов, указывающих на щелочной характер среды. В растворе образуется слабый электролит — гидроксид метиламмония:
Электролитическая диссоциация этого основания приводит к появлению в растворе гидроксид-ионов:
Как и аммиак, амины легко образуют соли с сильными неорганическими кислотами:
Третье положение теории строения органических соединений о взаимном влиянии атомов в молекулах подтверждается сравнением свойств рассматриваемых аминов и аммиака.
Основные свойства аминов, по сравнению с аммиаком, отражают влияние углеводородного радикала на поведение аминогруппы. Усиление основных свойств наблюдается в ряду
Аминогруппа оказывает ответное влияние на свойства углеводородного радикала. Действительно, анилин, в отличие от бензола, легко вступает в реакцию бромирования при добавлении бромной воды, при этом никакого катализатора не требуется, а бромирование протекает не по одному, а по трём атомам углерода цикла:
Продукт реакции — 2,4,6-триброманилин — это нерастворимое в воде вещество белого цвета, поэтому реакцию с бромной водой можно использовать для обнаружения анилина, т. е. как качественную реакцию на анилин.
Области применения аминов
Предельные амины широко используют в органическом синтезе для производства лекарственных веществ, синтетических волокон, пластмасс, стимуляторов роста растений. Встречаются предельные амины и в природе. Они являются результатом разложения природных азотсодержащих органических веществ и часто имеют неприятный запах, напоминающий запах протухшей рыбы.
Основное количество получаемого в промышленности анилина используют для производства полимерных материалов (полиуретана), лекарств, взрывчатых веществ, гербицидов, красителей.
Аминогруппа входит в состав не только аминов, но и более сложных органических соединений. О них пойдёт речь в следующем конспекте.
Справочная таблица «Амины»
Конспект урока по химии «Амины». В учебных целях использованы цитаты из пособия «Химия. 10 класс : учеб, для общеобразоват. организаций : базовый уровень / О. С. Габриелян, И. Г. Остроумов, С. А. Сладков. — М. : Просвещение». Выберите дальнейшее действие:
Амины: способы получения, строение и свойства
Амины – это органические производные аммиака NH3, в молекуле которого один, два или три атома водорода замещены на углеводородные радикалы.
Строение аминов
Также атом азота в аминах имеет неподелённую электронную пару, поэтому амины проявляют свойства органических оснований.
Классификация аминов
По количеству углеводородных радикалов, связанных с атомом азота, различают первичные, вторичные и третичные амины.
По типу радикалов амины делят на алифатические, ароматические и смешанные.
| Амины | Первичные | Вторичные | Третичные | |||||||||||
| Алифатические | Метиламин CH3-NH2 | Диметиламин CH3-NH-CH3 | Триметиламин (CH3)3N | |||||||||||
| Ароматические | Фениламин C6H5-NH2 | Дифениламин (C6H5)2NH | Трифениламин (C6H5)3N | |||||||||||
| Смешанные | Метилфениламин CH3-NH-C6H5 | ДиметилфениламинНоменклатура аминовПри наличии одинаковых радикалов используют приставки ди и три. В этом случае аминогруппа указывается в названии приставкой амино-: Например, N-метиланилин: Символ N- ставится перед названием алкильного радикала, чтобы показать, что этот радикал связан с атомом азота, а не является заместителем в бензольном кольце. Изомерия аминовДля аминов характерна изомерия углеродного скелета, изомерия положения аминогруппы и изомерия различных типов аминов. Изомерия углеродного скелетаДля аминов характерна изомерия углеродного скелета (начиная с С4H9NH2).
Изомерия положения аминогруппыДля аминов характерна изомерия положения аминогруппы (начиная с С3H9N).
Изомерия между типами аминов
(первичный амин) | Метилэтиламин (вторичный амин) | Триметиламин (третичный амин) | ||||||||||
 |  |  |
Физические свойства аминов
При обычной температуре низшие алифатические амины CH3NH2, (CH3)2NH и (CH3)3N – газы (с запахом аммиака), средние гомологи – жидкости (с резким рыбным запахом), высшие – твердые вещества без запаха.
Ароматические амины – бесцветные жидкости с высокой температурой кипения или твердые вещества.
Первичные и вторичные амины образуют слабые межмолекулярные водородные связи:
Это объясняет относительно более высокую температуру кипения аминов по сравнению с алканами с близкой молекулярной массой.
Амины также способны к образованию водородных связей с водой:
Поэтому низшие амины хорошо растворимы в воде.
С увеличением числа и размеров углеводородных радикалов растворимость аминов в воде уменьшается. Ароматические амины в воде не растворяются.
Химические свойства аминов
| Амины имеют сходное с аммиаком строение и проявляют подобные ему свойства. |
Как в аммиаке, так и в аминах атом азота имеет неподеленную пару электронов:


| Поэтому амины и аммиак обладают свойствами оснований. |
1. Основные свойства аминов
| Алифатические амины являются более сильными основаниями, чем аммиак, а ароматические — более слабыми. |
Это объясняется тем, что радикалы СН3–, С2Н5– увеличивают электронную плотность на атоме азота:
Это приводит к усилению основных свойств.
| Основные свойства аминов возрастают в ряду: |
1.1. Взаимодействие с водой
В водном растворе амины обратимо реагируют с водой. Среда водного раствора аминов — слабощелочная:
1.2. Взаимодействие с кислотами
Амины реагируют с кислотами, как минеральными, так и карбоновыми, и аминокислотами, образуя соли (или амиды в случае карбоновых кислот):
При взаимодействии аминов с многоосновными кислотами возможно образование кислых солей:
1.3. Взаимодействие с солями
Амины способны осаждать гидроксиды тяжелых металлов из водных растворов.
| Например, при взаимодействии с хлоридом железа (II) образуется осадок гидроксида железа (II): |
2. Окисление аминов
Амины сгорают в кислороде, образуя азот, углекислый газ и воду. Например, уравнение сгорания этиламина:
3. Взаимодействие с азотистой кислотой
Первичные алифатические амины при действии азотистой кислоты превращаются в спирты:
| Это качественная реакция на первичные амины – выделение азота. |
Вторичные амины (алифатические и ароматические) образуют нитрозосоединения — вещества желтого цвета:
4. Алкилирование аминов
Первичные амины способны взаимодействовать с галогеналканами с образованием соли вторичного амина:
Из полученной соли щелочью выделяют вторичный амин, который можно далее алкилировать до третичного амина.
Особенности анилина
Анилин С6H5-NH2 – это ароматический амин.
| Анилин – бесцветная маслянистая жидкость с характерным запахом. На воздухе окисляется и приобретает красно-бурую окраску. Ядовит. В воде практически не растворяется. |
При 18 о С в 100 мл воды растворяется 3,6г анилина. Раствор анилина не изменяет окраску индикаторов.
| Для анилина характерны реакции как по аминогруппе, так и по бензольному кольцу. |
Анилин не реагирует с водой, но реагирует с сильными кислотами, образуя соли:
Реакция с галогенами идёт без катализатора во все три орто- и пара- положения.
| Качественная реакция на анилин: реагирует с бромной водой с образованием 2,4,6-триброманилина (белый осадок ↓). |
Получение аминов
Восстановление нитросоединений
Первичные амины можно получить восстановлением нитросоединений.
Алюминий реагирует с щелочами с образованием гидроксокомплексов.
В щелочной и нейтральной среде получаются амины.
Восстановлением нитробензола получают анилин.
При этом образуются не сами амины, а соли аминов:
Амины из раствора соли выделяют с помощью щелочи:
Алкилирование аммиака и аминов
При взаимодействии аммиака с галогеналканами происходит образование соли первичного амина, из которой действием щелочи можно выделить сам первичный амин.
Если проводить реакцию с избытком аммиака, то сразу получится амин, а галогеноводород образует соль с аммиаком:
Гидрирование нитрилов
Таким образом получают первичные амины. Возможно восстановление нитрилов водородом на катализаторе:
.
Соли аминов
Соль амина с более слабыми основными свойствами может реагировать с другим амином, образуя новую соль (более сильные амины вытесняют менее сильные из солей):
12 комментариев
Добавить ваш
Да, спасибо, поправил. В узком смысле реакцией Зинина называют получение именно ароматических аминов, в широком смысле так называют восстановление любых нитросоединений сульфидом аммония.
Здравствуйте! Скажите, пожалуйста, реагируют ли третичные амины с галогеналканами? Если да, то как идет реакция и что получается? Например,при взаимодействии триметиламина с хлорметаном?
Здравствуйте! Реагируют, но дальнейшее замещение по связям N-H не идет.
Здравствуйте! Не показано взаимодействие аминов со спиртами.
Третичные амины с алкилгалогенидами реагируют. Получаются четвертичные аммониевые соли. Говорить, что они вообще не реагируют, неправильно. Они не вступают в реакцию алкилирования.
По такой схеме за счет пары электронов на азоте реагируют алифатические амины, ароматические амины, пиридин с получением N-алкилпиридинийхлорида (иодида) и пр.
Да, спасибо за комментарий. Я имел в виду, что не идет дальнейшее замещение.
спасибо, отличная идея!
для полноты информации я бы добавил оптическую изомерию и примеры этой изомерии ко всем классам органических веществ, потому что на егэ это есть
На ЕГЭ пока оптической изомерии нет.
Admin>Здравствуйте! Реагируют, но дальнейшее замещение по связям N-H не идет.
что значит «дальнейшее»? у триметиламина — и так уже нет N-H связей, может вы имели в виду протонированный триметил-амин (скажем) солянокислый, что в форме соли он останется третичным амином например до момента щелочного депротонирования(высвобождения основания амина)
—
а что кстати, есть способ галоидным алкилом моноалкилирование первичного ароматического амина до вторичного осуществить, избежав образования третичного амина — диалкилированного уже
на этилировании уже проще, а вот метиллирование нейромедиаторов не удавалось остановить на стадии N,N-ДиМет.(например в ацетоне с карбонатом калия, или с DIPEA), выход третичного целевого амина всегда оказывался либо самым низким из продуктов реакции, либо просто очень низким(10% в сложной смеси аминов с преобладанием четвертичной соли триметиламмония метилиодида, а сейчас подумал — если при N-метилировании первичного ароматического амина метилиодидом, образуется гидроиодид N-метил…исх.пер.амина, он же даже во второе метиллирование уже не должен входить, усиленным основанием став (скажем адреналином, основнее норадреналина исходного как я понимаю за счет появившегося электроннодонороного метила) и так будет выведен из реакционной среды(например выпав осадком соли, не солватированной в неполярной РС)
получается в отсутствие основного катализа алкилирование первичных аминов ограничивается моно-алкилированием — не далее чем до вторичного амина? или на практике соли не так надёжны как в оптимистичных прогнозах теоретизирующего учащегося?
Добавить комментарий Отменить ответ
Этот сайт использует Akismet для борьбы со спамом. Узнайте, как обрабатываются ваши данные комментариев.