ушиб тазобедренного сустава код мкб
Поверхностная травма области тазобедренного сустава и бедра (S70)
Алфавитные указатели МКБ-10
Внешние причины травм — термины в этом разделе представляют собой не медицинские диагнозы, а описание обстоятельств, при которых произошло событие (Класс XX. Внешние причины заболеваемости и смертности. Коды рубрик V01-Y98).
Лекарственные средства и химические вещества — таблица лекарственных средств и химических веществ, вызвавших отравление или другие неблагоприятные реакции.
В России Международная классификация болезней 10-го пересмотра (МКБ-10) принята как единый нормативный документ для учета заболеваемости, причин обращений населения в медицинские учреждения всех ведомств, причин смерти.
МКБ-10 внедрена в практику здравоохранения на всей территории РФ в 1999 году приказом Минздрава России от 27.05.97 г. №170
Выход в свет нового пересмотра (МКБ-11) планируется ВОЗ в 2022 году.
Сокращения и условные обозначения в Международой классификации болезней 10-го пересмотра
БДУ — без дополнительных уточнений.
НКДР — не классифицированный(ая)(ое) в других рубриках.
† — код основной болезни. Главный код в системе двойного кодирования, содержит информацию основной генерализованной болезни.
* — факультативный код. Дополнительный код в системе двойного кодирования, содержит информацию о проявлении основной генерализованной болезни в отдельном органе или области тела.
Травмы области тазобедренного сустава и бедра (S70-S79)
Исключена: травматическая ампутация области тазобедренного сустава и бедра (S78.-)
Исключена: травма подколенной артерии (S85.0)
Исключена: травматическая ампутация ноги на неуточненном уровне (T13.6)
Алфавитные указатели МКБ-10
Внешние причины травм — термины в этом разделе представляют собой не медицинские диагнозы, а описание обстоятельств, при которых произошло событие (Класс XX. Внешние причины заболеваемости и смертности. Коды рубрик V01-Y98).
Лекарственные средства и химические вещества — таблица лекарственных средств и химических веществ, вызвавших отравление или другие неблагоприятные реакции.
В России Международная классификация болезней 10-го пересмотра (МКБ-10) принята как единый нормативный документ для учета заболеваемости, причин обращений населения в медицинские учреждения всех ведомств, причин смерти.
МКБ-10 внедрена в практику здравоохранения на всей территории РФ в 1999 году приказом Минздрава России от 27.05.97 г. №170
Выход в свет нового пересмотра (МКБ-11) планируется ВОЗ в 2022 году.
Сокращения и условные обозначения в Международой классификации болезней 10-го пересмотра
БДУ — без дополнительных уточнений.
НКДР — не классифицированный(ая)(ое) в других рубриках.
† — код основной болезни. Главный код в системе двойного кодирования, содержит информацию основной генерализованной болезни.
* — факультативный код. Дополнительный код в системе двойного кодирования, содержит информацию о проявлении основной генерализованной болезни в отдельном органе или области тела.
Ушиб тазобедренного сустава, бедра причины, симптомы, методы лечения и профилактики
Ушиб — механическое повреждение мягких тканей в области тазобедренного сустава и части нижней конечности, при котором отсутствуют существенные нарушения их структур. Повреждается кожа, подкожная жировая клетчатка, надкостница, мышцы, особенно при тяжёлом ударе страдают мягкие ткани. Травмы получают люди любого возраста и по разным причинам. Чаще возникают в быту, во время занятий спортом, при падении на бок, ударе, столкновении. Самые постоянные симптомы — боль, отёчность, ограничение подвижности, синяки. Диагностикой и лечением ушиба тазобедренного сустава занимаются врачи-ортопеды и травматологи.
Причины
Повреждение тканей в области тазобедренного сустава, бедра возникает под воздействием механического фактора. Ушиб может быть получен при падении, подворачивании ноги, от удара тупым предметом, в условиях производственных, бытовых, спортивных, уличных травм, дорожно-транспортных происшествий, в результате природных и промышленных катастроф, криминальных инцидентов.
Статью проверил
Дата публикации: 24 Марта 2021 года
Дата проверки: 24 Марта 2021 года
Дата обновления: 20 Октября 2021 года
Содержание статьи
Симптомы
Наиболее постоянные симптомы ушиба — боль и припухлость в области бедра, ограничение движений. При этом, чем тяжелее травма, тем более ограничена подвижность, выраженный отёк и боль. Максимальная болезненность возникает в точке удара, и может распространяться на переднюю, заднюю или боковую поверхность бедра. Бедро увеличено в объеме, контуры сглажены, ощупывание болезненное, наблюдается хромота.
На месте нарушения целостности сосудов образуются гематомы. Вначале место повреждения становится багровым или синюшным, позже на 3-4 сутки зелёным, на 5-7 день приобретает жёлтый оттенок. При гематомах, расположенных в области мышц и подфасциально цвет кожи может не меняться. При ушибах лёгкой степени симптомы проходят в течение 7-15 дней, тяжёлые травмы и средней степени тяжести сходят до месяца.
Диагностика
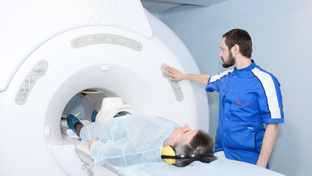
Диагностику ушиба тазобедренного сустава, бедра осуществляют специалисты из области травматологии и ортопедии. Врач проводит внешний осмотр, оценивает обширность и глубину травмы, качество и амплитуду движений, выясняет причину травмы. Для уточнения диагноза при ушибе, исключения костной патологии выполняют рентгенографию тазобедренного сустава, бедренной кости. Исследование позволяет подтвердить целостность костей, определить форму, размер и структуру исследуемого сустава, последствия травмы. При недостаточной информативности рентгенографии, так и для детального планирования лечебных мероприятий назначают артроскопию, компьютерную томографию или магнитно-резонансную томографию.
МРТ (магнитно-резонансная томография)
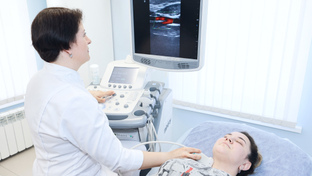
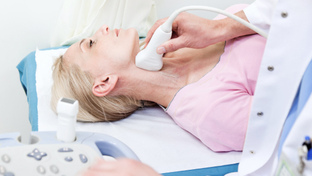
УЗИ (ультразвуковое исследование)
Дуплексное сканирование
Компьютерная топография позвоночника Diers
Компьютерная электроэнцефалография
Чек-ап (комплексное обследование организма)
Неотложная помощь
В первую очередь необходимо осмотреть пострадавшего, при необходимости вызвать бригаду скорой помощи. В первые часы или минуты после травмы важно приложить холод к месту повреждения. Это поможет снизить боль, интенсивность кровотечения, таким образом уменьшить объем гематомы. Далее наложить тугую повязку или эластичный бинт. При этом следует контролировать кровообращение, при изменении цвета кожи на синюшный ослабить повязку. При интенсивной боли до обращения за врачебной помощью или приезда скорой можно выпить обезболивающее.
Лечение
Лечение проводят амбулаторно, при тяжёлых ушибах пострадавшего госпитализируют. Больному назначают покой, возвышенное положение конечности, накладывают давящую повязку или гипсовую лонгету. Местно назначают охлаждающие, обезболивающие, противоотёчные мази. Некоторые пациенты в первые дни после травмы вынуждены использовать костыль, трость для передвижения.
На 2-3 сутки потребность в охлаждении отпадает, наоборот нужны тепловые процедуры для скорейшего рассасывания гематом. Показаны тепловые ванны, примочки, теплые сухие и спиртовые компрессы, согревающие мази, крема. Мази и компрессы не используют при нарушении целостности кожи (раны, ссадины, царапины) на месте травмирования. В восстановительном периоде применяют электрофорез, ультразвук, УФО-терапию, массаж, лечебную гимнастику.
Когда ушибы тазобедренного сустава сопряжены с невыносимой болью, пострадавшему назначают внутрь анальгетики, нестероидные противовоспалительные препараты. Дозировку и курс лечения подбирают индивидуально в случае конкретного пациента.
Если имеет место обширная гематома, заполненная большим количеством жидкости, сгустками крови или синовией под местной анестезией вскрывают полость, дренируют, проводят дезинфекцию, накладывают стерильную повязку. Может потребоваться повторная пункция.
Публикации в СМИ
Повреждения капсульно-связочного аппарата суставов
К повреждениям капсульно-связочного аппарата суставов относят растяжения, частичные и полные разрывы.
Причины — травмы, при которых происходит временное расхождение суставных поверхностей за пределы сустава, растяжение и возвращение в исходное положение связок.
Клиническая картина • Боль в области сустава, усиливающаяся при движении • Область сустава увеличена в объёме (кровоизлияние, отёк) • Нарушение функции.
Лечение • Покой — кратковременная иммобилизация гипсовой лонгетой или мягкой фиксирующей повязкой • Холод — в первые сутки, затем — тепло, УВЧ, фонофорез с гидрокортизоном, ЛФК, массаж • Новокаиновые блокады для снятия боли • При повреждениях связок суставов с нарушением их целости — иммобилизация гипсовой лонгетой в положении гиперкоррекции на 4–6 нед • При неэффективности консервативного лечения — хирургическое восстановление целостности связок.
МКБ-10 • T03 Вывихи, растяжения и повреждения капсульно-связочного аппарата суставов, захватывающие несколько областей тела • T09.2 Вывих, растяжение и повреждение капсульно-связочного аппарата суставов на неуточнённом уровне туловища • T14.3 Вывих, растяжение и повреждение капсульно-связочного аппарата сустава неуточнённой области тела • T11.2 Вывих, растяжение, деформация неуточнённых сустава и связки верхней конечности на неуточнённом уровне • T13.2 Вывих, растяжение и повреждение капсульно-связочного аппарата неуточнённого сустава нижней конечности на неуточнённом уровне
Код вставки на сайт
Повреждения капсульно-связочного аппарата суставов
К повреждениям капсульно-связочного аппарата суставов относят растяжения, частичные и полные разрывы.
Причины — травмы, при которых происходит временное расхождение суставных поверхностей за пределы сустава, растяжение и возвращение в исходное положение связок.
Клиническая картина • Боль в области сустава, усиливающаяся при движении • Область сустава увеличена в объёме (кровоизлияние, отёк) • Нарушение функции.
Лечение • Покой — кратковременная иммобилизация гипсовой лонгетой или мягкой фиксирующей повязкой • Холод — в первые сутки, затем — тепло, УВЧ, фонофорез с гидрокортизоном, ЛФК, массаж • Новокаиновые блокады для снятия боли • При повреждениях связок суставов с нарушением их целости — иммобилизация гипсовой лонгетой в положении гиперкоррекции на 4–6 нед • При неэффективности консервативного лечения — хирургическое восстановление целостности связок.
МКБ-10 • T03 Вывихи, растяжения и повреждения капсульно-связочного аппарата суставов, захватывающие несколько областей тела • T09.2 Вывих, растяжение и повреждение капсульно-связочного аппарата суставов на неуточнённом уровне туловища • T14.3 Вывих, растяжение и повреждение капсульно-связочного аппарата сустава неуточнённой области тела • T11.2 Вывих, растяжение, деформация неуточнённых сустава и связки верхней конечности на неуточнённом уровне • T13.2 Вывих, растяжение и повреждение капсульно-связочного аппарата неуточнённого сустава нижней конечности на неуточнённом уровне
Лечение ушибов мягких тканей
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Цель исследования: определить эффективность анальгетической терапии при ушибах мягких тканей верхней и нижней конечностей.
Материал и методы: проведено пилотное проспективное сравнительное исследование с участием 54 человек в возрасте 25–50 лет, из них 27 — с ушибом мягкий тканей плеча, 27 — с ушибом бедра. Ушибы у всех пациентов характеризовались образованием подкожного или внутрикожного кровоизлияния, отеком мягких тканей без повреждения мышц. Для оценки эффективности применения таблетированной и инъекционной форм кетопрофена и диклофенака в зависимости от локализации повреждения было сформировано 8 групп. Оценивали скорость наступления обезболивающего эффекта в 1-е сутки после получения травмы и динамику выраженности боли по визуальной аналоговой шкале, выраженность отека. Лечение и наблюдение за пациентами прекращали при достижении стойкого анальгезирующего эффекта, восстановлении функции конечности.
Результаты исследования: средний возраст пациентов составил 44,7 года. Соотношение мужчин и женщин было 1:1. Особенностью оценки болевого синдрома при первичном обращении явилось то, что пациенты с ушибом плеча оценивали боли на 2–3 балла выше, чем пациенты с ушибом бедра. При ушибах верхней конечности кетопрофен в таблетках начинал проявлять свою активность уже на 10-й минуте, при ушибах нижней конечности — на 20-й минуте. Инъекционная форма препарата обеспечивала выраженный обезболивающий эффект уже на 5-й минуте. Как таблетированная, так и инъекционная форма кетопрофена продемонстрировали преимущество перед диклофенаком. К 3–4-м суткам во всех случаях удавалось добиться полного купирования боли.
Заключение: настоящее пилотное исследование подтвердило эффективность и быстрое начало анальгетического действия кетопрофена в лечении ушибов мягких тканей.
Ключевые слова: ушиб, мягкие ткани, боль, анальгетическая терапия, кетопрофен, диклофенак
Для цитирования: Жуков Д.В., Устикова Н.В., Прохоренко В.М. Лечение ушибов мягких тканей. РМЖ. Медицинское обозрение. 2021;5(3):145-149. DOI: 10.32364/2587-6821-2021-5-3-145-149.
1 Novosibirsk State Medical University, Novosibirsk, Russian Federation
2 Novosibirsk Research Institute of Traumatology and Orthopedics named after Ya.L. Tsivyan,
Novosibirsk, Russian Federation
Background: soft tissue injuries accompany the patient’s life and make up the main number of visits to primary health care facilities. As a rule, contusions occur when falling or hitting hard objects and are inherently associated with pain.
Aim: to determine the analgesic therapy efficacy for soft tissue injuries of the upper and lower extremities.
Patients and Methods: a pilot prospective comparative study was conducted including 54 subjects aged 25–50 years (27 patients with shoulder contusion and 27 with hip contusion). Contusions in all patients were characterized by the formation of subcutaneous or intradermal hemorrhage and soft tissue edema without muscle damage. 8 groups were formed to assess the efficacy of the tablet and injection administration types of ketoprofen and diclofenac, depending on the location of the injury. The time of analgesic effect onset on the 1st day after the injury and the trend of pain severity were evaluated using a visual analog s cale, as well as edema severity. Treatment and follow-up of patients were discontinued when a persistent analgesic effect was achieved and the function of the limb was restored.
Results: the patients’ median age was 44.7 years. The ratio of men and women was 1:1. A feature of the pain syndrome assessment during the initial treatment was that patients with a shoulder contusion rated pain 2-3 points higher than patients with a hip contusion. In the upper limb contusions, ketoprofen in tablets activated already at the 10th minute, in the lower limb contusions – at the 20th minute. The drug injectable form provided a pronounced analgesic effect already at the 5th minute. Both the tablet and injectable forms of ketoprofen demonstrated a benefit over diclofenac. By the 3rd-4th day, it was possible to achieve complete pain relief in all cases.
Conclusion: this pilot study confirmed the efficacy and rapid onset of the ketoprofen analgesic effect in the treatment of soft tissue injuries.
Keywords: contusion, soft tissue, pain, analgesic therapy, ketoprofen, diclofenac.
For citation: Zhukov D.V., Ustikova N.V., Prokhorenko V.M. Treatment of soft tissue injuries. Russian Medical Inquiry. 2021;5(3):145–149. DOI: 10.32364/2587-6821-2021-5-3-145-149.
Введение
Повреждения мягких тканей сопровождают жизнь человека. Ушиб — это закрытое механическое повреждение мягких тканей, обусловленное кратковременным воздействием повреждающего фактора, которое не сопровождается образованием ран. При ушибе всегда происходит разрыв мелких сосудов с последующим кровоизлиянием, степень выраженности которого может быть различной. Повреждения мягких тканей, вне зависимости от причины, их вызвавших, составляют основное число обращений в учреждения первичного звена здравоохранения. Ушибы возникают, как правило, при падении или ударах о твердые предметы. У детей первых лет жизни преобладают бытовые, игровые травмы, ушиб мягких тканей лица и шеи. В более старшем возрасте основными видами травм являются транспортные, спортивные, уличные травмы [1]. Повреждение поверхностных мягких тканей всегда сопровождается отеком места повреждения в результате пропитывания кожи лимфой, кровью и местным асептическим воспалением. Величина отека зависит от площади повреждения подкожной клетчатки в месте ушиба. Так, например, в области свода черепа ввиду тонкого слоя подкожно-жировой клетчатки отек незначительный, тогда как даже слабые ушибы лица сопровождаются развитием выраженного отека [2]. Продолжающееся в глубине тканей кровотечение нередко приводит к дополнительной травме соседних тканей в результате их сдавливания, что сопровождается постепенным усилением боли и нарушением функции. Ушиб иногда сопутствует другим повреждениям (перелому и др.), поэтому всегда следует исключать более сложные повреждения и оценивать последствия травм [2, 3].
Травмы мягких тканей сопровождаются болью различной интенсивности. Так, при ушибах крупных нервов и их окончаний боль всегда резкая, простреливающая. При ушибах туловища и конечностей (плечо, бедро) могут формироваться напряженные гематомы, с распирающими болями, иногда с поверхностным онемением.
Лечение ушибов мягких тканей традиционно направлено на устранение вышеперечисленных симптомов и исключение более тяжелой патологии [4]. В настоящее время существуют стандарты лечения — клинические рекомендации по оказанию скорой медицинской помощи при повреждениях мягких тканей, где особое место отводится вопросам иммобилизации, туалету раны и обезболиванию [5]. Введение опиоидных и неопиоидных анальгетиков рекомендовано проводить в сочетании с антигистаминными препаратами (метамизолом натрия, тримеперидином, дифенгидрамином). Необходимо как можно раньше выполнить иммобилизацию. Даже при легких повреждениях лучше наложить на ушибленное место тугую повязку или выполнить иммобилизацию ортезом. Это обеспечит покой ушибленного сегмента, нормализует микроциркуляцию, уменьшит двигательную активность. Некоторые ортезные изделия обладают эффектом микромассажа, что тоже благотворно влияет на репаративные процессы. Вместе с этим проводится анальгезирующая терапия. Эти мероприятия необходимо выполнять в течение первых 3 сут. Затем возможно применение согревающих процедур, физиотерапевтических мероприятий. Местную терапию мазями и гелями возможно применять с 1-х суток, если они не обладают согревающим эффектом и не увеличивают проницаемость сосудов.
Функционирование ноцицептивной системы опосредовано нейрохимическими механизмами, реализуемыми эндогенными пептидами и медиаторами, среди которых гистамин, субстанция Р, кинины, простагландины, лейкотриены, ионы калия и водорода [4–6]. При боли активируются процессы гиперкоагуляции, пероксидного окисления липидов, увеличивается содержание протеолитических ферментов, что вызывает деструкцию тканей. Боль способствует развитию тканевой гипоксии, дистрофических процессов и нарушению микроциркуляции в тканях. Это, в свою очередь, усиливает альтерацию травмированных тканей [7].
Таким образом, боль является сложным психофизиологическим феноменом, который как с этической стороны, так и с позиции нормативно-правового регулирования требует лечения, направленного на облегчение боли [8]. Понимание сложности ее природы, механизмов развития и регулирования позволяет дифференцированно подходить к вопросу выбора анальгетической терапии.
К одним из наиболее эффективных средств защиты периферических ноцицепторов, не вызывающих депрессию витальных функций, относят нестероидные противовоспалительные препараты (НПВП). Современная концепция эффективного обезболивания ушибов и других видов травм предполагает мультимодальный подход — воздействие на различные звенья проведения болевой импульсации. В связи с этим целесообразно сочетать введение НПВП с опиатами или опиоидами при сильном болевом синдроме, например при шокогенных травматических повреждениях.
Нестероидные противовоспалительные препараты являются препаратами выбора при лечении легкой и умеренной боли. В основе их противовоспалительного действия лежит ингибирование циклооксигеназы (ЦОГ). Одним из представителей НПВП является кетопрофен, выпускаемый в различных формах (таблетированной, инъекционной, наружной). Тройной эффект — противовоспалительный, анальгезирующий и жаропонижающий — обусловлен блокированием ферментов ЦОГ-1 и ЦОГ-2 и, частично, липоксигеназы, что приводит к подавлению синтеза простагландинов (в т. ч. в ЦНС, вероятнее всего, в гипоталамусе) и тромбоксанов. Кетопрофен стабилизирует in vitro и in vivo липосомальные мембраны, при высоких концентрациях in vitro подавляет синтез брадикинина и лейкотриенов. Не оказывает отрицательного влияния на состояние суставного хряща [9].
С точки зрения соотношения противовоспалительной и анальгетической активности кетопрофен представляется оптимальной молекулой. Так, согласно данным экспериментального исследования с использованием модели зубной боли, кетопрофен обладает наиболее выраженным противовоспалительным эффектом по сравнению с многими НПВП, при этом показатель клинической эффективности (суммарное снижение боли через 4 ч) наибольший для кетопрофена [10]. Важно отметить, что эти экспериментальные данные были подтверждены данными метаанализа 13 РКИ: в отношении купирования умеренной и тяжелой боли кетопрофен существенно превосходит диклофенак и ибупрофен [11].
Несмотря на то, что кетопрофен является «традиционным» неселективным НПВП, он в меньшей степени способен вызывать НПВП-ассоциированные осложнения со стороны желудочно-кишечного тракта и сердечно-сосудистой системы — данные финского популяционного исследования по оценке причин развития 9191 события в верхних отделах ЖКТ (в т. ч. случаи крово-течения, язв и перфорации). Согласно полученным результатам вероятность развития серьезных осложнений со стороны ЖКТ при использовании кетопрофена была ниже в сравнении с другими НПВП, например диклофенаком. Кетопрофен демонстрировал аналогичный или даже меньший риск развития патологии ЖКТ, чем ряд селективных НПВП [9–11]. Минимальное негативное влияние кетопрофена на состояние сердечно-сосудистой системы продемонстрировано в ряде масштабных эпидемиологических исследований.
В исследовании анальгетического эффекта кетопрофена в острый период травмы у пострадавших с различными скелетными повреждениями было отмечено начало обезболивающего эффекта уже через 12,2±2,6 мин после внутримышечного применения 100 мг кетопрофена. Применение 200 мг позволило сократить ожидание развития анальгезии до 8,2±2,2 мин. При этом у больных с тяжелой скелетно-мышечной травмой кетонал применялся в дозе 200 мг в комбинации с внутривенным введением трамадола (100 мг), при этом обезболивающий эффект реализовывался через 5,8±0,9 мин, что было быстрее по сравнению с монотерапией трамадолом в той же дозировке (6,0±1,2 мин) [12].
Цель исследования: определить эффективность анальгетической терапии при ушибах верхних и нижних конечностей.
Материал и методы
Проведено пилотное проспективное сравнительное исследование, в которое включено 54 пациента с ушибом мягких тканей плеча (n=27) и бедра (n=27). Ушибы у всех пациентов характеризовались образованием подкожного или внутрикожного кровоизлияния, отеком мягких тканей без повреждения мышц. Критерии включения: возраст 25–50 лет, компенсированная коморбидная патология. Критерии невключения: декомпенсированная или требующая постоянной медикаментозной поддержки сопутствующая патология; тяжелые повреждения мягких тканей; давность повреждения более 1 сут; самостоятельный прием анальгезирующих и других медикаментозных средств с целью обезболивания до первичного посещения. Все пациенты подписывали информированное согласие на участие в исследовании.
При первичном осмотре всем больным выполнено УЗИ места повреждения для исключения более тяжелой патологии. Оценку отека мягких тканей определяли на каждом посещении по объему окружности поврежденного сегмента конечности, измеряя в верхней, средней и нижней трети, и сравнивали с неповрежденной конечностью. Восстановление функции оценивали по возможности выполнения пациентом сгибания в локтевом и плечевом суставе и приседания не менее 10 раз, а также удержания груза 2,5 кг более 2 мин в вытянутой руке.
В зависимости от получаемой формы препаратов пациенты были разделены на 8 групп. 1-я группа (n=6) — пациенты с повреждением верхней конечности, получавшие таблетки кетопрофена (Кетонал ® ) в дозировке 100 мг 1 р/сут; 2-я группа — пациенты с повреждением верхней конечности (n=6), получавшие таблетки диклофенака в суточной дозировке 100 мг; 3-я группа (n=7) — пациенты с повреждением нижней конечности, получавшие таблетки кетопрофена в дозировке 100 мг 1 р/сут; 4-я группа (n=7) — пациенты с повреждением нижней конечности, получавшие таблетки диклофенака в дозировке 100 мг; 5-я группа (n=7) — пациенты с повреждениями верхней конечности, в курации которых использовали инъекционную форму кетопрофена в суточной дозировке 100 мг; 6-я группа (n=7) — пациенты с повреждениями верхней конечности, в лечении которых использовали инъекционную форму диклофенака 100 мг; 7-я группа (n=7) — пациенты с повреждениями нижней конечности, получавшие кетопрофен в инъекциях в дозе 100 мг; 8-я группа (n=7) — пациенты с повреждениями нижней конечности и применением инъекционной формы диклофенака.
У всех пациентов помимо анальгезирующей терапии в 1-е сутки проводили иммобилизацию тугой повязкой места повреждения и применяли охлаждающие процедуры. При повторном визите (на 2-е сутки и далее ежедневно) оценивали интенсивность боли по ВАШ, выраженность отека. Лечение и наблюдение за пациентами прекращали при достижении стойкого анальгезирующего эффекта (по ВАШ), отсутствии нарастания отека мягких тканей, восстановлении функции конечности.
Результаты и обсуждение
Средний возраст пациентов составил 44,7 года. Соотношение мужчин и женщин было 1:1.
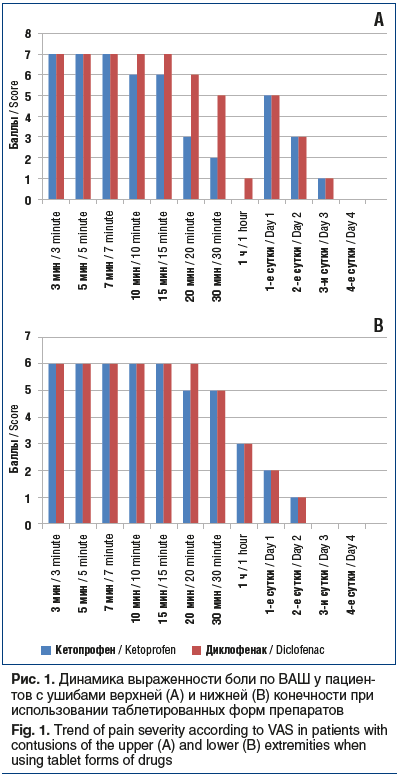
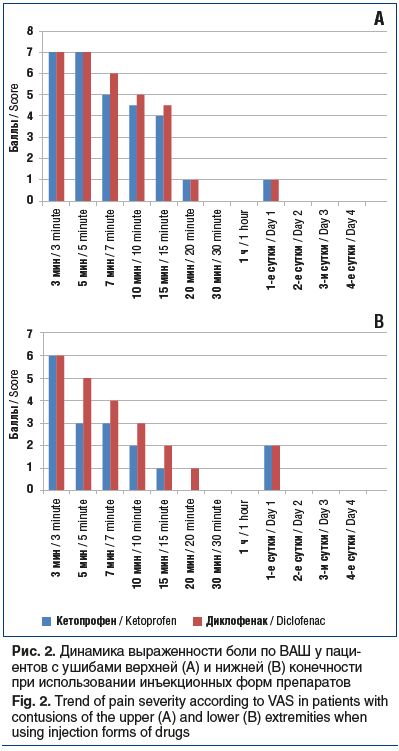
Как видно на рисунке 1, при ушибах верхней конечности кетопрофен в таблетках начинал проявлять свою активность уже на 10-й минуте, при ушибах нижней конечности — несколько позже, на 20-й минуте. Применение инъекционной формы (рис. 2) обеспечивало выраженный обезболивающий эффект уже на 5-й минуте. Как таблетированная, так и инъекционная форма кетопрофена продемонстрировали преимущество перед диклофенаком. К 3–4-м суткам во всех случаях удавалось добиться полного купирования боли. Продолжительность анальгезирующего действия препаратов не изучали ввиду большой психоэмоциональной составляющей и малой выборки пациентов. Особенностью оценки болевого синдрома при первичном обращении явилось то, что пациенты с ушибом плеча оценивали боли на 2–3 балла выше, чем пациенты с ушибом бедра (6–8 баллов).
Хотелось бы отметить, что, несмотря на эффективность инъекционной формы препарата, формой выбора для пациентов с повреждением руки, согласно опросу, оставалась таблетированная форма. У пациентов с повреждениями ноги предпочтительной оказалась инъекционная форма. Здесь приходится констатировать парадокс: при более выраженном болевом синдроме при ушибе верхней конечности более эффективная инъекционная форма используется значительно реже, чем у пациентов с повреждением нижней конечности.
Заключение
Таким образом, данное пилотное исследование подтвердило эффективность и быстрое начало анальгетического эффекта кетопрофена в лечении ушибов мягких тканей. Использование препарата позволяет полностью купировать болевой синдром в течение 3 сут. Полученные в рамках небольшой выборки данные дают основания расширить группу наблюдения для увеличения мощности исследования, сформировав клинические группы в зависимости от вида, степени повреждения и локализации травмы.
Сведения об авторах:
Жуков Дмитрий Викторович — к.м.н., доцент кафедры травматологии и ортопедии ФГБОУ ВО НГМУ Минздрава России; 630091, Россия, г. Новосибирск, Красный пр-т, д. 52; ORCID iD 0000-0002-4334-217X.
Устикова Нина Васильевна — врач-ревматолог ФГБУ «ННИТО им. Я.Л. Цивьяна» Минздрава России; 630091, Россия, г. Новосибирcк, ул. Фрунзе, д. 17.
Прохоренко Валерий Михайлович — д.м.н., профессор, заведующий кафедрой травматологии и ортопедии ФГБОУ ВО НГМУ Минздрава России; 630091, Россия, г. Новосибирск, Красный пр-т, д. 52; ведущий научный сотрудник ФГБУ «ННИТО им. Я.Л. Цивьяна» Минздрава России; 630091, Россия, г. Новосибирcк, ул. Фрунзе, д. 17.
Контактная информация: Жуков Дмитрий Викторович, e-mail: zhukdv@ngs.ru. Источник финансирования: публикация осуществлена при поддержке АО «Сандоз». Конфликт интересов: авторы получили вознаграждение за написание статьи. Никто из авторов не имеет финансовой заинтересованности в представленных материалах, методах и результатах. Статья поступила 22.03.2021, поступила после рецензирования 14.04.2021, принята в печать 28.04.2021.
Dmitry V. Zhukov — Cand. of Sci. (Med.), Associate Professor of the Department of Traumatology and Orthopedics, Novosibirsk State Medical University; 52, Krasnyi prospect, Novosibirsk, 630091, Russian Federation; ORCID iD 0000-0002-4334-217X.
Nina V. Ustikova — rheumatologist, Novosibirsk Research Institute of Traumatology and Orthopedics named after Ya.L. Tsivyan; 17, Frunze str., Novosibirsk, 630091, Russian Federation.
Valery M. Prokhorenko — Dr. of Sci. (Med.), Professor, Head of the Department of Traumatology and Orthopedics, Novosibirsk State Medical University; 52, Krasnyi prospect, Novosibirsk, 630091, Russian Federation; leading researcher of the Novosibirsk Research Institute of Traumatology and Orthopedics named after Ya.L. Tsivyan; 17, Frunze str., Novosibirsk, 630091, Russian Federation.
Contact information: Dmitry V. Zhukov, e-mail: zhukdv@ngs.ru. Financial Disclosure: this article was published with the support of JSC Sandoz. Conflict of interests: authors received a reward for preparing a paper. No authors have a financial or property interest in any material, method or results mentioned. Received 22.03.2021, revised 14.04.2021, accepted 28.04.2021.
Только для зарегистрированных пользователей